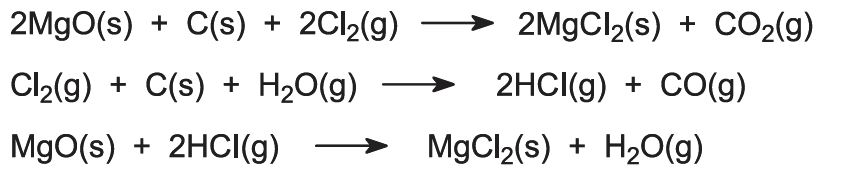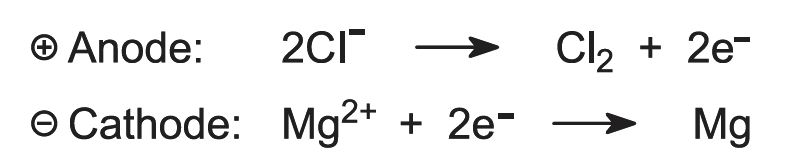Použití hořčíku
Hořčík je třetím nejpoužívanějším kovem ve stavebnictví (po železe a hliníku).
Téměř 70 % světové produkce hořčíku se používá k výrobě slitin, které mají velmi nízkou hustotu, poměrně vysokou pevnost a vynikající obrobitelnost. Tyto slitiny obsahují jeden nebo více prvků hliník, zinek, mangan nebo křemík v různém množství v závislosti na způsobu zpracování slitiny.
Polovina těchto slitin se používá k výrobě tlakových odlitků s přibližně 90 % hořčíku. Součásti automobilů, jako jsou jádra volantů, skříně převodovek, konstrukce přístrojových desek a podpěry chladičů, se často vyrábějí z vysokotlakých hořčíkových slitin litých pod tlakem.
Do některých slitin se přidává zirkonium a prvky vzácných zemin, aby byla slitina pevnější. Z této skupiny slitin se obvykle odlévají do písku díly, jako jsou převodovky vrtulníků a pomocné převodovky proudových motorů. Některé vysoce výkonné automobily jsou vyrobeny ze slitiny hořčíku, stejně jako pouzdra fotoaparátů.
Další polovina hořčíku používaného ve slitinách je jako legující přísada, v hliníkovém průmyslu. Slitiny se používají v obalech, zejména v nápojových (plechovkách) a ve fóliích na ochranu potravin.
Většina kovových nápojových plechovek vyráběných ve Spojených státech se vyrábí z hliníku legovaného asi 5 % hořčíku a malým množstvím dalších prvků. V Evropě a Asii obsahuje kovová plechovka přibližně 50 % oceli a 50 % slitiny hliníku, přičemž vrchní část tvoří slitina hliníku.
Slitiny hořčíku se používají také jako obětní anody. Po připojení k méně reaktivnímu kovu se hořčík stává anodou elektrického článku a koroduje přednostně před druhým kovem. Toho se využívá k ochraně trupů ocelových lodí a podvodních konstrukcí ropných plošin a potrubí před korozí.
Další velmi důležité využití hořčíku je při výrobě titanu. Tímto způsobem se využívá asi 10 % světové produkce hořčíku.
Dalších 10 % se používá při výrobě vysoce kvalitní oceli pro konstrukce, jako jsou velké budovy a mosty. Přidává se v roztaveném stavu do roztaveného železa, aby se chemickou reakcí odstranila síra, přičemž struska sulfidu hořečnatého se odvádí.
Možná jedno z nejznámějších, ale nejmenších použití hořčíku je v nouzových světlicích, ohňostrojích a jiných zápalných zařízeních. Obsahují velmi malé kousky hořčíku, které lze zapálit.
Roční výroba hořčíku
Tyto údaje se týkají primární výroby z rudy a nezahrnují sekundární výrobu z recyklovaných materiálů.
| Svět | 910 000 tun1 |
| Čína | 800 000 tun1 |
| USA. | 70 000 tun2 |
| Rusko | 30 000 tun1 |
| Izrael | 25 000 tun1 |
| Kazachstán | 20 000 tun1 |
Údaje pocházejí z:
1 U.S. Geological Survey, Mineral Commodity Summaries, 2016.
2 Poslední dostupný údaj je z roku 2012 (Minor Metals Trade Association, 2012)
V roce 1993 bylo množství hořčíku vyrobeného v Číně zanedbatelné (cca 5 %), o dvacet let později Čína nyní vyrábí téměř 90 % světové produkce hořčíku. Ačkoli má země bohatá ložiska vhodných hořčíkových rud, byl to právě rychlý hospodářský růst, který vedl ke zvýšené poptávce v zemi po výrobcích využívajících hořčíkové slitiny. To následně vedlo k uzavření závodů v mnoha zemích. Výrobní procesy spotřebovávají velmi velké množství energie, a z tohoto důvodu je výroba v mnoha zemích neekonomická. Hořčík se nyní v západní Evropě nevyrábí.
Výroba hořčíku
Hořčík se nachází v roztoku v mořské vodě (asi 1,3 kg m-3 hořčíku) a v přírodních solankách. Hojně se vyskytuje také v rudách magnezitu (MgCO3) a dolomitu (MgCO3.CaCO3).
Hořčík se vyrábí hlavně dvěma způsoby:
a) tepelnou redukcí oxidu hořečnatého
b) elektrolýzou chloridu hořečnatého
Před rozšířením výroby v Číně byla elektrolýza běžnějším způsobem výroby v zemích, kde se elektrická energie vyrábí relativně levně. Většina čínských závodů však používá aktualizovanou verzi procesu termické redukce, který byl původně vyvinut v Kanadě ve 40. letech 20. století za účelem zvýšení výroby během druhé světové války („Pidgeonův proces“).
(a) Proces termické redukce
Dolomitová ruda se rozdrtí a zahřeje v peci za vzniku směsi oxidů hořčíku a vápníku, což je proces známý jako kalcinace:
Dalším krokem je redukce oxidu hořečnatého. Redukčním činidlem je ferosilicium (slitina železa a křemíku), které se vyrábí zahříváním písku s koksem a železným šrotem a obvykle obsahuje asi 80 % křemíku.
Oxidy se smíchají s rozdrceným ferosiliciem a vyrobí se z nich brikety pro vložení do reaktoru. Může se také přidávat oxid hlinitý, aby se snížil bod tání strusky. Reakce probíhá při teplotě 1500 až 1800 K za velmi nízkého tlaku, blízkého vakuu. Za těchto podmínek vzniká hořčík jako pára, která se kondenzuje ochlazením na teplotu asi 1100 K v kondenzátorech s ocelovou výstelkou a poté se odebírá a odlévá do ingotů:
Přímá reakce je endotermická a poloha rovnováhy je ve prospěch oxidu hořečnatého. Odstraněním par hořčíku při jeho vzniku však reakce probíhá do konce. Oxid křemičitý se spojuje s oxidem vápenatým za vzniku roztavené strusky, křemičitanu vápenatého:
Postup dává hořčík s čistotou až 99,99 %, což je o něco více než u elektrolytických postupů.
(b) Elektrolytický postup
Mimo Čínu se obvykle upřednostňuje elektrolytický postup.
Postup zahrnuje dvě fáze:
i) výroba čistého chloridu hořečnatého z mořské vody nebo solanky
ii) elektrolýza taveného chloridu hořečnatého
(i) Výroba čistého chloridu hořečnatého z mořské vody nebo solanky
Pokud je surovinou mořská voda, upravuje se s dolomitem, který byl zahřátím na vysokou teplotu převeden na směsné oxidy. Hydroxid hořečnatý se vysráží, zatímco hydroxid vápenatý zůstává v roztoku. Hydroxid hořečnatý se odfiltruje a při zahřívání snadno vytvoří čistý oxid.
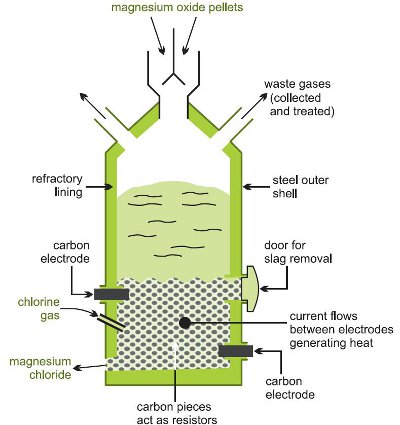
Přeměny na chlorid hořečnatý se dosáhne zahříváním oxidu smíšeného s uhlíkem v proudu chloru při vysoké teplotě v elektrické peci (obrázek 1).
Obrázek 1 znázorňující výrobu chloridu hořečnatého z oxidu hořečnatého.
Probíhá několik reakcí:
Pokud jsou zdrojem hořčíku solanky bohaté na chlorid hořečnatý, roztok se upravuje za účelem odstranění různých nečistot a zbývající roztok chloridu hořečnatého se zahušťuje odpařováním v několika stupních.
Poslední stupeň dehydratace musí být proveden za přítomnosti plynného chlorovodíku, aby se zabránilo hydrolýze chloridu hořečnatého:
V současné době se vyvíjí nový proces s použitím magnezitu. Malé kousky rudy se převádějí přímo na roztavený chlorid hořečnatý zahříváním chlorem v elektrické peci za přítomnosti oxidu uhelnatého.
(ii) Elektrolýza roztaveného chloridu hořečnatého
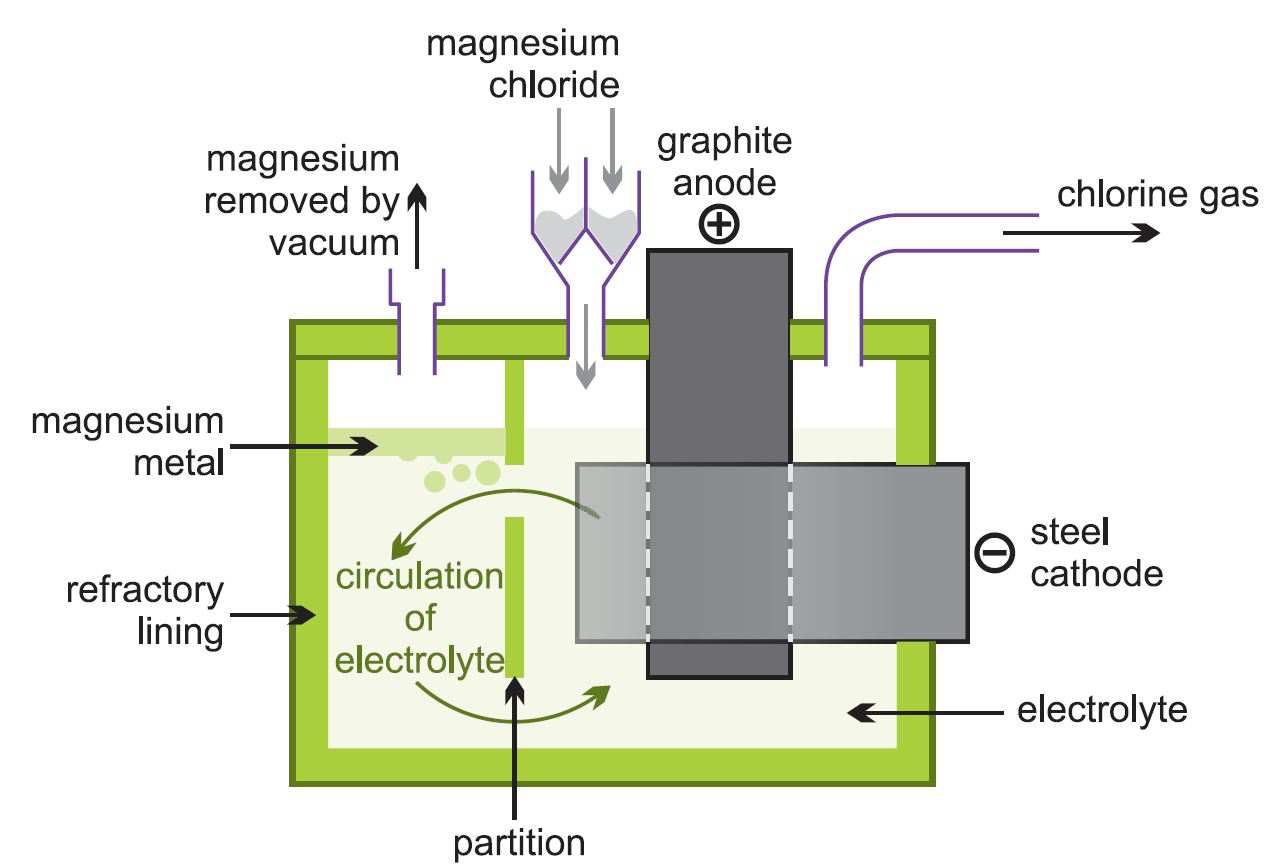
Vzniklý bezvodý chlorid hořečnatý se průběžně přivádí do elektrolytických cel (obrázek 2), které jsou dostatečně horké, aby jej roztavily.
Při elektrolýze vzniká hořčík a chlor:
Obrázek 2 znázorňující elektrolýzu chloridu hořečnatého.
Tavený kov se odebírá a odlévá do ingotů. Plynný chlor se recykluje do chlorovací pece.
Druhotná výroba
Pouze asi 3 % z celkového ročně použitého hořčíku pochází z recyklace, odhadem 23 000 tun.
.