Background
舌は非常に特殊で、口腔内の重要な器官である。 舌の一部または全部を切除すると、外科医は味覚、咀嚼、嚥下、および発声に対する重度の機能障害を回避、制限、または回復する必要があり、さまざまな困難が生じる。
発生学
舌は、発生から4週目に、盲腸孔より頭側の原始咽頭底にある間充織の腫脹であるインパール結節の出現により現れる。 舌の前方2/3は、第四咽頭結節の両側にできる2つの外側の膨らみ(第一咽頭弓に由来する)から形成される。 これらの舌芽は融合し、舌の中央溝を形成する。 舌の後方1/3は、舌小帯隆起の過成長部分から生じている。 舌小帯は第2咽頭弓の腹内側と第3咽頭弓の頭側の一部で形成される。 舌の上皮は前腸内胚葉から発生する。 舌筋の多くは後頭筋節から移動してきた筋芽細胞から発生する。 舌の結合組織、リンパ管、血管は咽頭弓間充織から発生する。
組織学
舌は咀嚼層扁平上皮で覆われる。
関連解剖学
総解剖学
前方から後方に、舌は先端、本体、底面の3つの面を持つ。 先端は舌の前方で可動性が高く、尖った部分である。 先端より後方は舌の本体で、背面(上面)と腹面(下面)があります(下図参照)
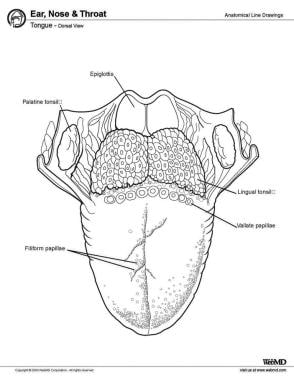 舌、背面図。
舌、背面図。 筋肉
人間の舌の8つの筋肉は、固有筋と外来筋に分類される。 4つの固有筋は、舌の形を変えるために働き、どの骨にも付着していません。 4つの外在筋は、舌の位置を変えるために働き、骨に固定されている。
血管供給
舌は主に外頚動脈の枝である舌動脈から血液供給を受けている。 口底部も舌動脈から血液を供給されている。 舌小帯筋の中間腱、舌小帯筋の後縁、舌下神経によって形成される三角形をPirogov-Belclard ‘s triangleと呼ぶことがある。 舌への二次的な血液供給は顔面動脈扁桃枝と上行咽頭動脈からである。
神経供給
舌前部3分の2の感覚は顔面神経(chorda tympani, CN VII)によって与えられる。 舌の前方2/3の一般的な感覚は、CN V3の枝である舌神経によって供給される。 舌咽神経 (CN IX) は舌の後1/3の一般的な感覚を提供する。 舌の内在筋と外在筋はすべて舌下神経 (CN XII) によって供給されているが、外在筋の1つである口蓋垂は咽頭神経叢のCN Xによって神経支配されている。
関連する解剖学の詳細については、舌の解剖学を参照してください。
嚥下の生理学
嚥下の開始は、食物ボーラスを口腔内に収容することから始まります。 その後、自由に動く舌が前口蓋に接触し、ボーラスを形成し、舌根を咽頭壁に向かって後方に移動させ、ボーラスを喉の奥に推進させることが可能になる。 舌骨と喉頭の上昇により上部食道括約筋が開き、ボーラスが通過する。
病理
扁平上皮癌(SCC)
舌癌の95%以上は扁平上皮癌(SCC)である。 舌の他のあまり一般的でない悪性腫瘍(腺癌、腺様嚢胞癌)および肉腫(歯槽軟部肉腫)についての治療の考察は、本章の範囲外である。 SCCに対する舌の部分切除術および全切除術で確立された原則は、他の悪性腫瘍にも一般的に適用できる。
舌のSCCは一般的に人生の5、6年目に発症し、男性に多く見られる。 喫煙タバコとエタノールの乱用は舌のSCCの発症と強く関連しており、タバコとエタノールの両方を乱用している患者は、がん発症リスクが6倍から15倍高くなる。
リンパ節転移
舌SCCのリンパ節転移は一般的に順序よく起こり、まず最上部(レベルI-II)、次に中部(レベルII-III)、最後に下部頸部リンパ節(レベルIV)を巻き込みます。 舌のリンパドレナージには、内頸部、胃下部、舌骨部、顎下および顎下リンパ節盆地(レベルI~III)が含まれる。
前方経路は口腔舌の先端を排出し、主にレベルIIIに排出される。 外側群は、先端から円乳頭まで舌背の外側1/3を排水し、顎下腺、内頸動脈結節盆地、時には顎下腺結節盆地(レベルI~III)にも排水する。 中央経路は舌の中央2/3を流出する。 これらの血管は顎下領域(レベルI)または舌下結節(レベルIII)を介して上部頸部鎖骨結節盆地に流出する。 正中線に接近した舌の原発病変は、この領域に有意なリンパの交差が存在するため、しばしば両側の結節性病巣にドレインする。
患者の評価
舌癌の評価のために来院した患者には、詳細な病歴と徹底した身体検査が必要である。 痛み、出血、耳痛、嚥下障害、構音障害などの症状の有無とその期間を確認する必要がある。
身体検査は、原発巣の範囲、頸部リンパ節転移の存在と位置、および原発巣の同時性スクリーニングを含む患者の治療前の状態を評価するために実施される。
舌病変の生検は通常、臨床の場で局所麻酔で行うことができ、正式な汎内視鏡検査では全身麻酔で行うこともできる。 触知可能な頸部腫瘤または大きな転移性頸部リンパ節は、通常、細針吸引生検が可能である。 超音波ガイド下穿刺は、頸部疾患の診断が困難な場合にしばしば用いられ、従来の穿刺と比較して優れた感度と特異性を有すると報告されている。
画像診断
コンピュータ断層撮影
舌癌のX線検査で最もよく用いられるのは、静脈内造影によるコンピュータ断層撮影(CT)である。 造影CTは原発巣の3次元的な評価を可能にし、関連する解剖学的構造および局所浸潤の範囲に関する貴重な情報を提供する。 一般に、進行した舌のSCCと診断された患者は、肺転移を評価するために胸部の造影CTも受けるべきである。
臨床的にN0、肥満、または以前に照射した頸部の転移性疾患を評価する場合、CTは依然として選択すべきイメージングモダリティである。
磁気共鳴画像法
磁気共鳴画像法(MRI)はCTと比較して優れた軟組織解像度を提供する。 軟部原発病変の拡大診断精度の向上、および頸部リンパ節病期分類の精度向上により、頭頸部悪性腫瘍に対するルーチンMRIスキャンを推奨する著者もいる。 MRIは、原発腫瘍の浸潤範囲の評価が必要な場合に、従来のCTスキャンよりも優れた精度を有する優れた画像診断手段である。 舌や口腔底に位置する大きな病変で、歯や骨の断層像のアーチファクトを受けやすいものは、特にMRIに適している。 MRIは、神経周囲浸潤を示す症例に特に有用であり、これらの病変における病変の進展に関する精度を向上させることができる。 この精度の向上にもかかわらず、CTの場合と同様に、MRIは微小転移病変を検出するには不十分である。
Positron Emission Tomography(PET)は、癌と同様に代謝活性細胞を検出するために放射標識トレーサー(18-FDG)を使用する機能画像技術である。 PETは、頭頸部悪性腫瘍の検出、治療後の腫瘍の監視、頸部/遠隔転移性疾患の評価において精度(真陽性)を高めています。
進行期の原発巣がわかっている場合、PETはCTやMRIに比べてほとんど利点はない。 PETは原発巣の範囲を評価するには解像度が劣るため、診断精度を上げるためにはCTと併用する必要がある。 現在、検出限界は約5mmの解像度に相関している。 PETは早期病変のN0頸部の評価に大きな期待が持てるが、進行した舌癌の患者では、頸部の状態は予後的な意義しかない。
内視鏡検査
舌癌の評価では内視鏡(直接喉頭鏡、食道鏡、気管支鏡)はしばしば有用である。 原発腫瘍の範囲、特に正中線、舌根部、および下顎との関係が評価される。 組織学的診断がまだ確立していない場合は、全周性内視鏡検査時に生検を実施する。 パネンドスコピーはまた、同時性悪性腫瘍の除外にも用いられる。
舌のSCC病期分類
頭頸部悪性腫瘍の評価を受けるすべての患者は、以下に示す口腔病変に対する米国がん合同委員会(AJCC)のTNM病期分類に従って病期分類することが推奨される。
AJCC TNM分類: 口腔内SCCA
原発腫瘍(T)
-
TX -原発腫瘍は評価不能
-
T0 -原発腫瘍は評価不能
-原発腫瘍は評価不能 -原発腫瘍は評価不能 原発巣を認めない
-
Tis – Carcinoma in situ
-
T1 – (注)原発巣がある場合は、原発巣がないことを示す。 最大径2cm以下の腫瘍
-
T2 – 最大径2cm以上4cm以下の腫瘍
-
T3 – 最大径4cm以上の腫瘍
-
T4 (唇) – 皮質骨から侵入した腫瘍です。 下歯槽神経、口腔底、または顔面(顎または鼻)の皮膚
-
T4a (口腔)-腫瘍は皮質骨を通して侵入する。 舌(舌小帯、舌下帯、口蓋垂、舌小帯)の深層筋、上顎洞、顔面皮膚
-
T4b – 腫瘍は咀嚼筋腔、翼状片に浸潤。 または頭蓋底、および/または内頸動脈を包む
所属リンパ節(N)
-
NX -。 所属リンパ節の評価ができない
-
N0 – 所属リンパ節転移なし
-
N1 – 同側リンパ節1個に転移あり。 最大径3cm以下
-
N2 – 同側の単一リンパ節に転移、最大径3cm以上、6cm以下。 または両側または対側のリンパ節への転移で、最大径が6cmを超えないもの
-
N2a – 同側リンパ節への転移で最大径が3cmを超え6cm以下
-
N2b – 同側リンパ節転移で複数あるもの。 最大径が6cmを超えないもの
-
N2c – 両側または対側のリンパ節に転移があるもの。 最大径6cm以上のものはない
N3 – 最大径6cm以上のリンパ節への転移
遠隔転移 (M)
-
MX -。 遠隔転移を評価できない
-
M0 – 遠隔転移なし
-
M1 – 遠隔転移
AJCC Staging System.による遠隔転移の判定ができない
– 遠隔転移の判定ができない
病期分類
予後に影響する因子
腫瘍厚
一般に腫瘍サイズと厚さの増加は生存率の低下を著しく予測し、局所再発の割合が増加する。 早期の口腔癌患者における腫瘍の厚みと浸潤のパターンを測定することで、より侵攻性の高い疾患を有する患者を特定することができるかもしれない。 腫瘍径が1.5cm以上または腫瘍厚が5mm以上の患者は、その後、頸部リンパ節転移のリスクが高まるため、病期にかかわらず、より積極的な補助療法と選択的頸部郭清を検討することができる。
組織学的評価が標準であるが,MRIは口腔内SCCの腫瘍厚を決定するのに十分な精度を有している。 腫瘍の厚みは、局所リンパ節転移や生存率の低下を確実に予測しますが、口腔SCC患者の予後に関する要因は多岐にわたるため、腫瘍の厚みに基づいた具体的な治療戦略はまだ評価されていません。 進行期口腔内SCC(ステージIII、IV)の場合、腫瘍の深さは通常5mmを超えるため、治療計画において腫瘍の厚さは一般的に考慮されず、患者は一般的にネオアジュバントおよび/またはアジュバント化学放射線療法を伴う積極的な外科手術を受けている。
神経周囲浸潤
神経周囲浸潤は局所再発および頸部転移のリスク上昇と関連しており、一般に口腔SCC患者の生存の独立した予測因子であると考えられている。 末梢神経への浸潤がわずかであっても、生存率の低下と関連している。 病理学的に確認された場合、局所再発に関連した治療成績は不良であるため、原発腫瘍を治療するための術後放射線治療のフルコースを強く考慮する必要がある。
切除断端陽性
切除断端陽性による微小残存腫瘍は,頭頸部のSCC治療において局所再発と死亡を統計的に増加させる。 一次治療として手術を受けた患者は、切除断端が陰性であれば、局所制御率が有意に改善することが示された。 進行した口腔内原発SCCの切除を行う外科医は、切除断端が陽性となる可能性を最小限にするため、最低でも1cm、できれば2~3cmの切除断端を確保するよう努力すべきである。 原発巣や頸部郭清後の頸部で切除断端が陽性であれば、術後放射線療法を実施し、治療成績を向上させることが必要である。 術後放射線治療(62.5Gy以上)を受けた切除断端陽性患者の2年無病生存率は33.6%から75.6%に改善したことが報告されている。
頸部転移
頸部リンパ節転移の存在は、舌SCCにおける生存率の低下と局所再発を予兆する最も重要な因子として繰り返し引用されてきた。 さらに、頸部のより遠いレベル(レベルIII/IV)、または対側の頸部にある頸部リンパ節転移は、生存率を有意に低下させる傾向がある。 頸部リンパ節転移を認めない患者さんと、リンパ節転移を認める患者さんを比較した場合、全体の5年生存率はそれぞれ42.8%と17.5%と報告されています。 進行期口腔内SCCの患者さんは、一般的にリンパ節転移を有すると定義されています。
被膜外進展
被膜外進展を示す頸部リンパ節転移は、統計的に全生存率を低下させることが知られています。 結節外進展の存在は、治療後の子宮頸部再発にも関係する。 進行期の舌のSCCでは、広範な頸部リンパ節病変を呈することがあり、その場合、被膜外進展の可能性が高くなる。 多発性リンパ節に被膜外進展を認める患者は、一般に予後が極めて不良である。
治療計画における決定因子
腫瘍厚
一般に、腫瘍サイズと厚さの増大は生存率の低下を著しく予測し、局所再発の割合を増加させる。 早期の口腔癌患者における腫瘍の厚みと浸潤のパターンを測定することで、より侵攻性の高い疾患を有する患者を特定することができるかもしれない。 腫瘍径が1.5cm以上または腫瘍厚が5mm以上の患者は、その後、頸部リンパ節転移のリスクが高まるため、病期にかかわらず、より積極的な補助療法と選択的頸部郭清を検討することができる。
組織学的評価が標準であるが,MRIは口腔内SCCの腫瘍厚を決定するのに十分な精度を有している。 腫瘍の厚みは局所リンパ節転移と生存率の低下を確実に予測するが,口腔内SCC患者の予後に関連する因子が多岐にわたるため,腫瘍の厚みに基づく特定の治療戦略はまだ評価されていない。 進行期口腔内SCC(ステージIII、IV)の場合、腫瘍の深さは通常5mmを超え、患者は一般的にネオアジュバントおよび/またはアジュバント化学放射線療法を伴う積極的な手術を受けるため、一般的に治療計画において腫瘍厚さは考慮されない。
神経周囲浸潤
神経周囲浸潤は局所再発および頸部転移のリスク上昇と関連しており、一般に口腔SCC患者の生存の独立予測因子であると考えられている。 末梢神経への浸潤がわずかであっても、生存率の低下と関連している。 病理学的に確認された場合、局所再発に関連した治療成績は不良であるため、原発腫瘍を治療するための術後放射線治療のフルコースを強く考慮する必要がある。
切除断端陽性
切除断端陽性による微小残存腫瘍は,頭頸部のSCC治療において局所再発と死亡を統計的に増加させる。 一次治療として手術を受けた患者は、切除断端が陰性であれば、局所制御率が有意に改善することが示された。 進行した口腔内原発SCCの切除を行う外科医は、切除断端が陽性となる可能性を最小限にするため、最低でも1cm、できれば2~3cmの切除断端を確保するよう努力すべきである。 原発巣や頸部郭清後の頸部で切除断端が陽性であれば、術後放射線療法を実施し、治療成績を向上させることが必要である。 術後放射線治療(62.5Gy以上)を受けた切除断端陽性患者の2年無病生存率は33.6%から75.6%に改善したことが報告されている。
頸部転移
頸部リンパ節転移の存在は、舌SCCにおける生存率の低下と局所再発を予兆する最も重要な因子として繰り返し引用されてきた。 さらに、頸部のより遠いレベル(レベルIII/IV)、または対側の頸部にある頸部リンパ節転移は、生存率を有意に低下させる傾向がある。 頸部リンパ節転移を認めない患者さんと、リンパ節転移を認める患者さんを比較した場合、全体の5年生存率はそれぞれ42.8%と17.5%と報告されています。 進行期口腔内SCCの患者さんは、一般的にリンパ節転移を有すると定義されています。
被膜外進展
被膜外進展を示す頸部リンパ節転移は、統計的に全生存期間を短縮させることが知られています。 結節外進展の有無は、治療後の頸部再発にも関係する。 進行期の舌のSCCでは、広範な頸部リンパ節病変を呈することがあり、その場合は、被膜外進展の可能性が高くなる。 多発性リンパ節に被膜外進展を認める患者は、一般に予後が極めて不良である。