Amide dimerisieren stärker als Imide, obwohl sie weniger sauer sind. Dieses unerwartete Ergebnis wurde mit der Jorgensen-Sekundärwechselwirkungs-Hypothese (JSIH) begründet, die die Zuschauer- (C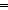 OS) und H-gebundenen (C
OS) und H-gebundenen (C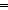 OHB) Carbonylgruppen in Imiden einbezieht. Ungeachtet der zahlreichen experimentellen und theoretischen Belege, die die JSIH stützen, gibt es einige rechnerische Studien, die darauf hindeuten, dass es andere relevante intermolekulare Wechselwirkungen geben könnte als die, die in diesem Modell berücksichtigt werden. Wir vermuteten, dass die Spektator-Carbonylgruppen die resonanzunterstützten Wasserstoffbrückenbindungen in Imiddimeren stören könnten, aber unsere Ergebnisse zeigten, dass dies nicht der Fall war. Aus Interesse an diesem Phänomen untersuchten wir die Selbstassoziation einer Reihe von Amiden und Imiden mittels1H-NMR, 1H-DOSY-Experimenten, DFT-Berechnungen, topologischen QTAIM-Analysen der Elektronendichte und IQA-Partitionen der Elektronenenergie. Diese Analysen ergaben, dass es in der Tat Abstoßungen des Typs OS⋯OHB in Übereinstimmung mit dem JSIH gibt, aber unsere Daten deuten auch darauf hin, dass die C
OHB) Carbonylgruppen in Imiden einbezieht. Ungeachtet der zahlreichen experimentellen und theoretischen Belege, die die JSIH stützen, gibt es einige rechnerische Studien, die darauf hindeuten, dass es andere relevante intermolekulare Wechselwirkungen geben könnte als die, die in diesem Modell berücksichtigt werden. Wir vermuteten, dass die Spektator-Carbonylgruppen die resonanzunterstützten Wasserstoffbrückenbindungen in Imiddimeren stören könnten, aber unsere Ergebnisse zeigten, dass dies nicht der Fall war. Aus Interesse an diesem Phänomen untersuchten wir die Selbstassoziation einer Reihe von Amiden und Imiden mittels1H-NMR, 1H-DOSY-Experimenten, DFT-Berechnungen, topologischen QTAIM-Analysen der Elektronendichte und IQA-Partitionen der Elektronenenergie. Diese Analysen ergaben, dass es in der Tat Abstoßungen des Typs OS⋯OHB in Übereinstimmung mit dem JSIH gibt, aber unsere Daten deuten auch darauf hin, dass die C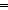 OS-Gruppe eine allgemeine Anziehung mit dem wechselwirkenden Molekül ausübt. Stattdessen fanden wir Korrelationen zwischen der Selbstassoziationsstärke und einfachen Brønsted-Lowry-Säure/Base-Eigenschaften, nämlich N-H-Aziditäten und C
OS-Gruppe eine allgemeine Anziehung mit dem wechselwirkenden Molekül ausübt. Stattdessen fanden wir Korrelationen zwischen der Selbstassoziationsstärke und einfachen Brønsted-Lowry-Säure/Base-Eigenschaften, nämlich N-H-Aziditäten und C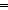 O-Basizitäten. Die Ergebnisse in CDCl3 und CCl4 deuten darauf hin, dass Imide aufgrund der geringeren Basizität ihrer Carbonylfragmente weniger stark dimerisieren als strukturell verwandte Amide – ein Aspekt, der bei der Untersuchung von H-Bindungen häufig übersehen wird. Insgesamt könnte das hier vorgeschlagene Modell wichtige Erkenntnisse in verschiedenen Bereichen der supramolekularen Chemie liefern, wie z. B. bei der Untersuchung von Addukten mit multiplen Wasserstoffbrückenbindungen, an denen funktionelle Amid- oder Imidgruppen beteiligt sind.
O-Basizitäten. Die Ergebnisse in CDCl3 und CCl4 deuten darauf hin, dass Imide aufgrund der geringeren Basizität ihrer Carbonylfragmente weniger stark dimerisieren als strukturell verwandte Amide – ein Aspekt, der bei der Untersuchung von H-Bindungen häufig übersehen wird. Insgesamt könnte das hier vorgeschlagene Modell wichtige Erkenntnisse in verschiedenen Bereichen der supramolekularen Chemie liefern, wie z. B. bei der Untersuchung von Addukten mit multiplen Wasserstoffbrückenbindungen, an denen funktionelle Amid- oder Imidgruppen beteiligt sind.