Le chlorure est l’anion le plus abondant dans le compartiment du liquide extracellulaire (FEC). L’hyperchlorémie est définie comme une augmentation de la concentration de chlorure dans l’eau du plasma. L’hyperchlorémie et un excès relatif de chlorure dans l’organisme ont été associés à l’apparition d’un débit sanguin rénal réduit,1,2 d’un œdème interstitiel accru, notamment dans les reins et le système gastro-intestinal,3 d’une morbidité et d’une mortalité excessives chez les patients gravement malades,4,5 et d’une survie et d’une récupération réduites chez les patients souffrant de lésions rénales aiguës.6 Comme le sodium et d’autres substances chimiques dans le compartiment du liquide extracellulaire, la concentration de chlorure est régulée. L’organe responsable du maintien de l’équilibre du chlorure dans l’organisme est le rein. Cet article passe en revue la manipulation du chlorure par le rein et les situations cliniques dans lesquelles une hyperchlorémie peut se produire.
Manipulation rénale du chlorure
Le niveau du chlorure dans le plasma est régulé par le rein. Le rein filtre librement le chlorure à travers les membranes basales des glomérules. La quantité de chlorure qui est excrétée dans l’urine est déterminée par le chlorure filtré par les glomérules et par une série de processus de transport qui se produisent le long du néphron. Dans des circonstances normales, plus de 60 % du chlorure filtré est absorbé le long du tubule proximal. Dans le premier tubule proximal, le sodium est absorbé avec une quantité proportionnelle d’eau, de sorte que la concentration de sodium ne change pas. En revanche, le bicarbonate et les autres anions non chlorure sont rapidement absorbés avec le sodium et éliminés du filtrat7 (Fig. 1A). Au fur et à mesure que le sodium et les anions non chlorure sont absorbés dans les premiers segments du tubule proximal (S1 et S2), la concentration de chlorure dans la lumière du tubule proximal augmente. Lorsque le liquide tubulaire atteint le dernier segment du tubule proximal (S3), la concentration de chlorure est élevée par rapport à sa concentration plasmatique, ce qui permet l’absorption passive du chlorure le long de son gradient de concentration (Fig. 1B). La perméabilité transépithéliale pour le chlorure est plus élevée que la perméabilité pour le bicarbonate, de sorte que malgré le gradient péritubulaire-lumière pour le bicarbonate, le transport de chlorure quittant la lumière dépasse celui du bicarbonate entrant dans le fluide tubulaire.

(A) Dans le tubule proximal précoce, l’absorption isotonique du sodium se produit avec les solutés organiques, le bicarbonate, le phosphate ainsi que l’eau, ce qui entraîne une augmentation de la concentration en chlorure. (B) La concentration élevée de chlorure dans la lumière favorise également le transport transcellulaire et paracellulaire. Les jonctions intercellulaires dans le dernier tubule proximal deviennent plus perméables au chlorure, ce qui facilite le transport paracellulaire. Même lorsque la concentration de bicarbonate diminue dans la lumière, l’échange Na+-H+ continue de jouer un rôle dans la réabsorption du NaCl. L’absorption transcellulaire du chlorure de sodium peut se produire via le couplage de l’échange Na+-H+ avec l’échange chlorure-anion organique (formate, oxalate). L’acide organique (acide formique ou oxalique) est recyclé dans les cellules.
Dans la partie précoce du tubule proximal, l’absorption du chlorure se produit également via des échangeurs chlorure-anion (formate, oxalate, base) apicaux et il sort de la cellule via des transporteurs membranaires basolatéraux8 (Fig. 1B). En cas d’acidose métabolique hyperchlorémique due à une charge en HCl- ou en chlorure d’ammonium, la réabsorption du chlorure dans le tubule proximal est réduite, en partie, en raison de la réduction des transporteurs d’anions organiques qui facilitent le transport du chlorure de sodium9 ainsi que de la réduction du gradient lumen/péritubulaire pour le chlorure.
La branche ascendante épaisse de l’anse de Henle (TALH) est un site important pour la réabsorption du chlorure10. A ce site, le sodium, le potassium et le chlorure sont transportés simultanément via un co-transporteur sodium-potassium-2 chlorure (NKCC2) (Fig. 2). Le chlorure entre dans la cellule TALH et quitte son aspect basolatéral par un canal chlorure électrogène ou par le co-transporteur chlorure de potassium électroneutre. Le mouvement du chlorure à travers le canal chlorure basolatéral (CLC-NKB) contribue à la génération d’un gradient de potentiel transépithélial positif (lumen) à négatif (basolatéral). Le potentiel positif intracellulaire qui serait généré par le mouvement du chlorure hors de la cellule est contrebalancé par la Na+-K+ ATPase électrogène basolatérale qui transporte le sodium hors de la cellule en échange du potassium dans la cellule dans un rapport 3-2. Les canaux potassiques ROMK sur la membrane apicale de la cellule TALH contribuent au potentiel positif de la lumière (négatif intracellulaire) par le mouvement conductif des ions potassium de la cellule vers la lumière. L’effet global est que le chlorure, le sodium et le potassium entrent dans la cellule via NKCC2 et, pour la plupart, le chlorure sort de la cellule via le canal chlorure ClC-NKB basolatéral, le sodium sort de la cellule via la Na+-K+ ATPase et le potassium se recycle dans la lumière via le canal ROMK ou sort basolatéralement via le co-transporteur KCl. Le couplage étroit entre le transport du sodium et du chlorure dans le TALH est mis en évidence par l’une des variétés du syndrome de Bartter dans laquelle des défauts dans les canaux chlorure basolatéraux perturbent la réabsorption du chlorure de sodium et imitent le défaut rénal observé avec des protéines NKCC2 anormales. Bien que d’autres transporteurs du côté péritubulaire de la cellule TAL, comme le co-transporteur KCl, transportent le chlorure d’une manière indépendante du sodium, la majeure partie du chlorure absorbé par le TALH est couplée à la réabsorption du sodium. Par conséquent, les facteurs qui augmentent la réabsorption du sodium dans ce segment augmenteront également la réabsorption du chlorure.
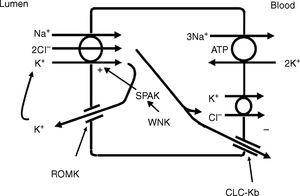
L’épais membre ascendant de l’anse de Henle absorbe le chlorure par le cotransporteur apical Na+-K+-2Cl- (NKCC2) et la sortie du chlorure de la cellule par un canal chlorure basolatéral et par le cotransport K+-Cl-. Le recyclage du K+ dans la lumière et la sortie conductrice basolatérale du Cl- par le CLC-Kb contribuent au gradient transépithélial positif-négatif de la lumière vers le basolatéral. Le chlorure intracellulaire peut réguler le transport de NKCC2 par le biais d’une kinase WNK sensible au chlorure (WNK) qui peut activer la kinase riche en proline/alanine liée à STE20/SPS1 (SPAK) et NKCC2 lorsque le Cl- intracellulaire est faible. D’autre part, lorsque le chlorure s’accumule dans la cellule en raison de défauts dans la voie de sortie du canal chlorure basolatéral, le transport de NKCC2 est bloqué. Lorsque NKCC2 est stimulé, par exemple par l’hormone antidiurétique, l’entrée de chlorure est augmentée, mais la conductance Cl basolatérale est également augmentée.
Dans le tubule contourné distal, le sodium et le chlorure sont transportés de la lumière dans la cellule par un cotransporteur sodium-chlorure (NCC)11 (figure 3). La force motrice du mouvement du chlorure de la lumière vers les cellules provient du gradient de sodium de la lumière vers les cellules qui est généré par la Na+-K+ ATPase basolatérale qui pompe le sodium hors de la cellule, maintenant ainsi de faibles concentrations de sodium intracellulaire. Une régulation supplémentaire du NCC et du NKCC peut se produire par l’intermédiaire des kinases WNK, qui peuvent servir de capteurs de chlorure12 et réguler ces transporteurs en modifiant leur trafic ou leur état de phosphorylation.13 Dans les parties ultérieures du tubule contourné distal, un potentiel lumineux négatif généré par le mouvement du sodium à travers le canal sodique épithélial apical (ENaC) peut également servir de force motrice pour la réabsorption passive de chlorure. Ainsi, les segments du tubule contourné distal présentent un couplage direct du transport du sodium et du chlorure via le NCC et un couplage indirect du transport via un mouvement passif vers le bas d’un gradient électrochimique.
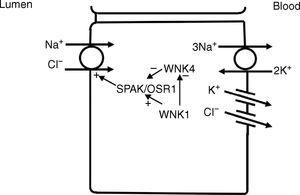
Dans le tubule contourné distal, le sodium et le chlorure présents dans la lumière sont absorbés par la cellule via un cotransporteur Na+-Cl- (NCC). Le transport par le NCC est entraîné par un faible taux de sodium intracellulaire généré principalement par la Na+-K+ ATPase basolatérale. La kinase WNK1 peut servir de capteur de chlorure pour bloquer l’inhibition du NCC par la kinase WNK4.
Le canal collecteur joue un rôle important dans la détermination de la teneur en chlorure de l’urine finale. La réabsorption du chlorure dans cette portion du néphron permet de conserver le chlorure en réponse à un apport faible en chlorure et peut contribuer aux effets hypertensifs d’un régime riche en chlorure de sodium. La majeure partie du sodium qui est réabsorbé dans le canal collecteur se produit dans les cellules principales par l’intermédiaire des canaux sodiques épithéliaux apicaux régulés par l’aldostérone. La réabsorption du chlorure dans le canal collecteur peut se produire par l’absorption paracellulaire du chlorure qui est entraînée par le potentiel transépithélial négatif de la lumière généré par le flux de sodium de la lumière vers la cellule par l’intermédiaire des ENaC (Fig. 4A). En outre, dans les cellules intercalaires de type B et de type non-A non-B, le chlorure peut être transporté par la pendrine, un échangeur chlorure-bicarbonate, le chlorure passant de la lumière à la cellule tandis que le bicarbonate est sécrété dans la lumière (Fig. 4B). La relation entre les différents processus de transport du sodium et du chlorure dans cette partie du néphron a été illustrée dans un article récent de Vallet et ses collègues.14 Les auteurs ont effectué un certain nombre de manœuvres physiologiques pour déterminer leurs effets sur les niveaux de protéines ENaC et pendrine dans le rein. Une charge de NaCl à long terme a diminué de manière significative les niveaux de protéines de la pendrine alors qu’il y avait une diminution de la soumission ENaC-γ » active » et une augmentation de la sous-unité β. Une dissociation entre le transport du sodium et du chlorure a été observée, cependant, avec l’inhibition du co-transporteur sodium-chlorure avec l’hydrochlorothiazide, les niveaux de pendrine ont diminué mais les niveaux d’ENaC ont augmenté. La restriction en NaCl a augmenté l’expression de la pendrine.15 Une concentration luminale accrue de bicarbonate qui serait créée par la sécrétion de bicarbonate médiée par la pendrine affecte la réabsorption du sodium en augmentant l’activité des ENaC en aval.16 Le transport du chlorure de sodium par les cellules intercalaires peut également être amélioré par la présence d’un échangeur chlorure-bicarbonate sodium-dépendant apical sensible aux thiazides (NDCBE, Slc4A8) qui transporte 1 ion sodium et 2 ions bicarbonate de la lumière dans la cellule en échange d’un ion chlorure qui quitte la cellule. Si le transport de NDCBE est couplé à l’échange chlorure-bicarbonate médié par la pendrine, les deux transporteurs travaillant ensemble pourraient entraîner une réabsorption nette de chlorure de sodium de la lumière, car le bicarbonate se recycle dans et hors de la cellule tandis que le sodium et le chlorure entrent dans la cellule17 (Fig. 4B). Les facteurs qui modifient le rapport entre les quantités ou les activités de ces deux échangeurs d’anions peuvent déterminer l’impact net sur la sécrétion de bicarbonate et la réabsorption de chlorure. Un autre transporteur qui peut être impliqué dans l’excrétion d’un excès de chlorure dans le corps est le transporteur Slc26A9 qui peut agir comme un canal de chlorure dans les parties médullaires du canal collecteur.18 Il peut modifier l’impact des charges de chlorure en augmentant la sécrétion de chlorure dans des conditions d’excès de chlorure. Le knock-out de ce gène entraîne une prédisposition à l’hypertension. Les souris déficientes en cette protéine développent une hypertension lorsqu’elles sont exposées à une charge élevée de chlorure de sodium.18 Bien que le transporteur Slc26a9 semble jouer un rôle important dans la gestion de charges importantes de chlorure de sodium, la régulation de l’activité native du transporteur en réponse à des charges variées de chlorure de sodium reste inconnue.

(A) Le chlorure peut être sécrété ou réabsorbé dans le canal collecteur. Une partie de l’absorption du chlorure est entraînée par un potentiel négatif de la lumière et un mouvement paracellulaire. (B) La réabsorption transcellulaire du chlorure peut également se produire via le couplage de l’échangeur chlorure-bicarbonate apical Pendrin à l’échangeur chlorure-2 bicarbonate dépendant du sodium SLCA48 (NDCBE). Deux cycles de Pendrin entraîneraient l’entrée de deux chlorures dans la cellule en échange de deux bicarbonates, tandis que le NDCBE transporterait un sodium et deux bicarbonates en échange d’un chlorure. Le résultat net serait le transport de 1 sodium et 1 chlorure dans la cellule. Des différences dans les activités apicales de Pendrin et de NDCBE pourraient déterminer si la sécrétion ou l’absorption de Cl- prédomine.
Concentration de chlorure et hyperchlorémie
Le taux de chlorure sérique est généralement mesuré comme une concentration de chlorure dans un volume de sérum. La concentration de chlorure biologiquement active est la concentration de chlorure libre dans l’eau du plasma. Le chlorure est le plus souvent mesuré à l’aide d’une électrode au chlorure d’argent, soit dans un échantillon de sérum direct, soit dans un échantillon de sérum dilué.19 Les méthodes automatisées que l’on trouve dans de nombreux laboratoires impliquent la dilution de l’échantillon de sérum avec un réactif, de sorte que le volume de l’échantillon est supposé avoir une teneur en eau normale et que les estimations sont faites sur la base d’un facteur de dilution normal. Lorsque les composants solides du sérum sont très élevés, comme cela peut se produire en cas d’hypertriglycéridémie et de myélome multiple, une pseudo-hypochlorémie peut se produire. Une pseudo-hyperchlorémie peut également être observée lors d’une intoxication au bromure ou à l’iodure. L’interaction du bromure ou de l’iodure avec l’électrode argent-chlorure génère une variation de tension plus importante que celle du chlorure, ce qui donne l’impression d’un excès de chlorure dans le sang.20,21
Causes de l’hyperchlorémie vraieHyperchlorémie due à une perte d’eau
L’hyperchlorémie peut résulter d’un certain nombre de mécanismes (tableau 1). Une perte d’eau supérieure à la perte de chlorure peut augmenter la concentration de chlorure.22 En cas de déshydratation, la réponse rénale consiste à conserver l’eau et à diminuer le débit urinaire. Comme il peut également y avoir une composante de déplétion volumique avec des degrés plus sévères de déshydratation, la conservation du chlorure ainsi que du sodium se produit via une augmentation de la réabsorption tubulaire proximale du chlorure et d’autres solutés, et une réduction de la livraison de chlorure et de sodium aux segments néphroniques plus distaux. L’augmentation de la réabsorption par le tubule proximal du fluide tubulaire et de son contenu ne modifiera pas nécessairement la concentration de chlorure, car l’absorption du fluide se fait de manière isotonique. Le traitement de la privation d’eau est l’administration judicieuse d’eau sans électrolytes qui réduira à la fois les concentrations de sodium et de chlorure.
Causes de l’hyperchlorémie.
Pseudohyperchlorémie
Quantités élevées de solides sériques (lipides ou protéines) lorsque des tests impliquant une dilution de l’échantillon. sont utilisés
Intoxication au bromure ou à l’iodure
Administration excessive de chlorure
Administration d’un grand volume de solution de chlorure de sodium à 0.9 % (normal) de chlorure de sodium
Administration d’une solution saline hypertonique
Noyade en eau salée
Pertes nettes d’eau
Fièvre
Transpiration
Apport insuffisant d’eau (faible soif ou accès à l’eau). d’eau (mauvaise soif ou accès à l’eau)
Diabète insipide
Perte d’eau en excès d’électrolytes
Certaines formes de diarrhée
Diurèse osmotique
Certains cas de diurèse postobstructive
Associés à une acidose métabolique
Certaines formes de diarrhée
Acidose tubulaire rénale
Inhibiteurs de l’anhydrase carbonique
Dérivation urétérale (par ex.g., vessie iléale)
Administration de chlorure d’ammonium
Administration de chlorhydrate d’arginine ou de lysine
Certains cas de maladie rénale chronique
Acidose organique dans laquelle l’anion acide est rapidement excrété (par ex, surdosage en toluène)
Alcalose respiratoire
Hyperchlorémie due à une exposition excessive au chlorure
L’hyperchlorémie peut se produire lorsque le corps est exposé à des liquides à forte teneur en chlorure. Un exemple extrême de ce phénomène est la noyade/ingestion d’eau salée. L’apport soudain et important d’eau de mer (la salinité moyenne est de 3,5 %) dépasse la capacité des reins à excréter la charge de chlorure de sodium et l’hypernatrémie et l’hyperchlorémie sont courantes.23 Néanmoins, une composante de l’hypernatrémie et de l’hyperchlorémie associées à l’ingestion excessive d’eau salée provient des pertes de liquide associées à la diarrhée et aux pertes urinaires.23 Le traitement des patients présentant une hyperchlorémie due à une noyade dans l’eau salée dépendra de l’état volumique du patient ainsi que de l’estimation des pertes liquidiennes et électrolytiques en cours et du remplacement judicieux de l’eau et des électrolytes selon les besoins.
Un exemple moins extrême d’hyperchlorémie avec une charge excessive en chlorure de sodium est l’administration de grands volumes de solution isotonique (0,9%) de chlorure de sodium (solution saline normale) fréquemment utilisée pour la réanimation volumique des patients. Il convient de noter que lorsqu’un individu normal reçoit un bolus important de solution saline isotonique, il peut mettre jusqu’à deux jours pour revenir à l’état d’équilibre du sodium et du chlorure qui prévalait avant le traitement.24 Cette rétention de chlorure se produit lors de l’exposition aux niveaux supraphysiologiques de chlorure dans la solution saline normale. La concentration normale de chlorure dans le plasma est comprise entre 95 et 110meq/L, alors que la solution saline normale a une concentration de chlorure de 154meq/L. La réponse excrétoire relativement lente à une solution saline isotonique peut être liée aux effets des charges de chlorure sur le flux sanguin rénal et sur la filtration glomérulaire (rétroaction tubuloglomérulaire). Bien qu’une régulation à la baisse des activités des transporteurs de réabsorption du chlorure se produise avec la charge de chlorure de sodium,14,25,26 la rapidité de la réduction de ces transporteurs n’est pas bien définie.
Lors de l’administration d’une solution saline isotonique, la concentration de bicarbonate peut également diminuer lorsque la concentration de chlorure augmente. Outre la dilution du bicarbonate plasmatique avec l’administration de solutions supraphysiologiques contenant du chlorure et sans base, comme le sérum physiologique, d’autres facteurs peuvent jouer un rôle dans la chute du bicarbonate et l’augmentation du chlorure. Les pertes urinaires de bicarbonate peuvent contribuer à la baisse du taux de bicarbonate sérique car il peut y avoir une réduction du seuil de réabsorption du bicarbonate avec l’expansion volumique.27 Cette perte de bicarbonate peut se produire même lorsque la concentration de bicarbonate sérique est faible.27 Dans les études menées chez l’homme, au cours des premières 24 heures après l’administration d’une perfusion de solution saline isotonique, les pertes de sodium et de potassium dépassent celles de chlorure. L’excrétion réduite de chlorure par rapport au sodium et au potassium suggère la perte urinaire d’autres anions tels que le bicarbonate et d’autres anions organiques qui peuvent également contribuer à une baisse de la concentration sérique de bicarbonate.24 L’utilisation de solutions électrolytiques équilibrées contenant des bases ou des équivalents de bases et des concentrations de chlorure plus physiologiques peut non seulement prévenir le développement d’une acidose hyperchlorémique, mais également éviter certains des effets nocifs possibles associés aux solutions hyperchlorémiques telles que le sérum physiologique.28,29 En comparaison avec des solutions salines équilibrées contenant des bases, l’administration de sérum physiologique à des sujets humains sains a entraîné une baisse du débit sanguin rénal et de la perfusion corticale30, ce qui soulève des inquiétudes quant à l’administration excessive de sérum physiologique lors de la réanimation volumique chez les patients. Néanmoins, certaines situations cliniques peuvent favoriser l’utilisation du sérum physiologique, notamment chez les patients présentant une alcalose métabolique hypochlorémique ou ceux présentant un œdème cérébral.
Hyperchlorémie avec acidose métabolique
L’hyperchlorémie se produit également lorsque de l’acide chlorhydrique (HCl) est ajouté au sang. Le HCl est rarement administré comme agent acidifiant direct mais peut être créé à partir du métabolisme du chlorure d’ammonium ou d’acides aminés cationiques tels que la lysine et l’arginine31. La génération de HCl conduit à la réaction de H+ avec HCO3- qui entraîne la production de CO2 et une perte nette de HCO3- et une augmentation de la concentration en chlorure.
Lors de la respiration titrée, le bicarbonate est perdu par l’organisme sous forme de CO2.
Ainsi, pour chaque milliéquivalent de HCl ajouté, un milliéquivalent de bicarbonate est consommé et converti en CO2, de sorte que le taux de chlorure augmente dans la même mesure que le taux de bicarbonate diminue.
Les acidoses tubulaires rénales (ACR proximale de type 2 et ACR distale de type 1 ou 4) entraînent une acidose métabolique hyperchlorémique. Dans l’ATR proximale (type 2), la réabsorption du bicarbonate dans le tubule proximal est altérée, ce qui entraîne une augmentation des pertes de bicarbonate hors de ce segment. Il y a également une certaine perturbation de la réabsorption du chlorure car l’absence d’extraction du bicarbonate empêche l’augmentation normale de la concentration luminale de chlorure. Néanmoins, dans l’ATR proximale, la réduction du transport du bicarbonate est plus importante que la réduction du transport du chlorure, de sorte qu’il y a relativement plus de chlorure réabsorbé que de bicarbonate. Si l’inhibition de l’anhydrase carbonique est utilisée comme modèle d’ATR proximale, la réabsorption du chlorure semble moins altérée que celle du bicarbonate, comme le reflète une augmentation relativement modeste du taux d’excrétion urinaire du chlorure alors que les taux d’excrétion du sodium, du potassium et, vraisemblablement, du bicarbonate sont nettement augmentés32.
Dans l’ATR distale classique (type 1) ou l’ATR de type 4, la réduction de la sécrétion acide nette empêche la génération rénale de nouveau bicarbonate en altérant l’excrétion d’ammonium et/ou d’acide titrable. En conséquence, le HCl généré par le métabolisme entraîne une chute du bicarbonate qui n’est pas compensée par la génération et la conservation de bicarbonate et l’excrétion de chlorure. Tant que la fonction rénale est préservée, les anions acides non chlorurés ne s’accumulent pas dans la circulation systémique, ce qui maintient un trou anionique relativement normal. En effet, l’excrétion rénale des anions phosphate et sulfate générés par le métabolisme des acides aminés contenant du phosphore et du soufre31 est en fait stimulée par l’acidose.33
Une autre cause d’acidose métabolique hyperchlorémique survient en cas de diarrhée. Dans de nombreux segments du tractus gastro-intestinal et des organes exocrines associés tels que le pancréas, le bicarbonate est sécrété dans l’intestin en échange du chlorure, de sorte que la perte de bicarbonate, en particulier dans les formes sécrétoires de diarrhée, peut être associée à des pertes de bicarbonate qui sont associées à la rétention de chlorure34.
La réparation des formes hyperchlorémiques d’acidose métabolique implique l’arrêt de la cause continue de la perte de bicarbonate ou de la génération de HCl tout en donnant au patient du bicarbonate ou des équivalents de base (par exemple, du citrate) ou en permettant aux reins du patient de régénérer le bicarbonate si la fonction rénale est relativement normale. Lors de la génération d’une acidose métabolique, il y a initialement des pertes nettes de sodium et une contraction du volume. En cas d’acidose plus prolongée, il peut y avoir une rétention de sodium due à des taux élevés d’aldostérone et à une régulation positive de l’ENaC dans le canal collecteur.35 Avec l’apport de bicarbonate pour corriger l’acidose, le bicarbonate est retenu dans le tubule proximal et la réabsorption normale du chlorure est également rétablie. La réexpansion du volume associée au bicarbonate peut contribuer à la chute du chlorure. Lorsque les reins réparent l’acidose métabolique, le chlorure d’ammonium est excrété dans l’urine tandis que le bicarbonate qui est fabriqué dans le tubule proximal comme sous-produit du métabolisme de la glutamine est renvoyé dans le sang.
Liste des points clés
-
Le rein joue un rôle clé dans le maintien de l’équilibre des chlorures dans l’organisme. Bien que le transport rénal du chlorure soit couplé au transport du sodium, le transport du chlorure peut parfois diverger du transport du sodium.
-
L’hyperchlorémie peut résulter de diverses conditions, notamment la déplétion hydrique, l’exposition excessive au chlorure et l’acidose métabolique.
-
La cause pathogène de l’hyperchlorémie fournira des indications sur la manière de traiter la perturbation : l’épuisement hydrique est traité par une réplétion hydrique judicieuse ; l’administration excessive de chlorure par l’abstention de toute nouvelle administration de chlorure ; et l’acidose métabolique hyperchlorémique par l’administration de bicarbonate.
Conflit d’intérêt
L’auteur ne déclare aucun conflit d’intérêt.