Nom générique : méprobamate et aspirine
Formation posologique : comprimés
Médicalement examiné par Drugs.com. Dernière mise à jour le 22 décembre 2020.
- Aperçu
- Effets secondaires
- Dosage
- Professionnel
- Interactions
- Images
- Plus
Code 1019A00
Rev. 09/06
Rx seulement
- Equagesic Description
- Equagesic – Pharmacologie clinique
- Indications et utilisation d’Equagesic
- Contre-indications
- Avertissements
- Précautions
- Généralités
- Information pour les patients
- Interactions médicamenteuses
- Interactions avec les tests de laboratoire
- Carcinogenèse, mutagenèse Altération de la fertilité
- Grossesse : Effets tératogènes. Catégorie de grossesse X.
- Laboratoire et accouchement
- Mères allaitantes
- Utilisation pédiatrique
- Utilisation gériatrique
- Réactions indésirables
- Drogue et dépendance
- Surdosage
- Dosage et administration
- Comment se procurer
Equagesic Description
Chaque comprimé d’Equagesic, pour administration orale, contient 200 mg de méprobamate et 325 mg d’aspirine. Chimiquement, le méprobamate est le dicarbamate de 2-méthyl-2-propyl-1,3- propanediol. Sa formule moléculaire est C9H18N2O4 avec un poids moléculaire de 218,25.
Chimiquement, l’aspirine est l’acide benzoïque 2-(acétyloxy)-. Sa formule moléculaire est C9H8O4 avec un poids moléculaire de 180,16. Elle se présente sous la forme d’une substance blanche inodore, cristalline ou poudreuse, ressemblant à une aiguille. Lorsqu’elle est exposée à l’humidité, l’aspirine s’hydrolyse en acides salicylique et acétique, et dégage une odeur de vinaigre. Elle est très soluble dans les lipides et légèrement soluble dans l’eau. Les formules structurelles du méprobamate et de l’aspirine sont :
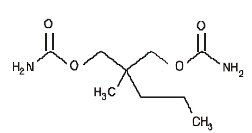
MEPROBAMATE
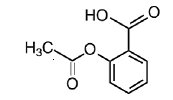
ASPIRINE
Les ingrédients inactifs présents sont le D&C jaune 10, le FD&C rouge 3, le FD&C jaune 6, l’huile végétale hydrogénée, le stéarate de magnésium, la cellulose microcristalline, le polacrilin de potassium et l’amidon.
Equagesic – Pharmacologie clinique
Le méprobamate est un dérivé du carbamate dont il a été démontré (dans des études animales et/ou humaines) qu’il avait des effets sur de multiples sites du système nerveux central, notamment le thalamus et le système limbique. L’aspirine est un analgésique non narcotique doté de propriétés antipyrétiques et anti-inflammatoires.
Indications et utilisation d’Equagesic
Comme adjuvant dans le traitement à court terme de la douleur accompagnée de tension et/ou d’anxiété chez les patients atteints de maladies musculo-squelettiques. Les essais cliniques ont démontré que dans ces situations, le soulagement de la douleur est un peu plus important qu’avec l’aspirine seule. Equagesic n’est pas destiné à être utilisé pendant plus de 10 jours.
Contre-indications
Utilisation pendant la grossesse et l’allaitement
Une augmentation du risque de malformations congénitales associée à l’utilisation de tranquillisants mineurs (méprobamate, chlordiazépoxide et diazépam) pendant le premier trimestre de la grossesse a été suggérée dans plusieurs études. Comme l’utilisation de ces médicaments est rarement une question d’urgence, leur utilisation pendant cette période devrait presque toujours être évitée.
En raison de l’effet connu des anti-inflammatoires non stéroïdiens (AINS) sur le système cardiovasculaire du fœtus (fermeture du canal artériel), leur utilisation pendant le troisième trimestre de la grossesse devrait être évitée. Les produits à base de salicylates ont également été associés à des altérations des mécanismes d’hémostase maternelle et néonatale, à une diminution du poids de naissance et à une mortalité périnatale. La possibilité qu’une femme en âge de procréer soit enceinte au moment de l’instauration du traitement doit être envisagée. Les patientes doivent être informées que si elles deviennent enceintes pendant le traitement ou si elles ont l’intention de le devenir, elles doivent discuter avec leur médecin de l’opportunité d’arrêter le traitement. Le méprobamate passe la barrière placentaire. Il est présent à la fois dans le sang du cordon ombilical à des taux plasmatiques maternels ou proches de ceux-ci et dans le lait maternel des mères qui allaitent à des concentrations deux à quatre fois supérieures à celles du plasma maternel. Lorsque l’utilisation du méprobamate est envisagée chez des patientes qui allaitent, les concentrations plus élevées du médicament dans le lait maternel par rapport aux niveaux plasmatiques maternels doivent être prises en compte.
Equagesic est contre-indiqué chez les patients atteints de porphyrie aiguë intermittente et chez les patients présentant des réactions allergiques ou idiosyncrasiques à l’aspirine, au méprobamate ou à des composés apparentés, tels que le carbromal, le carisoprodol, le mébutamate, les anti-inflammatoires non stéroïdiens, les salicylates ou le tybamate. Equagesic est également contre-indiqué chez les patients présentant un syndrome d’asthme, une rhinite et des polypes nasaux. Le composant aspirine d’Equagesic peut provoquer un angioedème sévère, un bronchospasme (asthme) ou une urticaire. Syndrome de Reye : L’aspirine ne doit pas être utilisée chez les enfants ou les adolescents pour des infections virales, avec ou sans fièvre, en raison du risque de syndrome de Reye lors de l’utilisation concomitante d’aspirine dans certaines maladies virales.
Avertissements
Equagesic doit être prescrit avec prudence et en petites quantités aux patients ayant des tendances suicidaires.
Effets additifs : Puisque les effets suppressifs sur le SNC du méprobamate et de l’alcool ou du méprobamate et d’autres psychotropes peuvent être additifs, une prudence appropriée doit être exercée chez les patients qui prennent plus d’un de ces agents simultanément.
Avertissement concernant l’alcool : Les patients qui consomment trois boissons alcoolisées ou plus chaque jour doivent être conseillés sur les risques de saignement liés à une consommation chronique et importante d’alcool lors de la prise d’aspirine.
Anomalies de la coagulation : Même de faibles doses d’aspirine peuvent inhiber la fonction plaquettaire conduisant à une augmentation du temps de saignement. Cela peut avoir un effet négatif sur les patients atteints de troubles de la coagulation héréditaires (hémophilie) ou acquis (maladie du foie ou carence en vitamine K).
Effets secondaires gastro-intestinaux (GI) : Les effets secondaires GI comprennent les saignements GI bruts, les brûlures d’estomac, les nausées, les douleurs d’estomac et les vomissements. Bien que les symptômes gastro-intestinaux supérieurs mineurs, tels que la dyspepsie, soient courants et puissent survenir à tout moment pendant le traitement, les médecins doivent rester attentifs aux signes d’ulcération et de saignement, même en l’absence de symptômes gastro-intestinaux antérieurs. Les médecins doivent informer les patients des signes et symptômes des effets secondaires gastro-intestinaux et des mesures à prendre s’ils surviennent.
Ulcère gastro-duodénal : Les patients ayant des antécédents d’ulcère gastroduodénal actif doivent éviter d’utiliser l’aspirine, qui peut provoquer une irritation de la muqueuse gastrique et des saignements.
Tâches potentiellement dangereuses
Les patients doivent être avertis que le méprobamate peut altérer les capacités mentales et/ou physiques nécessaires à l’exécution de tâches potentiellement dangereuses, telles que la conduite d’un véhicule à moteur ou l’utilisation de machines. De telles tâches doivent être évitées pendant la prise de ce produit.
Précautions
Généralités
Equagesic doit être prescrit avec prudence dans certaines populations à risque particulier, telles que les patients âgés ou affaiblis et ceux présentant des affections abdominales aiguës, une maladie d’Addison, des troubles de la coagulation, une pression intracrânienne élevée, des traumatismes crâniens, une hypothyroïdie, une altération de la fonction hépatique ou rénale, une hypertrophie prostatique ou un rétrécissement urétral. Le méprobamate est métabolisé dans le foie et excrété par les reins. Pour éviter son accumulation excessive, il faut faire preuve de prudence lors de l’administration à des patients dont la fonction hépatique ou rénale est compromise. Le méprobamate peut occasionnellement précipiter des crises chez les patients épileptiques.
Information pour les patients
Les patients doivent être informés qu’Equagesic contient de l’aspirine et ne doit pas être pris par les patients allergiques à l’aspirine.
Les patients ayant une prédisposition aux saignements gastro-intestinaux doivent être avertis que l’utilisation concomitante de médicaments contenant de l’aspirine et/ou de l’alcool peut avoir un effet additif à cet égard.
Interactions médicamenteuses
Inhibiteurs de l’enzyme de conversion de l’angiotensine (ECA) : Les effets hyponatrémiques et hypotensifs des inhibiteurs de l’ECA peuvent être diminués par l’administration concomitante d’aspirine en raison de son effet indirect sur la voie de conversion rénine-angiotensine.
Acétazolamide : L’utilisation concomitante d’aspirine et d’acétazolamide peut entraîner des concentrations sériques élevées d’acétazolamide (et une toxicité) en raison de la compétition au niveau du tubule rénal pour la sécrétion.
Alcool, anesthésiques généraux, analgésiques narcotiques, hypnotiques sédatifs, tranquillisants tels que le chlordiazépoxide, ou autres dépresseurs du SNC : Les effets de ces substances peuvent être renforcés, entraînant une dépression accrue du SNC.
Traitement anticoagulant (héparine et warfarine) : Les patients sous traitement anticoagulant présentent un risque accru de saignement en raison des interactions médicamenteuses et de l’effet sur les plaquettes. L’aspirine peut déplacer la warfarine des sites de liaison aux protéines, ce qui entraîne une prolongation du temps de prothrombine et du temps de saignement. L’aspirine peut augmenter l’activité anticoagulante de l’héparine, augmentant ainsi le risque de saignement.
Anticonvulsivants : Les salicylates peuvent déplacer la phénytoïne et l’acide valproïque liés aux protéines, entraînant une diminution de la concentration totale de phénytoïne et une augmentation des taux sériques d’acide valproïque.
Bêta-bloquants : Les effets hypotenseurs des bêtabloquants peuvent être diminués par l’administration concomitante d’aspirine en raison de l’inhibition des prostaglandines rénales, entraînant une diminution du débit sanguin rénal et une rétention de sel et de liquide.
Corticostéroïdes : Chez les patients recevant de façon concomitante des corticostéroïdes et une utilisation chronique de médicaments contenant de l’aspirine, le retrait des corticostéroïdes peut entraîner un salicylisme car les corticostéroïdes augmentent la clairance rénale des salicylates et leur retrait est suivi d’un retour à des taux normaux de clairance rénale.
Diurétiques : L’efficacité des diurétiques chez les patients présentant une maladie rénale ou cardiovasculaire sous-jacente peut être diminuée par l’administration concomitante d’aspirine en raison de l’inhibition des prostaglandines rénales, entraînant une diminution du flux sanguin rénal et une rétention de sel et de liquide.
6-Mercaptopurine et méthotrexate : La toxicité de la moelle osseuse et la dyscrasie sanguine peuvent résulter du déplacement de ces médicaments des sites de liaison secondaires et, dans le cas du méthotrexate, de la réduction également de son excrétion.
Médicaments anti-inflammatoires non stéroïdiens (AINS) : L’utilisation simultanée d’aspirine et d’autres AINS doit être évitée car cela peut augmenter les saignements ou entraîner une diminution de la fonction rénale.
Hypoglycémiants oraux : Des doses modérées d’aspirine peuvent augmenter l’efficacité des hypoglycémiants oraux, entraînant une hypoglycémie.
Agents uricosuriques (Probénicid et Sulfinpyrazone) : Les salicylés antagonisent l’action uricosurique, réduisant leur efficacité dans le traitement de la goutte. L’aspirine entre en compétition avec ces agents pour les sites de liaison aux protéines.
Interactions avec les tests de laboratoire
L’aspirine peut interférer avec les déterminations de laboratoire suivantes dans le sang : azote uréique sanguin, cholestérol, enzymes hépatiques élevées, y compris l’aspartate aminotransférase (AST), glycémie à jeun, hyperkaliémie, temps de saignement prolongé, protéines, temps de prothrombine, amylase sérique, créatinine sérique et acide urique. L’aspirine peut interférer avec les dosages de laboratoire suivants dans l’urine : acide 5-hydroxyindoleacétique, acide diacétique, cétone de Gerhardt, glucose, protéinurie, acide urique, détection spectrophotométrique des barbituriques et acide vanillylmandélique (AVM).
Carcinogenèse, mutagenèse Altération de la fertilité
L’administration d’aspirine pendant 68 semaines à 0,5 % dans l’alimentation des rats n’a pas été cancérigène. Dans le test d’Ames sur Salmonella, l’aspirine n’était pas mutagène ; cependant, l’aspirine a induit des aberrations chromosomiques dans des fibroblastes humains en culture.
Grossesse : Effets tératogènes. Catégorie de grossesse X.
Voir contre-indications
Laboratoire et accouchement
L’aspirine doit être évitée pendant le troisième trimestre de la grossesse et pendant le travail et l’accouchement car elle peut entraîner une perte de sang excessive lors de l’accouchement. Une gestation prolongée et un travail prolongé dus à l’inhibition des prostaglandines ont été rapportés.
Mères allaitantes
Les mères allaitantes doivent éviter d’utiliser l’aspirine car le salicylate est excrété dans le lait maternel. L’utilisation de doses élevées peut entraîner des éruptions cutanées, des anomalies plaquettaires et des saignements chez les nourrissons. En raison du risque d’effets indésirables graves chez le nourrisson, il convient de décider de l’arrêt de l’allaitement ou de l’arrêt du médicament, en tenant compte de l’importance du médicament pour la mère ( Voir également Contre-indications).
Utilisation pédiatrique
La sécurité et l’efficacité n’ont pas été établies pour les patients pédiatriques âgés de moins de 12 ans (Voir Contre-indications).
Utilisation gériatrique
Les études cliniques du méprobamate avec l’aspirine n’ont pas inclus un nombre suffisant de sujets âgés de 65 ans et plus pour déterminer s’ils répondent différemment des sujets plus jeunes. En général, la sélection de la dose pour un patient âgé doit être prudente, commençant habituellement à l’extrémité inférieure de la gamme de dosage, reflétant la plus grande fréquence de diminution de la fonction hépatique, rénale ou cardiaque, et de maladie concomitante ou d’autres traitements médicamenteux.
Réactions indésirables
Corps entier
Fièvre, hypothermie, soif.
Réactions allergiques ou idiosyncrasiques
Réactions graves d’hypersensibilité, notamment anaphylaxie, oedème angioneurotique, anurie, asthme, bronchospasme, dermatite bulleuse, frissons, érythème polymorphe, érythrodermie exfoliative, oedème laryngé, oligurie, proctite, purpura, syndrome de Stevens-Johnson, stomatite et urticaire. Les réactions les plus bénignes sont caractérisées par une éruption maculopapuleuse ou urticarienne érythémateuse et prurigineuse qui peut être généralisée ou limitée à l’aine. D’autres réactions ont inclus un purpura aigu nonrombocytopénique, des adénopathies, une sensibilité croisée entre le méprobamate/mébutamate et le méprobamate/carbromal, des ecchymoses, une éosinophilie, une éruption médicamenteuse fixe avec réaction croisée au carisoprodol, une leucopénie, un œdème périphérique et des pétéchies.
Cardiovasculaire
Diverses formes d’arythmie, hypotension, palpitation, syncope, tachycardie et modifications transitoires de l’ECG.
Système nerveux central
Agitation, ataxie, œdème cérébral, coma, confusion, étourdissements, somnolence, dysphorie, euphorie, activité EEG rapide, céphalées, troubles de l’accommodation visuelle, léthargie, surstimulation, excitation paradoxale, paresthésies, sédation, troubles de l’élocution, hémorragie sous-durale ou intracrânienne, convulsions, vertiges et faiblesse.
Fluide et électrolyte
Déshydratation, hyperkaliémie, acidose métabolique et alcalose respiratoire.
Gastro-intestinal
Douleurs abdominales, constipation, diarrhée, dyspepsie, gêne épigastrique, détresse gastrique, saignement gastro-intestinal, brûlures d’estomac, hépatite, nausées, pancréatite, syndrome de Reye, élévations transitoires des enzymes hépatiques, ulcération et perforation et vomissements.
Hématologiques (voir également « Allergiques ou idiosyncrasiques »)
Une agranulocytose et une anémie aplasique ont été rapportées, bien qu’aucune relation de cause à effet n’ait été établie, une coagulopathie, coagulation intravasculaire disséminée, exacerbation des symptômes porphyriques, anémie hémolytique, anémie ferriprive, perte de sang occulte, allongement du temps de prothrombine, thrombocytopénie et purpura thrombocytopénique.
Musculo-squelettique
Rhabdomyolyse
Métabolisme
Hyperglycémie et hypoglycémie
Reproductif
Grossesse et travail prolongés, mortinatalité, enfants de faible poids de naissance et hémorragie antepartum et postpartum.
Respiratoire
Obstruction aiguë des voies respiratoires, hyperpnée, œdème pulmonaire et tachypnée.
Sens spéciaux
Perte auditive et acouphènes.
Urogénital
Néphrite interstitielle, nécrose papillaire, protéinurie et insuffisance et défaillance rénale.
Drogue et dépendance
Une dépendance physique, une dépendance psychologique et un abus ont été observés. L’intoxication chronique résultant de l’ingestion prolongée de doses, généralement supérieures à celles recommandées, se manifeste par une ataxie, des troubles de l’élocution et des vertiges. Par conséquent, il est conseillé de surveiller attentivement la dose et les quantités prescrites, ainsi que d’éviter l’administration prolongée, en particulier chez les alcooliques et les autres patients ayant une propension connue à prendre des quantités excessives de médicaments. Le retrait soudain du médicament après un usage prolongé et excessif peut précipiter la réapparition de symptômes préexistants, comme l’anorexie, l’anxiété ou l’insomnie, ou des réactions de sevrage, comme l’ataxie, les états confusionnels, l’hallucinose, les secousses musculaires, les tremblements, les vomissements et, rarement, les crises convulsives. Ces crises sont plus susceptibles de se produire chez les personnes présentant des lésions du système nerveux central ou des troubles convulsifs préexistants ou latents. Les symptômes de sevrage se manifestent habituellement dans les 12 à 48 heures suivant l’arrêt du méprobamate ; les symptômes cessent habituellement dans les 12 à 48 heures suivantes. Lorsque des doses excessives ont été maintenues pendant des semaines ou des mois, il convient de réduire progressivement la dose sur une période de 1 à 2 semaines plutôt que de l’arrêter brusquement. On peut également substituer un barbiturique à longue durée d’action, puis le retirer progressivement.
Surdosage
Le traitement du surdosage par Equagesic est essentiellement symptomatique et de soutien. Dans les cas où des doses excessives d’Equagesic ont été prises, le sommeil s’installe rapidement et la pression artérielle, le pouls et la fréquence respiratoire sont ramenés à des niveaux basaux. Tout médicament restant dans l’estomac doit être éliminé et un traitement symptomatique doit être administré. Après vomissement et/ou lavage, le charbon actif peut réduire l’absorption de l’aspirine et du méprobamate. Si la respiration ou la pression artérielle sont compromises, une assistance respiratoire, des stimulants du système nerveux central et des agents presseurs doivent être administrés avec précaution, selon les indications. La diurèse, la diurèse osmotique (mannitol), la dialyse péritonéale et l’hémodialyse ont été utilisées avec succès pour éliminer l’aspirine et le méprobamate. L’alcalinisation de l’urine augmente l’excrétion des salicylates. Il est nécessaire de surveiller attentivement le débit urinaire et de prendre des précautions pour éviter une surhydratation. La rechute et la mort, après le rétablissement initial, ont été attribuées à une vidange gastrique incomplète et à un retard d’absorption. La toxicité des salicylates peut résulter d’une ingestion aiguë (surdosage) ou d’une intoxication chronique. Les signes et symptômes comprennent des douleurs abdominales, des perturbations acido-basiques avec développement d’une acidose métabolique, des convulsions, un délire, une hyperpnée, une hyperthermie, une hypoprothrombinémie, une agitation, des acouphènes (bourdonnements d’oreilles) et des vomissements. Les premiers signes de surdosage salicylique (salicylisme), y compris les acouphènes, apparaissent à des concentrations plasmatiques proches de 200 μg/ml. Les concentrations plasmatiques d’aspirine supérieures à 300 μg/mL sont clairement toxiques. Des effets toxiques sévères sont associés à des concentrations supérieures à 400 μg/mL. Une dose létale unique d’aspirine chez l’adulte n’est pas connue avec certitude, mais la mort peut être attendue à 30 g. En cas de surdosage réel ou suspecté, un centre antipoison doit être contacté immédiatement. Une prise en charge médicale attentive est essentielle. En cas de surdosage aigu d’aspirine, de graves perturbations acido-basiques et électrolytiques peuvent se produire et sont compliquées par une hyperthermie et une déshydratation. L’alcalose respiratoire survient rapidement en cas d’hyperventilation, mais elle est rapidement suivie d’une acidose métabolique. Le traitement du surdosage en aspirine consiste principalement à soutenir les fonctions vitales, à augmenter l’élimination des salicylates et à corriger la perturbation acido-basique. La vidange gastrique et/ou le lavage sont recommandés le plus rapidement possible après l’ingestion, même si le patient a vomi spontanément. Après le lavage et/ou les vomissements, l’administration de charbon actif, sous forme de bouillie, est bénéfique, si moins de 3 heures se sont écoulées depuis l’ingestion. L’adsorption au charbon ne doit pas être employée avant les vomissements et le lavage.
La gravité de l’intoxication à l’aspirine est déterminée par la mesure du taux de salicylate sanguin. L’état acido-basique doit être suivi de près par des mesures en série des gaz du sang et du pH sérique. L’équilibre hydrique et électrolytique doit également être maintenu. Dans les cas graves, l’hyperthermie et l’hypovolémie sont les menaces immédiates pour la vie. Les enfants doivent être épongés avec de l’eau tiède. Des liquides de remplacement doivent être administrés par voie intraveineuse et augmentés pour corriger l’acidose. Les électrolytes plasmatiques et le pH doivent être surveillés pour favoriser la diurèse alcaline du salicylate si la fonction rénale est normale. Une perfusion de glucose peut être nécessaire pour contrôler l’hypoglycémie.
L’hémodialyse et la dialyse péritonéale peuvent être réalisées pour réduire le contenu corporel du médicament. Chez les patients souffrant d’insuffisance rénale ou en cas d’intoxication mettant en jeu le pronostic vital, la dialyse est généralement nécessaire. Une exsanguino-transfusion peut être indiquée chez les nourrissons et les jeunes enfants. Les tentatives de suicide avec le méprobamate ont entraîné une ataxie, un coma, une somnolence, une léthargie, un choc, une stupeur et un collapsus respiratoire et vasomoteur. Certaines tentatives de suicide ont été fatales. Les données suivantes ont été rapportées dans la littérature et par d’autres sources. On ne s’attend pas à ce que ces données correspondent à chaque cas (compte tenu de facteurs tels que la susceptibilité individuelle et le délai entre l’ingestion et le traitement), mais elles représentent les fourchettes habituelles signalées. Surdosage simple aigu (méprobamate seul) : La mort a été rapportée avec l’ingestion d’aussi peu que 12 grammes de méprobamate et la survie avec jusqu’à 40 grammes.
NIVEAUX SANGUINS
0,5 à 2 mg pour cent représente la gamme habituelle des niveaux sanguins de méprobamate après des doses thérapeutiques. 3 à 10 mg pour cent correspond généralement aux constatations de symptômes légers à modérés de surdosage, tels que stupeur ou coma léger. 10 à 20 mg pour cent correspondent généralement à un coma plus profond, nécessitant un traitement plus intensif. Certains décès surviennent. À des niveaux supérieurs à 20 mg pour cent, on peut s’attendre à plus de décès que de survivants. Surdosage aigu combiné (méprobamate avec d’autres psychotropes du SNC ou alcool) : Les effets pouvant être additifs, une histoire d’ingestion d’une faible dose de méprobamate plus l’un de ces composés (ou d’un taux sanguin ou tissulaire relativement faible) ne peut pas être utilisée comme indicateur pronostique.
Dosage et administration
La posologie habituelle d’Equagesic est d’un ou deux comprimés, chaque comprimé contenant du méprobamate, 200 mg, et de l’aspirine, 325 mg, par voie orale 3 à 4 fois par jour selon les besoins pour le soulagement de la douleur en cas de tension ou d’anxiété. Equagesic n’est pas recommandé pour les patients âgés de 12 ans et moins.
Comment se procurer
Equagesic® (comprimés de méprobamate et d’aspirine) Les comprimés, 200 mg de méprobamate et 325 mg d’aspirine, sont disponibles comme suit : NDC 10551-091-10, comprimé rose et jaune, double couche, rond, sécable, marqué « LP » et « 91 », en flacon de 100 comprimés.
Réservez à température ambiante contrôlée, 20°-25°C (68°-77°F).
Protégez de l’humidité.
Conservez hermétiquement fermé.
Protéger de la lumière.
Dispenser dans un contenant étanche et résistant à la lumière.
Fabriqué pour :
Leitner Pharmaceuticals™, LLC
Bristol, TN 37620
www.leitnerpharma.com
Fabriqué par :
Mikart, Inc.
Atlanta, GA 30318
1019A00
| Equagesic comprimé de méprobamate et d’aspirine |
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
Étiqueteuse – Mikart, Inc.