Bewertung | Biopsychologie | Vergleichende | Kognitive | Entwicklungspsychologie | Sprache | Individuelle Unterschiede | Persönlichkeit | Philosophie | Soziales |
Methoden | Statistik |Klinische | Pädagogische | Industrielle | Berufliche Gegenstände |Weltpsychologie |
Biologische:Verhaltensgenetik – Evolutionspsychologie – Neuroanatomie – Neurochemie – Neuroendokrinologie -Neurowissenschaften – Psychoneuroimmunologie – Physiologische Psychologie – Psychopharmakologie(Index, Überblick)
| Hirn: Hypothalamus | ||
|---|---|---|
 |
||
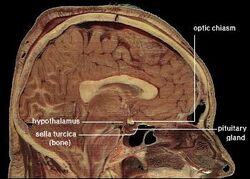
| Lage des menschlichen Hypothalamus | ||
 |
||
| Dienchephalon | ||
| Latein | Hypothalamus | |
| Gray’s | Subject #189 812 | |
| Part von | ||
| Bestandteile | ||
| Arterie | ||
| Vein | ||
| GehirnInfo/UW | hier-358 | |
| MeSH | A08.186.211.730.385.357 | |
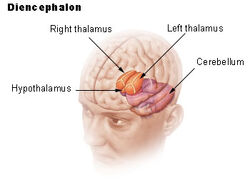
Der Hypothalamus verbindet das Nervensystem über die Hypophyse (Hirnanhangdrüse) mit dem endokrinen System. Der Hypothalamus (von griechisch ὑποθαλαμος = unter dem Thalamus) befindet sich unterhalb des Thalamus, direkt oberhalb des Hirnstamms. Diese Drüse nimmt den größten Teil der ventralen Region des Zwischenhirns ein. Sie ist in allen Säugetiergehirnen zu finden. Beim Menschen hat sie etwa die Größe einer Mandel.
Der Hypothalamus reguliert bestimmte Stoffwechselprozesse und andere Aktivitäten des autonomen Nervensystems. Er synthetisiert und sezerniert Neurohormone, die oft als hypothalamisch freisetzende Hormone bezeichnet werden, und diese wiederum stimulieren oder hemmen die Sekretion von Hypophysenhormonen.
Der Hypothalamus kontrolliert Körpertemperatur, Hunger, Durst, Müdigkeit, Wut und zirkadiane Zyklen.
- Inputs
- Geruchsreize
- Über das Blut übertragene Reize
- Steroide
- Neurale Eingänge
- Kerne
- Ausgänge
- Neurale Projektionen
- Endokrine Hormone
- Kontrolle der Nahrungsaufnahme
- Geschlechtsdimorphismus
- Reaktionen auf Eierstocksteroide
- Gonadale Steroide im Neugeborenenalter von Ratten
- Androgene bei Primaten
- Andere Einflüsse auf die hypothalamische Entwicklung
- Auswirkungen des Alterns auf den Hypothalamus
- Siehe auch
- Weitere Bilder
- Referenzen & Literaturverzeichnis
- Aufsätze
- Zusätzliches Material
- Papers
Inputs
Der Hypothalamus ist eine sehr komplexe Region im Gehirn des Menschen, und selbst kleine Kerne innerhalb des Hypothalamus sind an vielen verschiedenen Funktionen beteiligt. Der paraventrikuläre Kern enthält beispielsweise Neuronen für Oxytocin und Vasopressin (auch antidiuretisches Hormon genannt), die in die hintere Hypophyse projizieren, aber auch Neuronen, die die ACTH- und TSH-Sekretion (die in die vordere Hypophyse projizieren), die Magenreflexe, das mütterliche Verhalten, den Blutdruck, die Nahrungsaufnahme, die Immunantwort und die Temperatur regulieren.
Der Hypothalamus koordiniert viele hormonelle und verhaltensbezogene zirkadiane Rhythmen, komplexe Muster neuroendokriner Leistungen, komplexe homöostatische Mechanismen und viele wichtige Verhaltensweisen. Der Hypothalamus muss daher auf viele verschiedene Signale reagieren, von denen einige von außen und andere von innen kommen. Er steht daher in reicher Verbindung mit vielen Teilen des ZNS, einschließlich der retikulären Formation des Hirnstamms und der autonomen Zonen, dem limbischen Vorderhirn (insbesondere der Amygdala, dem Septum, dem diagonalen Band von Broca und den Riechkolben sowie der Großhirnrinde).
Der Hypothalamus reagiert auf:
- Licht: Tageslänge und Photoperiode zur Regulierung zirkadianer und saisonaler Rhythmen
- Olfaktorische Reize, einschließlich Pheromone
- Steroide, einschließlich gonadaler Steroide und Kortikosteroide
- Neural übertragene Informationen, die insbesondere vom Herzen, dem Magen, und dem Fortpflanzungstrakt
- Autonome Eingänge
- Blutgebundene Stimuli, einschließlich Leptin, Ghrelin, Angiotensin, Insulin, Hypophysenhormone, Zytokine, Plasmakonzentrationen von Glukose und Osmolarität usw
- Stress
- Einfall von Mikroorganismen durch Erhöhung der Körpertemperatur, wodurch der Thermostat des Körpers nach oben versetzt wird.
Geruchsreize
Geruchsreize sind bei vielen Tierarten wichtig für die Fortpflanzung und die neuroendokrine Funktion. Wenn zum Beispiel eine trächtige Maus in einer kritischen Phase nach dem Koitus dem Urin eines „fremden“ Männchens ausgesetzt wird, scheitert die Schwangerschaft (Bruce-Effekt). So bildet ein Mäuseweibchen während des Koitus ein präzises „olfaktorisches Gedächtnis“ ihres Partners, das mehrere Tage lang bestehen bleibt. pheromonale Hinweise helfen bei vielen Arten bei der Synchronisierung der Brunst; bei Frauen kann die synchronisierte Menstruation auch aus pheromonalen Hinweisen resultieren, obwohl die Rolle der Pheromone beim Menschen von einigen bezweifelt wird.
Über das Blut übertragene Reize
Peptidhormone haben wichtige Einflüsse auf den Hypothalamus und müssen dazu die Blut-Hirn-Schranke überwinden. Der Hypothalamus wird zum Teil von spezialisierten Hirnregionen begrenzt, die keine wirksame Blut-Hirn-Schranke haben; das Kapillarendothel an diesen Stellen ist gefenstert, so dass selbst große Proteine und andere Moleküle ungehindert passieren können. Einige dieser Stellen sind die Orte der Neurosekretion – die Neurohypophyse und die Eminenz mediana. Andere wiederum sind Stellen, an denen das Gehirn die Zusammensetzung des Blutes prüft. Zwei dieser Stellen, das subfornische Organ und das OVLT (Organum vasculosum der Lamina terminalis) sind so genannte zirkumventrikuläre Organe, in denen die Neuronen in engem Kontakt mit Blut und Liquor stehen. Diese Strukturen sind dicht vaskularisiert und enthalten osmorezeptive und natriumrezeptive Neuronen, die das Trinken, die Vasopressinfreisetzung, die Natriumausscheidung und den Natriumappetit steuern. Sie enthalten auch Neuronen mit Rezeptoren für Angiotensin, atrialen natriuretischen Faktor, Endothelin und Relaxin, die alle für die Regulierung des Flüssigkeits- und Elektrolythaushalts wichtig sind. Die Neuronen des OVLT und des SFO projizieren in den Nucleus supraopticus und den Nucleus paraventricularis sowie in präoptische hypothalamische Bereiche. Die zirkumventrikulären Organe können auch der Wirkungsort von Interleukinen sein, die über Wirkungen auf paraventrikuläre Neuronen sowohl Fieber als auch ACTH-Sekretion auslösen.
Es ist nicht klar, wie alle Peptide, die die hypothalamische Aktivität beeinflussen, den notwendigen Zugang erhalten. Im Falle von Prolaktin und Leptin gibt es Hinweise auf eine aktive Aufnahme am Plexus choroideus aus dem Blut in den Liquor. Einige Hypophysenhormone haben einen negativen Rückkopplungseffekt auf die hypothalamische Sekretion; so wirkt beispielsweise das Wachstumshormon auf den Hypothalamus zurück, aber es ist nicht klar, wie es in das Gehirn gelangt. Es gibt auch Hinweise auf zentrale Wirkungen von Prolaktin und TSH.
Steroide
Der Hypothalamus enthält Neuronen, die auf gonadale Steroide und Glukokortikoide (die Steroidhormone der Nebenniere, die als Reaktion auf ACTH freigesetzt werden) reagieren. Es enthält auch spezialisierte glukoseempfindliche Neuronen (im Nucleus arcuatus und im ventromedialen Hypothalamus), die für den Appetit wichtig sind. Der präoptische Bereich enthält wärmeempfindliche Neuronen, die für die TRH-Sekretion wichtig sind.
Neurale Eingänge
Der Hypothalamus erhält viele Eingänge aus dem Hirnstamm, insbesondere vom Nucleus solitaire, dem Locus coeruleus und der ventrolateralen Medulla. Die Oxytocin-Sekretion als Reaktion auf das Stillen oder die vaginozervikale Stimulation wird über einige dieser Bahnen vermittelt; die Vasopressin-Sekretion als Reaktion auf kardiovaskuläre Reize, die von Chemorezeptoren im Sinus carotis und im Aortenbogen sowie von Niederdruckrezeptoren des Vorhofvolumens ausgehen, wird über andere vermittelt. Bei der Ratte bewirkt die Stimulation der Vagina auch eine Prolaktinausschüttung, die nach einer unfruchtbaren Paarung zu einer Pseudoschwangerschaft führt. Beim Kaninchen löst der Koitus reflexartig einen Eisprung aus. Beim Schaf kann die Stimulation des Gebärmutterhalses in Anwesenheit hoher Östrogenspiegel bei einem jungfräulichen Mutterschaf mütterliches Verhalten hervorrufen. Diese Wirkungen werden alle vom Hypothalamus vermittelt, und die Informationen werden hauptsächlich über spinale Bahnen im Hirnstamm weitergeleitet. Die Stimulation der Brustwarzen regt die Freisetzung von Oxytocin und Prolaktin an und unterdrückt die Freisetzung von LH und FSH.
Kardiovaskuläre Reize werden vom Nervus vagus weitergeleitet, aber der Vagus überträgt auch eine Vielzahl viszeraler Informationen, einschließlich der Signale, die beispielsweise durch die Magendehnung zur Unterdrückung der Nahrungsaufnahme entstehen. Auch diese Informationen erreichen den Hypothalamus über Relais im Hirnstamm.
Kerne
Zu den hypothalamischen Kernen gehören die folgenden:
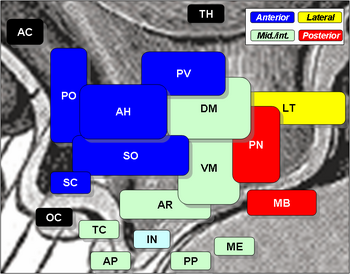
Hypothalamische Kerne
| Region | Bereich | Nukleus | Funktion |
| Anterior | Medial | Medialer präoptischer Nukleus |
|
| supraoptischer Nukleus (SO) |
|
||
| Paraventrikulärer Nukleus (PV) |
|
||
| Anteriorer Hypothalamuskern (AH) |
|
||
| Suprachiasmatischer Kern (SC) |
|
||
| Lateraler | Lateraler präoptischer Nukleus | ||
| Lateraler Nukleus (LT) |
|
||
| Teil des supraoptischen Kerns (SO) |
|
||
| Tuberal | Medial | Dorsomedialer Hypothalamuskern (DM) |
|
| Ventromedialer Nukleus (VM) |
|
||
Nucleus Arcuatus (AR)
|
|||
| Lateral | Lateraler Nukleus (LT) |
|
|
| Laterale tuberale Kerne | |||
| Posterior | Medial | Mammillarkerne (Teil der Mammillarkörper) (MB) |
|
| Nucleus posterior (PN) |
|
||
| Lateraler | Lateraler Nukleus (LT) |
Siehe auch: Ventrolateraler präoptischer Nukleus
Ausgänge
Die Ausgänge des Hypothalamus können in zwei Kategorien unterteilt werden: neurale Projektionen und endokrine Hormone.
Neurale Projektionen
Die meisten Fasersysteme des Hypothalamus verlaufen in zwei Richtungen (bidirektional).
- Projektionen in Bereiche kaudal des Hypothalamus gehen durch das mediale Vorderhirnbündel, den mammillotegmentalen Trakt und den dorsalen longitudinalen Fasciculus.
- Projektionen in Gebiete rostral des Hypothalamus erfolgen über den mammillothalamischen Trakt, den Fornix und die terminale Stria.
Endokrine Hormone
Der Hypothalamus beeinflusst das endokrine System und steuert das emotionale Verhalten, z. B. Wut und sexuelle Aktivität. Die meisten der vom Hypothalamus gebildeten Hormone werden über das hypophysäre Portalsystem an die Hypophyse abgegeben. Der Hypothalamus hält die Homöostase aufrecht, was die Regulierung von Blutdruck, Herzfrequenz und Temperatur einschließt.
Die wichtigsten hypothalamischen Hormone sind:
| Name | Andere Namen | Abkürzungen | Ort | Funktion |
|---|---|---|---|---|
| Corticotropin-releasing hormone | Corticotropin-releasing factor, Corticoliberin | CRH, CRF | parvozelluläre neuroendokrine Neuronen im Nucleus paraventricularis | mit Vasopressin, stimuliert Hypophysenvorderlappen zur Sekretion von ACTH |
| Dopamin | Prolaktin-hemmendes Hormon | DA, PIH | neuroendokrine Neuronen des Nucleus arcuatus | hemmt die Sekretion von Prolaktin aus dem Hypophysenvorderlappen |
| Gonadotropin-Releasing-Hormon | Luteinisierendes-Hormon-Releasing-Hormon | GnRH, LHRH | neuroendokrine Neuronen in den medialen präoptischen und arcuaten Kernen | stimuliert den Hypophysenvorderlappen zur Sekretion von LH und FSH |
| Wachstumshormon-Releasing-Hormon | Growth-Hormon-Releasing-Faktor, Somatocrinin | GHRH, GHRF, GRF | neuroendokrine Neuronen des Nucleus arcuatus | stimuliert Hypophysenvorderlappen zur Sekretion von Wachstumshormon |
| Melatonin | Nucleus suprachiasmaticus | |||
| Somatostatin | Wachstumshormonhemmendes Hormon, Somatotropin-Releasing-Inhibiting-Faktor | SS, GHIH, SRIF | neuroendokrine Neuronen des periventrikulären Kerns | hemmt die Sekretion von Wachstumshormon aus dem Hypophysenvorderlappen |
| Thyrotropin-freisetzendes Hormon | Thyrotropin-freisetzender Faktor, Thyroliberin, Protirelin | TRH, TRF | parvozelluläre neuroendokrine Neuronen in den paraventrikulären und vorderen hypothalamischen Kernen | stimuliert Hypophysenvorderlappen zur Sekretion von TSH |
Siehe auch: Hypocretin
Kontrolle der Nahrungsaufnahme
Der äußerste seitliche Teil des ventromedialen Kerns des Hypothalamus ist für die Kontrolle der Nahrungsaufnahme verantwortlich. Die Stimulation dieses Bereichs bewirkt eine erhöhte Nahrungsaufnahme. Eine bilaterale Läsion dieses Bereichs führt zu einer vollständigen Einstellung der Nahrungsaufnahme. Mediale Teile des Nucleus haben eine kontrollierende Wirkung auf den lateralen Teil. Eine bilaterale Läsion des medialen Teils des Nucleus ventromedialis führt zu Hyperphagie und Fettleibigkeit des Tieres. Eine weitere Läsion des lateralen Teils des Nucleus ventromedialis bei demselben Tier führt zu einer vollständigen Einstellung der Nahrungsaufnahme.
Es gibt verschiedene Hypothesen zu dieser Regulierung:
- Lipostatische Hypothese – diese Hypothese besagt, dass das Fettgewebe ein humorales Signal erzeugt, das proportional zur Fettmenge ist und auf den Hypothalamus einwirkt, um die Nahrungsaufnahme zu verringern und die Energieproduktion zu erhöhen. Es wurde nachgewiesen, dass das Hormon Leptin auf den Hypothalamus einwirkt, um die Nahrungsaufnahme zu verringern und die Energieabgabe zu erhöhen.
- Gutpeptid-Hypothese – Magen-Darm-Hormone wie Grp, Glucagone, CCK und andere sollen die Nahrungsaufnahme hemmen. Die Nahrung, die in den Magen-Darm-Trakt gelangt, löst die Freisetzung dieser Hormone aus, die auf das Gehirn wirken, um Sättigung zu erzeugen. Im Gehirn gibt es sowohl CCK-A- als auch CCK-B-Rezeptoren.
- Glukostatische Hypothese – die Aktivität des Sättigungszentrums in den ventromedialen Kernen wird wahrscheinlich durch die Glukoseverwertung in den Neuronen bestimmt. Es wurde postuliert, dass die Aktivität der Neuronen abnimmt, wenn ihre Glukoseverwertung niedrig ist und folglich die arteriovenöse Blutglukosedifferenz in ihnen gering ist. Unter diesen Bedingungen ist die Aktivität des Fütterungszentrums unkontrolliert und die Person fühlt sich hungrig. Die Nahrungsaufnahme wird durch die intraventrikuläre Verabreichung von 2-Desoxyglukose rasch gesteigert, wodurch die Glukoseverwertung in den Zellen verringert wird.
- Thermostatische Hypothese – nach dieser Hypothese regt ein Absinken der Körpertemperatur unter einen bestimmten Sollwert den Appetit an, während ein Anstieg über den Sollwert den Appetit hemmt.
Geschlechtsdimorphismus
Einige hypothalamische Kerne sind geschlechtsdimorph, d.h. es gibt deutliche Unterschiede in Struktur und Funktion zwischen Männchen und Weibchen.
Einige Unterschiede zeigen sich sogar in der groben Neuroanatomie: am bemerkenswertesten ist der geschlechtsdimorphe Kern im präoptischen Bereich, der nur bei Männern vorhanden ist. Bei den meisten Unterschieden handelt es sich jedoch um subtile Veränderungen in der Konnektivität und chemischen Empfindlichkeit bestimmter Neuronengruppen.
Die Bedeutung dieser Veränderungen lässt sich an den funktionellen Unterschieden zwischen Männern und Frauen erkennen. Zum Beispiel ist das Muster der Sekretion von Wachstumshormonen geschlechtsdimorph, und dies ist ein Grund, warum bei vielen Arten erwachsene Männchen viel größer sind als Weibchen.
Reaktionen auf Eierstocksteroide
Andere auffällige funktionelle Dimorphismen sind in den Verhaltensreaktionen auf Eierstocksteroide des Erwachsenen. Männer und Frauen reagieren unterschiedlich auf Ovarialsteroide, zum Teil weil die Expression östrogenempfindlicher Neuronen im Hypothalamus geschlechtsdimorph ist, d.h. Östrogenrezeptoren werden in verschiedenen Gruppen von Neuronen exprimiert.
Östrogen und Progesteron können die Genexpression in bestimmten Neuronen beeinflussen oder Veränderungen des Zellmembranpotenzials und der Kinaseaktivierung hervorrufen, was zu verschiedenen nichtgenomischen Zellfunktionen führt. Östrogen und Progesteron binden an ihre entsprechenden nuklearen Hormonrezeptoren, die in den Zellkern wandern und mit DNA-Regionen interagieren, die als Hormonreaktionselemente (HREs) bekannt sind, oder sich an die Bindungsstelle eines anderen Transkriptionsfaktors binden. Es hat sich gezeigt, dass der Östrogenrezeptor (ER) andere Transkriptionsfaktoren auf diese Weise transaktivieren kann, obwohl im proximalen Promotorbereich des Gens kein Östrogenreaktionselement (ERE) vorhanden ist. ERs und Progesteronrezeptoren (PRs) sind in der Regel Genaktivatoren mit erhöhter mRNA und anschließender Proteinsynthese nach Hormonexposition.
Männliche und weibliche Gehirne unterscheiden sich in der Verteilung der Östrogenrezeptoren, und dieser Unterschied ist eine irreversible Folge der neonatalen Steroidexposition. Östrogenrezeptoren (und Progesteronrezeptoren) finden sich hauptsächlich in Neuronen im vorderen und mittleren Hypothalamus, insbesondere:
- im präoptischen Bereich (wo sich LHRH-Neuronen befinden)
- im periventrikulären Kern (wo sich Somatostatin-Neuronen befinden)
- im ventromedialen Hypothalamus (der für das Sexualverhalten wichtig ist).
Gonadale Steroide im Neugeborenenalter von Ratten
Im Neugeborenenalter beeinflussen die gonadalen Steroide die Entwicklung des neuroendokrinen Hypothalamus. Sie bestimmen zum Beispiel die Fähigkeit von Weibchen, einen normalen Fortpflanzungszyklus zu zeigen, und von Männchen und Weibchen, im Erwachsenenalter ein angemessenes Fortpflanzungsverhalten an den Tag zu legen.
- Wird einer weiblichen Ratte in den ersten Tagen des postnatalen Lebens (während der „kritischen Periode“ des Sexualsteroideinflusses) einmal Testosteron injiziert, wird der Hypothalamus irreversibel vermännlicht; die erwachsene Ratte ist nicht in der Lage, einen LH-Schub als Reaktion auf Östrogen zu erzeugen (ein Merkmal von Weibchen), ist aber in der Lage, männliche sexuelle Verhaltensweisen zu zeigen (Besteigen eines sexuell empfänglichen Weibchens).
- Im Gegensatz dazu wird eine männliche Ratte, die kurz nach der Geburt kastriert wird, verweiblicht, und das erwachsene Tier zeigt weibliches Sexualverhalten als Reaktion auf Östrogen (sexuelle Empfänglichkeit, Lordose).
Androgene bei Primaten
Bei Primaten ist der Einfluss der Androgene auf die Entwicklung weniger klar, und die Folgen sind weniger vollständig. Der „Tomboyismus“ bei Mädchen könnte die Auswirkungen von Androgenen auf das fötale Gehirn widerspiegeln, aber das Geschlecht der Aufzucht während der ersten zwei bis drei Jahre wird von vielen als wichtigster Bestimmungsfaktor für die Geschlechtsidentität angesehen, weil in dieser Phase entweder Östrogen oder Testosteron dauerhafte Auswirkungen auf ein weibliches oder männliches Gehirn haben und sowohl Heterosexualität als auch Homosexualität beeinflussen.
Das Paradoxe ist, dass die maskulinisierenden Auswirkungen von Testosteron durch Östrogen vermittelt werden. Im Gehirn wird Testosteron zu (Östradiol) aromatisiert, das das wichtigste aktive Hormon für Entwicklungseinflüsse ist. Der menschliche Hoden sondert ab der 8. Woche des Fötus bis 5-6 Monate nach der Geburt hohe Mengen an Testosteron ab (ein ähnlicher perinataler Anstieg des Testosterons wird bei vielen Tierarten beobachtet), ein Prozess, der dem männlichen Phänotyp zugrunde zu liegen scheint. Östrogen aus dem mütterlichen Kreislauf ist relativ unwirksam, was zum Teil auf die hohen zirkulierenden Spiegel steroidbindender Proteine in der Schwangerschaft zurückzuführen ist.
Andere Einflüsse auf die hypothalamische Entwicklung
Sexualsteroide sind nicht die einzigen wichtigen Einflüsse auf die hypothalamische Entwicklung; insbesondere präpubertärer Stress im frühen Leben bestimmt die Fähigkeit des erwachsenen Hypothalamus, auf einen akuten Stressor zu reagieren. Im Gegensatz zu gonadalen Steroidrezeptoren sind Glukokortikoidrezeptoren im gesamten Gehirn weit verbreitet; im paraventrikulären Nukleus vermitteln sie eine negative Rückkopplungskontrolle der CRF-Synthese und -Sekretion, aber ihre Rolle in anderen Bereichen ist nicht gut verstanden.
Auswirkungen des Alterns auf den Hypothalamus
Studien an weiblichen Mäusen haben gezeigt, dass sowohl der Nucleus supraopticus (SON) als auch der Nucleus paraventricularis (PVN) bei normaler Alterung etwa ein Drittel der immunreaktiven IGF-1R-Zellen verlieren. Außerdem verloren alte, kalorienreduzierte (CR) Mäuse eine größere Anzahl nicht-immunreaktiver IGF-1R-Zellen, während die Anzahl der immunreaktiven IGF-1R-Zellen im Vergleich zu alten Mäusen gleich blieb. Folglich zeigen Old-CR-Mäuse einen höheren Prozentsatz an IGF-1R-immunreaktiven Zellen, was eine erhöhte hypothalamische Empfindlichkeit gegenüber IGF-1 im Vergleich zu normal alternden Mäusen widerspiegelt.
Siehe auch
- HPA-Achse
- Hypothalamus-Hypophysen-Nebennieren-System
- Hypothalamus-Hypophysen-Nebennieren-System
- Hypothalamus-Läsionen
- Mediales Vorderhirnbündel
- Neuroendokrinologie
- Präoptisches Areal
Weitere Bilder
Foto zu dieser Galerie hinzufügen
- http://www.cancer.gov/Templates/db_alpha.aspx?CdrID=46359
- http://www.sci.uidaho.edu/med532/hypothal.htm
- Diagramm der Zellkerne (psycheducation.org)
- Diagramm der Kerne (universe-review.ca)
- Diagramm der Kerne (utdallas.edu)
- Wenn in der Tabelle nicht anders angegeben, dann ist die Referenz: Guyton Eight Edition
- Walter F., PhD. Boron. Medical Physiology: A Cellular And Molecular Approaoch, Elsevier/Saunders. Seite 840
- http://thalamus.wustl.edu/course/hypoANS.html
- http://www.vivo.colostate.edu/hbooks/pathphys/endocrine/hypopit/overview.html
- Theologides A (1976). Anorexie erzeugende Zwischenstoffwechselprodukte. Am J Clin Nutr 29 (5): 552-8.
- John Money, „Das Konzept der Geschlechtsidentitätsstörung in Kindheit und Jugend nach 39 Jahren“, Journal of Sex and Marital Therapy 20 (1994): 163-77.
- Romeo, Russell D, Rudy Bellani, Ilia N. Karatsoreos, Nara Chhua, Mary Vernov, Cheryl D. Conrad und Bruce S. McEwen (2005). Stressgeschichte und pubertäre Entwicklung beeinflussen die Plastizität der Hypothalamus-Hypophysen-Nebennieren-Achse. Endocrinology 147 (4): 1664-1674.
- Saeed O,Yaghmaie F,Garan SA,Gouw AM,Voelker MA,Sternberg H, Timiras PS. (2007). Insulin-like growth factor-1 receptor immunoreactive cells are selectively maintained in the paraventricular hypothalamus of calorically restricted mice. Int J Dev Neurosci 25 (1): 23-8.
- Yaghmaie F, Saeed O, Garan SA, Voelker MA, Gouw AM, Freitag W, Sternberg H, Timiras PS (2006). Der altersabhängige Verlust an immunreaktiven Zellen des Insulin-like Growth Factor-1-Rezeptors im supraoptischen Hypothalamus ist bei Mäusen mit Kalorienrestriktion geringer. Int J Dev Neurosci 24 (7): 431-6.
- F. Yaghmaie, O. Saeed, S.A. Garan, A.M. Gouw, P. Jafar, J. Kaur, S. Nijjar, P.S. Timiras, H. Sternberg, M.A. Voelker (2007). Verfolgung von Veränderungen der hypothalamischen IGF-1-Empfindlichkeit bei Alterung und Kalorienrestriktion. Experimental Gerontology 42 (1-2): 148-149.
Referenzen & Literaturverzeichnis
Aufsätze
- Arees, E.A. und Mayer, B, (1967) Anatomical connections between medial and lateral regions of the hypothalamus concerned with food intake, Science 157: 1574-5
- Grossman, S.P. (1960) Eating or drinking elicited by direct adrenergic or cholinergic stimulation of the hypothalamus, Science 132: 301-2.
- Hetherington, A.W. and Ranson, S.W. (1942) The relation of various hypothalamic lesions to adiposity in the rat, 76: 475-99.
Zusätzliches Material
Papers
- Google Scholar
- BrainMaps bei UCDavis Hypothalamus
- Endokrines System und Hypothalamus
- High-Resolution Cytoarchitectural Primate Brain Atlases
- Der Hypothalamus und die Hypophyse bei endotexts.org
- Diagramm der Kerne (psycheducation.org)
- Diagramm der Kerne (universe-review.ca)
- Diagramm der Kerne (utdallas.edu)
|
v-d-e
Menschliches Gehirn: Zwischenhirn (TA A14.1.08, GA 9.807) |
||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Epithalamus |
|
Oberfläche
|
||||||||||||||
| Thalamus |
|
Oberfläche
|
Graue Substanz/
Kerne |
|||||||||||||
| Hypothalamus |
|
|||||||||||||||
| Subthalamus |
Subthalamischer Kern – Zona incerta |
|||||||||||||||
| Ventrikelsystem: Dritter Ventrikel |
Rezessionen: (Optische Vertiefung, Infundibuläre Vertiefung, Suprapineale Vertiefung, Pineale Vertiefung) Hypothalamischer Sulcus – Tela chorioidea des dritten Ventrikels Subfornisches Organ Aperturen: Interventrikular/Monro Posterior commissure |
|||||||||||||||
|
v-d-e
Anatomie des Menschen, endokrines System: Endokrine Drüsen |
||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Hypothalamus-/ Hypophysenachse |
|
|
|
|
||||||||||||
| Kieferndrüse |
Kiefernzellen – Corpora arenacea |
|||||||||||||||
| Inseln der Pankreas |
Alpha-Zelle – Beta-Zelle – Delta-Zelle – PP-Zelle – Epsilon-Zelle |
|||||||||||||||
Menschliches Gehirn: Limbisches System
Amygdala – Gyrus Cinguli – Gyrus Fornicus – Hippocampus – Hypothalamus – Mammillarkörper – Nucleus accumbens – Orbitofrontaler Cortex – Gyrus Parahippocampus