Chlorid ist das am häufigsten vorkommende Anion im Kompartiment der extrazellulären Flüssigkeit (ECF). Hyperchlorämie ist definiert als eine Erhöhung der Chloridkonzentration im Plasmawasser. Hyperchlorämie und ein relativer Chloridüberschuss im Körper werden mit der Entwicklung einer verminderten Nierendurchblutung in Verbindung gebracht,1,2 mit einem erhöhten interstitiellen Ödem, auch in der Niere und im Magen-Darm-Trakt,3 mit erhöhter Morbidität und Mortalität bei kritisch kranken Patienten,4,5 und mit einer verminderten Überlebensrate und Genesung bei Patienten mit akuter Nierenschädigung.6 Wie Natrium und andere chemische Stoffe im ECF-Kompartiment wird auch die Chloridkonzentration reguliert. Das Organ, das für die Aufrechterhaltung des Chloridgleichgewichts im Körper verantwortlich ist, ist die Niere. Dieser Artikel befasst sich mit dem Umgang der Niere mit Chlorid und mit klinischen Situationen, in denen eine Hyperchlorämie auftreten kann.
Renaler Umgang mit Chlorid
Der Chloridspiegel im Plasma wird von der Niere reguliert. Die Niere filtert Chlorid frei über die Basalmembranen der Glomeruli. Die Menge an Chlorid, die mit dem Urin ausgeschieden wird, wird durch das von den Glomeruli gefilterte Chlorid und durch eine Reihe von Transportprozessen entlang des Nephrons bestimmt. Unter normalen Umständen werden über 60 % des gefilterten Chlorids entlang des proximalen Tubulus absorbiert. Im frühen proximalen Tubulus wird Natrium mit einer proportionalen Menge Wasser absorbiert, so dass sich die Natriumkonzentration nicht ändert. Im Gegensatz dazu werden Bikarbonat und andere Nicht-Chlorid-Anionen schnell mit Natrium absorbiert und aus dem Filtrat entfernt7 (Abb. 1A). Während Natrium und Nicht-Chlorid-Anionen in den frühen proximalen Tubulussegmenten (S1 und S2) absorbiert werden, steigt die Chloridkonzentration im Lumen des proximalen Tubulus. Wenn die Tubulusflüssigkeit das letzte Segment des proximalen Tubulus (S3) erreicht, ist die Chloridkonzentration im Vergleich zur Plasmakonzentration hoch, so dass Chlorid passiv über den Konzentrationsgradienten absorbiert werden kann (Abb. 1B). Die transepitheliale Permeabilität für Chlorid ist höher als die Permeabilität für Bicarbonat, so dass trotz des peritubulären Bicarbonatgradienten zum Lumen der Transport von Chlorid, das das Lumen verlässt, den Transport von Bicarbonat, das in die Tubulusflüssigkeit eintritt, übersteigt.

(A) Im frühen proximalen Tubulus erfolgt die isotonische Natriumabsorption mit organischen Lösungsmitteln, Bikarbonat, Phosphat und Wasser, was zu einer steigenden Chloridkonzentration führt. (B) Die hohe Chloridkonzentration im Lumen begünstigt auch den transzellulären und parazellulären Transport. Die interzellulären Verbindungen im späteren proximalen Tubulus werden durchlässiger für Chlorid, was den parazellulären Transport erleichtert. Selbst wenn die Bikarbonatkonzentration im Lumen sinkt, spielt der Na+-H+-Austausch weiterhin eine Rolle bei der NaCl-Rückresorption. Die transzelluläre Natriumchlorid-Resorption kann über die Kopplung des Na+-H+-Austauschs mit dem Austausch von Chlorid-organischen Anionen (Ameisensäure, Oxalat) erfolgen. Die organische Säure (Ameisen- oder Oxalsäure) wird in die Zellen zurückgeführt.
Im frühen Teil des proximalen Tubulus erfolgt die Chloridabsorption ebenfalls über apikale Chlorid-Anionen-Austauscher (Formiat, Oxalat, Base) und verlässt die Zelle über basolaterale Membrantransporter8 (Abb. 1B). Bei hyperchlorämischer metabolischer Azidose aufgrund von HCl- oder Ammoniumchlorid-Belastung ist die Chlorid-Rückresorption im proximalen Tubulus reduziert, zum Teil aufgrund der Verringerung der organischen Anionen-Transporter, die den Natriumchlorid-Transport9 erleichtern, sowie der Verringerung des Gradienten zwischen Lumen und Peritubulus für Chlorid.
Das dicke aufsteigende Glied der Henle-Schleife (TALH) ist eine wichtige Stelle für die Chlorid-Rückresorption.10 An dieser Stelle werden Natrium, Kalium und Chlorid gleichzeitig über einen Natrium-Kalium-2-Chlorid-Co-Transporter (NKCC2) transportiert (Abb. 2). Chlorid tritt in die TALH-Zelle ein und verlässt ihren basolateralen Aspekt über einen elektrogenen Chloridkanal oder über den elektroneutralen Kaliumchlorid-Cotransporter. Die Bewegung von Chlorid durch den basolateralen Chloridkanal (CLC-NKB) trägt zur Erzeugung eines transepithelialen positiven (Lumen) zu negativen (basolateralen) Potentialgradienten bei. Das intrazelluläre positive Potenzial, das durch die Bewegung von Chlorid aus der Zelle heraus entstehen würde, wird durch die basolaterale elektrogene Na+-K+ ATPase ausgeglichen, die Natrium aus der Zelle heraus und im Austausch gegen Kalium in die Zelle hinein im Verhältnis 3:2 transportiert. ROMK-Kaliumkanäle an der apikalen TALH-Zellmembran tragen durch die leitende Bewegung von Kaliumionen von der Zelle zum Lumen zum positiven (intrazellulären negativen) Potenzial bei. Die Gesamtwirkung besteht darin, dass Chlorid, Natrium und Kalium über NKCC2 in die Zelle gelangen und Chlorid die Zelle größtenteils über den basolateralen ClC-NKB-Chloridkanal verlässt, Natrium die Zelle über die Na+-K+-ATPase verlässt und Kalium über den ROMK-Kanal in das Lumen zurückgeführt wird oder basolateral über den KCl-Co-Transporter austritt. Die enge Kopplung zwischen Natrium- und Chloridtransport in der TALH wird durch eine der Varianten des Bartter-Syndroms unterstrichen, bei der Defekte in den basolateralen Chloridkanälen die Natriumchlorid-Rückresorption stören und den bei abnormen NKCC2-Proteinen beobachteten Nierenfehler nachahmen. Obwohl andere Transporter auf der peritubulären Seite der TAL-Zelle, wie z. B. der KCl-Co-Transporter, Chlorid auf natriumunabhängige Weise transportieren, ist der größte Teil des von der TALH aufgenommenen Chlorids an die Natriumrückresorption gekoppelt. Daher werden Faktoren, die die Natriumrückresorption in diesem Segment erhöhen, auch die Chloridrückresorption steigern.
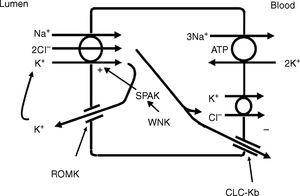
Das dicke aufsteigende Glied der Henleschen Schleife absorbiert Chlorid über den apikalen Na+-K+-2Cl- Cotransporter (NKCC2) und Chlorid verlässt die Zelle über einen basolateralen Chloridkanal und durch K+-Cl- Cotransport. Das K+-Recycling in das Lumen und der basolaterale leitende Cl–Austritt über CLC-Kb tragen zum positiven bis negativen transepithelialen Gradienten zwischen Lumen und Basolateralem bei. Intrazelluläres Chlorid kann den NKCC2-Transport über eine chloridempfindliche WNK-Kinase (WNK) regulieren, die die STE20/SPS1-verwandte Prolin/Alanin-reiche Kinase (SPAK) und NKCC2 aktivieren kann, wenn intrazelluläres Cl- niedrig ist. Wenn sich jedoch aufgrund von Defekten im basolateralen Chloridkanal-Austrittsweg Chlorid in der Zelle ansammelt, wird der NKCC2-Transport blockiert. Wenn NKCC2 stimuliert wird, zum Beispiel durch antidiuretisches Hormon, wird der Chlorideintritt erhöht, aber auch die basolaterale Cl-Leitfähigkeit wird verstärkt.
Im distalen Tubulus werden Natrium und Chlorid durch einen Natrium-Chlorid-Co-Transporter (NCC)11 aus dem Lumen in die Zelle transportiert (Abb. 3). Die treibende Kraft für die Bewegung von Chlorid aus dem Lumen in die Zellen ist der Natriumgradient zwischen Lumen und Zelle, der durch die basolaterale Na+-K+-ATPase erzeugt wird, die Natrium aus der Zelle pumpt und so die intrazelluläre Natriumkonzentration niedrig hält. Eine weitere Regulierung von NCC und NKCC kann durch WNK-Kinasen erfolgen, die als Chlorid-Sensoren12 dienen und diese Transporter durch Änderung des Trafficking oder ihres Phosphorylierungszustands regulieren können.13 In späteren Abschnitten des distalen Tubulus convolutus kann ein negatives Lumenpotential, das durch die Bewegung von Natrium durch den apikalen epithelialen Natriumkanal (ENaC) erzeugt wird, ebenfalls als treibende Kraft für die passive Chlorid-Rückresorption dienen. Somit weisen die Segmente des distalen Tubulus eine direkte Kopplung des Natrium- und Chloridtransports über den NCC und eine indirekte Kopplung des Transports über eine passive Bewegung entlang eines elektrochemischen Gradienten auf.
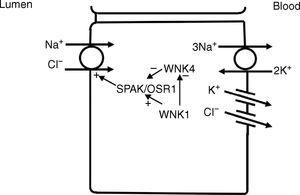
Im distalen Konvolutrohr werden Natrium und Chlorid im Lumen über einen Na+-Cl- Cotransporter (NCC) in die Zelle aufgenommen. Der Transport über den NCC wird durch einen niedrigen intrazellulären Natriumspiegel angetrieben, der hauptsächlich durch die basolaterale Na+-K+ ATPase erzeugt wird. Die WNK1-Kinase kann als Chlorid-Sensor dienen, um die Hemmung des NCC durch die WNK4-Kinase zu blockieren.
Der Sammelkanal spielt eine wichtige Rolle bei der Bestimmung des Chloridgehalts des Endharns. Die Chloridrückresorption in diesem Teil des Nephrons trägt dazu bei, Chlorid als Reaktion auf eine niedrige Chloridaufnahme zu konservieren, und kann zu den blutdrucksteigernden Auswirkungen einer Ernährung mit hohem Natriumchloridgehalt beitragen. Der größte Teil des im Sammelkanal rückresorbierten Natriums wird in den Hauptzellen über Aldosteron-regulierte apikale epitheliale Natriumkanäle aufgenommen. Die Chloridrückresorption im Sammelkanal kann über parazelluläre Chloridabsorption erfolgen, die durch das negative transepitheliale Potenzial im Lumen angetrieben wird, das durch den Natriumfluss vom Lumen zur Zelle über ENaC erzeugt wird (Abb. 4A). Darüber hinaus kann in interkalierten Zellen vom B-Typ und Nicht-A-Nicht-B-Typ Chlorid über Pendrin, einen Chlorid-Bikarbonat-Austauscher, transportiert werden, wobei Chlorid vom Lumen zur Zelle fließt, während Bikarbonat in das Lumen abgegeben wird (Abb. 4B). Die Beziehung zwischen den verschiedenen Natrium- und Chlortransportprozessen in diesem Teil des Nephrons wurde in einer kürzlich erschienenen Arbeit von Vallet und Kollegen veranschaulicht.14 Die Autoren führten eine Reihe von physiologischen Manövern durch, um deren Auswirkungen auf die ENaC- und Pendrin-Proteinspiegel in der Niere zu bestimmen. Eine langfristige NaCl-Belastung führte zu einem signifikanten Rückgang des Pendrin-Proteinspiegels, während die „aktive“ ENaC-γ-Untereinheit abnahm und die β-Untereinheit zunahm. Es wurde eine Dissoziation zwischen dem Natrium- und dem Chloridtransport beobachtet, doch bei der Hemmung des Natrium-Chlorid-Co-Transporters mit Hydrochlorothiazid sank der Pendrin-Spiegel, während der ENaC-Spiegel anstieg. Eine NaCl-Beschränkung erhöhte die Pendrin-Expression.15 Eine erhöhte luminale Bikarbonatkonzentration, die durch die Pendrin-vermittelte Bikarbonatsekretion entstehen würde, beeinflusst die Natriumrückresorption, indem sie die Aktivität der nachgeschalteten ENaC erhöht.16 Der Natrium-Chlorid-Transport durch interkalierte Zellen kann auch durch das Vorhandensein eines thiazidempfindlichen apikalen natriumabhängigen Chlorid-Bicarbonat-Austauschers (NDCBE, Slc4A8) verstärkt werden, der 1 Natrium- und 2 Bicarbonat-Ionen aus dem Lumen in die Zelle transportiert, im Austausch für 1 Chlorid-Ion, das die Zelle verlässt. Wenn der NDCBE-Transport mit dem Pendrin-vermittelten Chlorid-Bicarbonat-Austausch gekoppelt ist, könnte das Zusammenwirken der beiden Transporter zu einer Netto-Natrium-Chlorid-Rückresorption aus dem Lumen führen, da das Bicarbonat in die Zelle hinein und aus ihr heraus recycelt wird, während Natrium und Chlorid in die Zelle gelangen17 (Abb. 4B). Faktoren, die das Verhältnis der Mengen oder Aktivitäten dieser beiden Anionenaustauscher verändern, können die Nettoauswirkungen auf die Bikarbonatsekretion und die Chloridrückresorption bestimmen. Ein weiterer Transporter, der möglicherweise an der Ausscheidung von überschüssigem Chlorid im Körper beteiligt ist, ist der Slc26A9-Transporter, der als Chloridkanal in den medullären Teilen des Sammelkanals fungiert.18 Er kann die Auswirkungen von Chloridbelastungen modifizieren, indem er die Chloridsekretion unter Bedingungen eines Chloridüberschusses erhöht. Das Knockout dieses Gens führt zu einer Prädisposition für Bluthochdruck. Mäuse, denen dieses Protein fehlt, entwickeln Bluthochdruck, wenn sie einer hohen Natriumchlorid-Belastung ausgesetzt sind.18 Obwohl der Slc26a9-Transporter eine wichtige Rolle bei der Bewältigung großer Natriumchlorid-Belastungen zu spielen scheint, ist die Regulierung der Aktivität des nativen Transporters als Reaktion auf unterschiedliche Natriumchlorid-Belastungen noch unbekannt.

(A) Chlorid kann im Sammelkanal sezerniert oder rückresorbiert werden. Ein Teil der Chloridabsorption wird durch ein negatives Potential im Lumen und durch parazelluläre Bewegung angetrieben. (B) Die transzelluläre Rückresorption von Chlorid kann auch über die Kopplung des apikalen Pendrin-Chlorid-Bicarbonat-Austauschers mit dem SLCA48-Natrium-abhängigen Chlorid-2-Bicarbonat-Austauscher (NDCBE) erfolgen. Zwei Pendrin-Zyklen würden dazu führen, dass 2 Chloride im Austausch gegen 2 Bicarbonate in die Zelle gelangen, während der NDCBE 1 Natrium und 2 Bicarbonate im Austausch gegen 1 Chlorid nach außen transportieren würde. Das Nettoergebnis wäre der Transport von 1 Natrium und 1 Chlorid in die Zelle. Unterschiede in den apikalen Pendrin- und NDCBE-Aktivitäten könnten bestimmen, ob die Cl-Sekretion oder die Absorption überwiegt.
Chloridkonzentration und Hyperchlorämie
Der Serumchloridspiegel wird im Allgemeinen als Chloridkonzentration in einem Serumvolumen gemessen. Die biologisch aktive Chloridkonzentration ist die Konzentration des freien Chlorids im Plasmawasser. Chlorid wird am häufigsten mit einer Silberchloridelektrode entweder in einer direkten oder verdünnten Serumprobe gemessen.19 Bei den in vielen Labors üblichen automatisierten Methoden wird die Serumprobe mit Reagenz verdünnt, so dass das Volumen der Probe einen normalen Wassergehalt aufweist und die Schätzungen auf der Annahme eines normalen Verdünnungsfaktors basieren. Wenn die festen Bestandteile des Serums sehr hoch sind, wie es bei Hypertriglyceridämie und multiplem Myelom vorkommen kann, kann eine Pseudohypochlorämie auftreten. Eine Pseudohyperchlorämie kann auch bei einer Bromid- oder Jodidintoxikation auftreten. Die Wechselwirkung von Bromid oder Jodid mit der Silber-Chlorid-Elektrode erzeugt eine größere Spannungsänderung als Chlorid, wodurch der Eindruck eines Chloridüberschusses im Blut entsteht.20,21
Ursachen echter HyperchlorämieHyperchlorämie durch Wasserverlust
Hyperchlorämie kann durch eine Reihe von Mechanismen entstehen (Tabelle 1). Ein Wasserverlust, der den Chloridverlust übersteigt, kann zu einem Anstieg der Chloridkonzentration führen.22 Bei einer Dehydratation reagieren die Nieren mit einer Wassereinsparung und einer geringeren Urinausscheidung. Da bei schwereren Dehydratationsgraden auch eine Komponente der Volumendepletion vorhanden sein kann, erfolgt die Konservierung von Chlorid und Natrium über eine verstärkte Rückresorption von Chlorid und anderen gelösten Stoffen im proximalen Tubulus und eine verringerte Abgabe von Chlorid und Natrium an distalere Nephronsegmente. Die verstärkte proximale tubuläre Rückresorption von Tubulusflüssigkeit und deren Inhalt führt nicht unbedingt zu einer Veränderung der Chloridkonzentration, da die Flüssigkeitsaufnahme isotonisch erfolgt. Die Behandlung des Wasserentzugs besteht in der vernünftigen Verabreichung von elektrolytfreiem Wasser, das sowohl die Natrium- als auch die Chloridkonzentration senkt.
Ursachen der Hyperchlorämie.
Pseudohyperchlorämie
Hohe Mengen an Serumfeststoffen (Lipide oder Proteine), wenn Tests mit Probenverdünnung
Bromid- oder Jodidintoxikation
Übermäßige Chloridverabreichung
Verabreichung großer Mengen von 0.9%iger (normaler) Natriumchloridlösung
Verabreichung von hypertoner Kochsalzlösung
Ertrinken in Salzwasser
Netto-Wasserverluste
Fieber
Schwitzen
Unzureichende Wasser Wasseraufnahme (mangelnder Durst oder Zugang zu Wasser)
Diabetes insipidus
Wasserverlust durch übermäßige Elektrolyte
Bestimmte Formen von Durchfall
Osmotische Diurese
Bestimmte Fälle von post-obstruktiver Diurese
Assoziiert mit metabolischer Azidose
Bestimmte Formen von Durchfall
Renale tubuläre Azidose
Karbonatanhydrasehemmer
Ureterumleitung (z.g., Ilealblase)
Verabreichung von Ammoniumchlorid
Verabreichung von Arginin oder Lysinhydrochlorid
Bestimmte Fälle von chronischen Nierenerkrankungen
Organische Azidose, bei der saure Anionen schnell ausgeschieden werden (z. B., Toluol-Überdosis)
Respiratorische Alkalose
Hyperchlorämie aufgrund übermäßiger Chloridbelastung
Hyperchlorämie kann auftreten, wenn der Körper Flüssigkeiten mit hohem Chloridgehalt ausgesetzt ist. Ein extremes Beispiel hierfür ist das Ertrinken/Verschlucken von Salzwasser. Die plötzliche große Zufuhr von Meerwasser (der durchschnittliche Salzgehalt beträgt 3,5 %) überfordert die Fähigkeit der Niere, die Natriumchloridlast auszuscheiden, und Hypernatriämie und Hyperchlorämie sind häufig.23 Ein Teil der Hypernatriämie und Hyperchlorämie, die mit einer übermäßigen Salzwasseraufnahme einhergehen, ist jedoch auf Flüssigkeitsverluste zurückzuführen, die mit Durchfall und Urinverlusten einhergehen.23 Die Behandlung von Patienten mit Hyperchlorämie durch Ertrinken in Salzwasser hängt vom Volumenstatus des Patienten sowie von Schätzungen der laufenden Flüssigkeits- und Elektrolytverluste und dem umsichtigen Ersatz von Wasser und Elektrolyten nach Bedarf ab.
Ein weniger extremes Beispiel für Hyperchlorämie mit einer übermäßigen Natriumchloridbelastung ist die Verabreichung großer Mengen isotonischer (0,9 %iger) Natriumchloridlösung (normale Kochsalzlösung), die häufig zur Volumenreanimation von Patienten verwendet wird. Es ist bemerkenswert, dass es bei einer normalen Person, der ein großer Bolus isotonischer Kochsalzlösung verabreicht wird, bis zu zwei Tage dauern kann, bis der Zustand des Natrium- und Chloridgleichgewichts vor der Behandlung wiederhergestellt ist.24 Diese Retention von Chlorid tritt auf, wenn man den supraphysiologischen Chloridwerten in normaler Kochsalzlösung ausgesetzt ist. Die normale Chloridkonzentration im Plasma liegt im Bereich von 95-110 meq/L, während normale Kochsalzlösung eine Chloridkonzentration von 154 meq/L aufweist. Die relativ langsame Ausscheidungsreaktion auf isotonische Kochsalzlösung könnte mit den Auswirkungen der Chloridbelastung auf den renalen Blutfluss und die glomeruläre Filtration (tubuloglomeruläre Rückkopplung) zusammenhängen. Obwohl die Aktivitäten der Chlorid-Resorptions-Transporter unter Natriumchlorid-Belastung herabreguliert werden,14,25,26 ist die Geschwindigkeit der Reduktion dieser Transporter nicht genau definiert.
Bei der Verabreichung von isotonischer Kochsalzlösung kann die Bikarbonat-Konzentration ebenfalls sinken, wenn die Chlorid-Konzentration ansteigt. Neben der Verdünnung des Plasmabikarbonats bei der Verabreichung von supraphysiologischen chloridhaltigen, basenfreien Lösungen wie normaler Kochsalzlösung können auch andere Faktoren eine Rolle beim Absinken der Bikarbonat- und Anstieg der Chloridkonzentration spielen. Die Bikarbonatverluste im Urin können zum Absinken des Serumbikarbonatspiegels beitragen, da die Reabsorptionsschwelle für Bikarbonat mit der Volumenexpansion sinken kann.27 Dieser Bikarbonatverlust kann selbst dann auftreten, wenn die Serumbikarbonatkonzentration niedrig ist.27 In Studien am Menschen übersteigen die Natrium- und Kaliumverluste in den ersten 24 Stunden nach Verabreichung einer isotonischen Kochsalzinfusion die Chloridverluste. Die im Vergleich zu Natrium und Kalium verringerte Ausscheidung von Chlorid deutet auf den Verlust anderer Anionen im Urin hin, wie z. B. Bikarbonat und andere organische Anionen, die ebenfalls zu einem Rückgang der Serumbikarbonatkonzentration beitragen können.24 Die Verwendung ausgewogener Elektrolytlösungen, die Basen oder Basenäquivalente und Chloridkonzentrationen enthalten, die eher physiologisch sind, kann nicht nur die Entwicklung einer hyperchlorämischen Azidose verhindern, sondern auch einige der möglichen schädlichen Auswirkungen vermeiden, die mit hyperchlorämischen Lösungen wie normaler Kochsalzlösung verbunden sind.28,29 Im Vergleich zu ausgewogenen, basenhaltigen Salzlösungen führte die Verabreichung von normaler Kochsalzlösung an gesunde Menschen zu einem Rückgang des renalen Blutflusses und der kortikalen Perfusion30 , was Bedenken hinsichtlich der übermäßigen Verabreichung von normaler Kochsalzlösung bei der Volumenreanimation von Patienten aufkommen ließ. Dennoch können bestimmte klinische Situationen die Verwendung von normaler Kochsalzlösung begünstigen, z. B. bei Patienten mit hypochlorämischer metabolischer Alkalose oder bei Patienten mit Hirnödemen.
Hyperchlorämie mit metabolischer Azidose
Hyperchlorämie tritt auch auf, wenn dem Blut Salzsäure (HCl) zugesetzt wird. HCl wird selten als direktes Säuerungsmittel verabreicht, sondern kann durch den Stoffwechsel von Ammoniumchlorid oder kationischen Aminosäuren wie Lysin und Arginin entstehen.31 Die Erzeugung von HCl führt zu einer Reaktion von H+ mit HCO3-, was zu einer CO2-Produktion und einem Nettoverlust von HCO3- und einem Anstieg der Chloridkonzentration führt.
Bei der Atmung geht titriertes Bicarbonat als CO2 aus dem Körper verloren.
Für jedes Milliäquivalent HCl, das zugeführt wird, wird also ein Milliäquivalent Bicarbonat verbraucht und in CO2 umgewandelt, so dass der Chloridspiegel im gleichen Maße ansteigt, wie der Bicarbonatspiegel sinkt.
Renale tubuläre Azidosen (proximale RTA Typ 2 und distale RTA Typ 1 oder 4) führen zu einer hyperchlorämischen metabolischen Azidose. Bei der proximalen RTA (Typ 2) ist die Bikarbonat-Rückresorption im proximalen Tubulus gestört, was zu erhöhten Bikarbonatverlusten aus diesem Segment führt. Auch die Chlorid-Rückresorption ist in gewissem Maße gestört, da die fehlende Bicarbonat-Extraktion den normalen Anstieg der luminalen Chloridkonzentration verhindert. Dennoch ist in der proximalen RTA die Verringerung des Bikarbonattransports größer als die Verringerung des Chlortransports, so dass relativ mehr Chlorid als Bikarbonat rückresorbiert wird. Wird die Hemmung der Karbonsäureanhydrase als Modell für die proximale RTA verwendet, scheint die Chlorid-Rückresorption weniger beeinträchtigt zu sein als die Bikarbonat-Rückresorption, was sich in einem relativ bescheidenen Anstieg der Chlorid-Ausscheidungsrate im Urin widerspiegelt, während die Ausscheidungsraten von Natrium, Kalium und vermutlich auch Bikarbonat deutlich erhöht sind.32
Bei der klassischen distalen RTA (Typ 1) oder der RTA vom Typ 4 verhindert die verminderte Netto-Säuresekretion die renale Neubildung von Bikarbonat durch Beeinträchtigung der Ammonium- und/oder titrierbaren Säureausscheidung. Infolgedessen führt das durch den Stoffwechsel erzeugte HCl zu einem Bikarbonatabfall, der nicht durch die Bildung und Erhaltung von Bikarbonat und die Ausscheidung von Chlorid kompensiert wird. Solange die Nierenfunktion erhalten bleibt, reichern sich Nicht-Chlorid-Säureanionen nicht im systemischen Kreislauf an, wodurch eine relativ normale Anionenlücke aufrechterhalten wird. Tatsächlich wird die renale Ausscheidung von Phosphat- und Sulfatanionen, die aus dem Stoffwechsel phosphor- und schwefelhaltiger Aminosäuren31 stammen, durch die Azidose stimuliert.33
Eine weitere Ursache für eine hyperchlorämische metabolische Azidose tritt bei Durchfall auf. In vielen Abschnitten des Gastrointestinaltrakts und den damit verbundenen exokrinen Organen wie der Bauchspeicheldrüse wird Bikarbonat im Austausch gegen Chlorid in den Darm sezerniert, so dass Bikarbonatverluste, insbesondere bei sekretorischen Formen von Durchfall, mit Bikarbonatverlusten einhergehen können, die mit Chloridretention verbunden sind.34
Die Behandlung hyperchlorämischer Formen der metabolischen Azidose beinhaltet die Unterbrechung der anhaltenden Ursache des Bikarbonatverlustes oder der HCl-Bildung, während dem Patienten Bikarbonat oder Basenäquivalente (z. B. Citrat) verabreicht werden, oder es wird den Nieren des Patienten ermöglicht, Bikarbonat zu regenerieren, wenn die Nierenfunktion relativ normal ist. Während der Entstehung einer metabolischen Azidose kommt es zunächst zu Netto-Natriumverlusten und einer Volumenkontraktion. Bei länger andauernder Azidose kann es aufgrund hoher Aldosteronspiegel und einer Hochregulierung von ENaC im Sammelkanal zu einer Natriumretention kommen.35 Wird Bikarbonat zur Korrektur der Azidose verabreicht, wird Bikarbonat im proximalen Tubulus zurückgehalten und die normale Chloridrückresorption wiederhergestellt. Die mit dem Bikarbonat verbundene Volumenexpansion kann zum Rückgang des Chloridspiegels beitragen. Wenn die Nieren die metabolische Azidose beheben, wird Ammoniumchlorid mit dem Urin ausgeschieden, während Bikarbonat, das im proximalen Tubulus als Nebenprodukt des Glutaminstoffwechsels gebildet wird, ins Blut zurückgeführt wird.
Liste der wichtigsten Punkte
-
Die Niere spielt eine Schlüsselrolle bei der Aufrechterhaltung des Chloridgleichgewichts im Körper. Obwohl der renale Chloridtransport mit dem Natriumtransport gekoppelt ist, kann der Chloridtransport manchmal vom Natriumtransport abweichen.
-
Hyperchlorämie kann aus einer Vielzahl von Bedingungen resultieren, einschließlich Wasserverlust, übermäßiger Chloridbelastung und metabolischer Azidose.
-
Die pathogene Ursache der Hyperchlorämie gibt Aufschluss darüber, wie die Störung zu behandeln ist: Wassermangel wird mit einer vernünftigen Wasserergänzung behandelt; übermäßige Chloridverabreichung durch Zurückhalten weiterer Chloridverabreichung; und hyperchlorämische metabolische Azidose durch Verabreichung von Bikarbonat.
Interessenkonflikt
Der Autor erklärt, dass kein Interessenkonflikt besteht.