Generischer Name: Meprobamat und Aspirin
Dosierung Form: Tabletten
Medically reviewed by Drugs.com. Zuletzt aktualisiert am 22. Dezember 2020.
- Übersicht
- Nebenwirkungen
- Dosierung
- Beratung
- Interaktionen
- Bilder
- Mehr
Code 1019A00
Rev. 09/06
Nur Rx
- Equagesic Beschreibung
- Equagesic – Klinische Pharmakologie
- Indikationen und Anwendung von Equagesic
- Kontraindikationen
- Warnhinweise
- Vorsichtsmaßnahmen
- Allgemein
- Informationen für Patienten
- Arzneimittelwechselwirkungen
- Wechselwirkungen mit Labortests
- Karzinogenese, Mutagenese, Beeinträchtigung der Fruchtbarkeit
- Schwangerschaft: Teratogene Wirkungen. Schwangerschaftskategorie X.
- Labor und Geburt
- Stillende Mütter
- Anwendung bei Kindern
- Anwendung bei älteren Menschen
- Nebenwirkungen
- Drogenmissbrauch und -abhängigkeit
- Überdosierung
- Dosierung und Verabreichung
- Anwendungshinweise
Equagesic Beschreibung
Jede Tablette von Equagesic, zur oralen Verabreichung, enthält 200 mg Meprobamat und 325 mg Aspirin. Chemisch gesehen ist Meprobamat 2-Methyl-2-propyl-1,3-Propandioldicarbamat. Seine Summenformel ist C9H18N2O4 mit einem Molekulargewicht von 218,25.
Aspirin ist chemisch gesehen 2-(Acetyloxy)-benzoesäure. Seine Summenformel ist C9H8O4 mit einem Molekulargewicht von 180,16. Es kommt als geruchlose weiße, nadelförmige, kristalline oder pulverförmige Substanz vor. Wenn es Feuchtigkeit ausgesetzt wird, hydrolysiert Aspirin in Salicyl- und Essigsäure und verströmt einen essigartigen Geruch. Es ist gut fettlöslich und schwer wasserlöslich. Die Strukturformeln von Meprobamat und Aspirin sind:
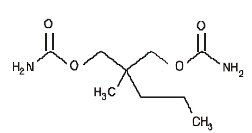
MEPROBAMAT
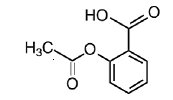
ASPIRIN
Die vorhandenen inaktiven Bestandteile sind D&C Gelb 10, FD&C Rot 3, FD&C Gelb 6, hydriertes Pflanzenöl, Magnesiumstearat, mikrokristalline Cellulose, Polacrilinkalium und Stärke.
Equagesic – Klinische Pharmakologie
Meprobamat ist ein Carbamat-Derivat, das (in Tier- und/oder Humanstudien) nachweislich Wirkungen an mehreren Stellen des zentralen Nervensystems, einschließlich des Thalamus und des limbischen Systems, hat. Aspirin ist ein nicht-narkotisches Analgetikum mit fiebersenkenden und entzündungshemmenden Eigenschaften.
Indikationen und Anwendung von Equagesic
Als Ergänzung zur kurzfristigen Behandlung von Schmerzen, die mit Verspannungen und/oder Angstzuständen einhergehen, bei Patienten mit Erkrankungen des Bewegungsapparates. Klinische Studien haben gezeigt, dass die Schmerzlinderung in diesen Situationen etwas stärker ist als bei Aspirin allein. Equagesic ist nicht für eine Anwendung von mehr als 10 Tagen vorgesehen.
Kontraindikationen
Verwendung in Schwangerschaft und Stillzeit
Ein erhöhtes Risiko für angeborene Missbildungen bei der Anwendung von leichten Beruhigungsmitteln (Meprobamat, Chlordiazepoxid und Diazepam) während des ersten Trimesters der Schwangerschaft wurde in mehreren Studien festgestellt. Da die Einnahme dieser Medikamente nur selten dringend erforderlich ist, sollte ihre Anwendung in diesem Zeitraum fast immer vermieden werden.
Aufgrund der bekannten Wirkung von nichtsteroidalen Antirheumatika (NSAIDs) auf das fetale Herz-Kreislauf-System (Verschluss des Ductus arteriosus) sollte die Anwendung während des dritten Trimesters der Schwangerschaft vermieden werden. Salicylatprodukte wurden auch mit Veränderungen der mütterlichen und neonatalen Hämostasemechanismen, einem geringeren Geburtsgewicht und perinataler Mortalität in Verbindung gebracht. Die Möglichkeit, dass eine Frau im gebärfähigen Alter zum Zeitpunkt der Einleitung der Therapie schwanger sein könnte, sollte in Betracht gezogen werden. Die Patientinnen sollten darauf hingewiesen werden, dass sie, wenn sie während der Therapie schwanger werden oder dies beabsichtigen, mit ihren Ärzten darüber sprechen sollten, ob ein Absetzen des Arzneimittels wünschenswert ist. Meprobamat passiert die Plazentaschranke. Es ist sowohl im Nabelschnurblut in oder nahe der mütterlichen Plasmakonzentration als auch in der Muttermilch stillender Mütter in zwei- bis vierfacher Konzentration vorhanden. Wenn die Anwendung von Meprobamat bei stillenden Patientinnen in Erwägung gezogen wird, sollten die höheren Konzentrationen des Arzneimittels in der Muttermilch im Vergleich zu den mütterlichen Plasmaspiegeln berücksichtigt werden.
Equagesic ist kontraindiziert bei Patienten mit akuter intermittierender Porphyrie und bei Patienten mit allergischen oder idiosynkratischen Reaktionen auf Aspirin, Meprobamat oder verwandte Verbindungen, wie Carbromal, Carisoprodol, Mebutamat, nichtsteroidale entzündungshemmende Arzneimittel, Salicylate oder Tybamat. Equagesic ist auch bei Patienten mit Asthma, Rhinitis und Nasenpolypen kontraindiziert. Die Aspirin-Komponente von Equagesic kann schwere Angioödeme, Bronchospasmen (Asthma) oder Urtikaria verursachen. Reye-Syndrom: Aspirin sollte bei Kindern und Jugendlichen bei Virusinfektionen mit oder ohne Fieber nicht angewendet werden, da bei gleichzeitiger Anwendung von Aspirin bei bestimmten Viruserkrankungen das Risiko eines Reye-Syndroms besteht.
Warnhinweise
Equagesic sollte Patienten mit Suizidalität nur mit Vorsicht und in geringen Mengen verschrieben werden.
Zusatzwirkungen: Da die ZNS-supprimierenden Wirkungen von Meprobamat und Alkohol oder Meprobamat und anderen Psychopharmaka additiv sein können, ist bei Patienten, die mehr als eines dieser Mittel gleichzeitig einnehmen, entsprechende Vorsicht geboten.
Alkohol-Warnhinweis: Patienten, die täglich drei oder mehr alkoholische Getränke zu sich nehmen, sollten über das Blutungsrisiko bei chronischem, starkem Alkoholkonsum während der Einnahme von Aspirin aufgeklärt werden.
Gerinnungsstörungen: Selbst niedrige Dosen von Aspirin können die Funktion der Blutplättchen hemmen, was zu einer Verlängerung der Blutungszeit führt. Dies kann Patienten mit vererbten (Hämophilie) oder erworbenen (Lebererkrankung oder Vitamin-K-Mangel) Blutungsstörungen beeinträchtigen.
Gastrointestinale Nebenwirkungen (GI): Zu den gastrointestinalen Nebenwirkungen gehören grobe GI-Blutungen, Sodbrennen, Übelkeit, Magenschmerzen und Erbrechen. Obwohl geringfügige Symptome des oberen Gastrointestinaltrakts, wie z. B. Dyspepsie, häufig sind und jederzeit während der Therapie auftreten können, sollten Ärzte auf Anzeichen von Ulzerationen und Blutungen achten, auch wenn zuvor keine gastrointestinalen Symptome aufgetreten sind. Die Ärzte sollten die Patienten über die Anzeichen und Symptome von Nebenwirkungen im Magen-Darm-Trakt und die zu ergreifenden Maßnahmen bei deren Auftreten informieren.
Peptische Ulkuskrankheit: Patienten mit einer aktiven peptischen Ulkuskrankheit in der Vorgeschichte sollten die Einnahme von Aspirin vermeiden, da es zu Reizungen der Magenschleimhaut und Blutungen führen kann.
Potenziell gefährliche Aufgaben
Patienten sollten darauf hingewiesen werden, dass Meprobamat die geistigen und/oder körperlichen Fähigkeiten beeinträchtigen kann, die für die Ausführung potenziell gefährlicher Aufgaben erforderlich sind, wie das Führen eines Kraftfahrzeugs oder das Bedienen von Maschinen. Solche Aufgaben sollten während der Einnahme dieses Arzneimittels vermieden werden.
Vorsichtsmaßnahmen
Allgemein
Equagesic sollte mit Vorsicht bei bestimmten Risikopopulationen verschrieben werden, wie z.B. bei älteren oder geschwächten Patienten und solchen mit akuten Bauchbeschwerden, Addison-Krankheit, Gerinnungsstörungen, erhöhtem Hirndruck, Kopfverletzungen, Hypothyreose, Beeinträchtigung der Leber- oder Nierenfunktion, Prostatahypertrophie oder Harnröhrenstriktur. Meprobamat wird in der Leber metabolisiert und über die Niere ausgeschieden. Um eine übermäßige Akkumulation zu vermeiden, sollte bei der Verabreichung an Patienten mit eingeschränkter Leber- oder Nierenfunktion Vorsicht walten. Meprobamat kann bei epileptischen Patienten gelegentlich Krampfanfälle auslösen.
Informationen für Patienten
Patienten sollten darüber informiert werden, dass Equagesic Aspirin enthält und von Patienten mit einer Aspirinallergie nicht eingenommen werden sollte.
Patienten mit einer Prädisposition für gastrointestinale Blutungen sollten darauf hingewiesen werden, dass die gleichzeitige Einnahme von Aspirin-haltigen Arzneimitteln und/oder Alkohol in dieser Hinsicht eine additive Wirkung haben kann.
Arzneimittelwechselwirkungen
Angiotensin Converting Enzyme (ACE)-Hemmer: Die hyponatriämischen und blutdrucksenkenden Wirkungen von ACE-Hemmern können durch die gleichzeitige Verabreichung von Aspirin aufgrund seiner indirekten Wirkung auf den Renin-Angiotensin-Umwandlungsweg abgeschwächt werden.
Acetazolamid: Die gleichzeitige Anwendung von Aspirin und Acetazolamid kann zu hohen Serumkonzentrationen von Acetazolamid (und zu Toxizität) führen, da es am Nierentubulus um die Sekretion konkurriert.
Alkohol, Allgemeinanästhetika, narkotische Analgetika, Sedativa, Tranquilizer wie Chlordiazepoxid oder andere ZNS-Depressiva: Die Wirkungen dieser Substanzen können verstärkt werden und zu einer verstärkten ZNS-Depression führen.
Gerinnungshemmende Therapie (Heparin und Warfarin): Bei Patienten, die eine Antikoagulationstherapie erhalten, besteht ein erhöhtes Risiko für Blutungen aufgrund von Wechselwirkungen zwischen den Medikamenten und der Wirkung auf die Blutplättchen. Aspirin kann Warfarin aus den Proteinbindungsstellen verdrängen, was zu einer Verlängerung sowohl der Prothrombinzeit als auch der Blutungszeit führt. Aspirin kann die gerinnungshemmende Wirkung von Heparin erhöhen und damit das Blutungsrisiko steigern.
Antikonvulsiva: Salicylate können proteingebundenes Phenytoin und Valproinsäure verdrängen, was zu einer Abnahme der Gesamtkonzentration von Phenytoin und einem Anstieg der Serumvalproinsäurekonzentration führt.
Betablocker: Die blutdrucksenkende Wirkung von Betablockern kann durch die gleichzeitige Verabreichung von Aspirin aufgrund der Hemmung der renalen Prostaglandine abgeschwächt werden, was zu einer verminderten renalen Durchblutung und einer Salz- und Flüssigkeitsretention führt.
Kortikosteroide: Bei Patienten, die gleichzeitig Kortikosteroide und chronische Aspirin-haltige Medikamente einnehmen, kann das Absetzen der Kortikosteroide zu Salicylismus führen, da Kortikosteroide die renale Clearance von Salicylaten erhöhen und nach dem Absetzen der Kortikosteroide die renale Clearance wieder normal ist.
Diuretika: Die Wirksamkeit von Diuretika bei Patienten mit zugrundeliegenden Nieren- oder Herz-Kreislauf-Erkrankungen kann durch die gleichzeitige Verabreichung von Aspirin aufgrund der Hemmung renaler Prostaglandine vermindert werden, was zu einem verminderten renalen Blutfluss und einer Salz- und Flüssigkeitsretention führt.
6-Mercaptopurin und Methotrexat: Knochenmarkstoxizität und Blutdyskrasie können durch die Verdrängung dieser Arzneimittel von sekundären Bindungsstellen und im Falle von Methotrexat auch durch die Verringerung seiner Ausscheidung entstehen.
Nonsteroidale Antirheumatika (NSAIDs): Die gleichzeitige Anwendung von Aspirin mit anderen NSAIDs sollte vermieden werden, da dies Blutungen verstärken oder zu einer verminderten Nierenfunktion führen kann.
Orale Hypoglykämika: Mäßige Dosen von Aspirin können die Wirksamkeit von oralen Hypoglykämika verstärken, was zu Hypoglykämie führen kann.
Uricosuric Agents (Probenicid und Sulfinpyrazon): Salicylate antagonisieren die urikosurische Wirkung, was ihre Wirksamkeit bei der Behandlung von Gicht verringert. Aspirin konkurriert mit diesen Mitteln um Proteinbindungsstellen.
Wechselwirkungen mit Labortests
Aspirin kann mit den folgenden Laborbestimmungen im Blut interferieren: Blut-Harnstoff-Stickstoff, Cholesterin, erhöhte Leberenzyme einschließlich Aspartat-Aminotransferase (AST), Nüchtern-Blutzucker, Hyperkaliämie, verlängerte Blutungszeit, Protein, Prothrombinzeit, Serum-Amylase, Serum-Kreatinin und Harnsäure. Aspirin kann die folgenden Laborbestimmungen im Urin beeinträchtigen: 5-Hydroxyindolessigsäure, Diessigsäure, Gerhardt-Keton, Glucose, Proteinurie, Harnsäure, spektrophotometrischer Nachweis von Barbituraten und Vanillylmandelsäure (VMA).
Karzinogenese, Mutagenese, Beeinträchtigung der Fruchtbarkeit
Die Verabreichung von Aspirin über 68 Wochen in einer Dosierung von 0,5 Prozent im Futter von Ratten war nicht karzinogen. Im Ames-Salmonella-Assay war Aspirin nicht mutagen; Aspirin induzierte jedoch Chromosomenaberrationen in kultivierten menschlichen Fibroblasten.
Schwangerschaft: Teratogene Wirkungen. Schwangerschaftskategorie X.
Siehe Gegenanzeigen
Labor und Geburt
Aspirin sollte während des dritten Trimesters der Schwangerschaft und während der Wehen und der Geburt vermieden werden, da es zu einem übermäßigen Blutverlust bei der Geburt führen kann. Es wurde über eine verlängerte Schwangerschaft und verlängerte Wehen aufgrund der Hemmung von Prostaglandinen berichtet.
Stillende Mütter
Stillende Mütter sollten Aspirin vermeiden, da Salicylat in die Muttermilch ausgeschieden wird. Die Einnahme hoher Dosen kann zu Hautausschlägen, Blutplättchenanomalien und Blutungen bei stillenden Säuglingen führen. Wegen des Potenzials für schwerwiegende unerwünschte Wirkungen bei stillenden Säuglingen sollte unter Berücksichtigung der Bedeutung des Arzneimittels für die Mutter entschieden werden, ob das Stillen unterbrochen oder das Arzneimittel abgesetzt werden soll (siehe auch Kontraindikationen).
Anwendung bei Kindern
Die Sicherheit und Wirksamkeit bei pädiatrischen Patienten unter 12 Jahren ist nicht erwiesen (siehe Kontraindikationen).
Anwendung bei älteren Menschen
Klinische Studien mit Meprobamat in Kombination mit Aspirin schlossen nicht genügend Probanden im Alter von 65 Jahren und darüber ein, um festzustellen, ob sie anders als jüngere Probanden reagieren. Im Allgemeinen sollte die Dosis für ältere Patienten vorsichtig gewählt werden, wobei in der Regel am unteren Ende des Dosierungsbereichs begonnen werden sollte, um die größere Häufigkeit einer verminderten Leber-, Nieren- oder Herzfunktion sowie einer Begleiterkrankung oder einer anderen Arzneimitteltherapie zu berücksichtigen.
Nebenwirkungen
Gesamtkörper
Fieber, Unterkühlung, Durst.
Allergische oder idiosynkratische
Schwere Überempfindlichkeitsreaktionen, einschließlich Anaphylaxie, angioneurotisches Ödem, Anurie, Asthma, Bronchospasmus, bullöse Dermatitis, Schüttelfrost, Erythema multiforme, exfoliatives Erythroderma, Larynxödem, Oligurie, Proktitis, Purpura, Stevens-Johnson-Syndrom, Stomatitis und Urtikaria. Mildere Reaktionen sind durch einen juckenden, erythematösen makulopapulösen oder urtikariellen Ausschlag gekennzeichnet, der generalisiert oder auf die Leistengegend beschränkt sein kann. Zu den weiteren Reaktionen gehören akute nicht-thrombozytopenische Purpura, Adenopathie, Kreuzallergie zwischen Meprobamat/Mebutamat und Meprobamat/Carbromal, Ekchymosen, Eosinophilie, fixe Arzneimitteleruption mit Kreuzreaktion auf Carisoprodol, Leukopenie, periphere Ödeme und Petechien.
Kardiovaskulär
Verschiedene Formen von Herzrhythmusstörungen, Hypotonie, Herzklopfen, Synkope, Tachykardie und vorübergehende EKG-Veränderungen.
Zentralnervensystem
Agitation, Ataxie, Hirnödem, Koma, Verwirrung, Schwindel, Schläfrigkeit, Dysphorie, Euphorie, schnelle EEG-Aktivität, Kopfschmerzen, Beeinträchtigung der visuellen Akkommodation, Lethargie, Überstimulation, paradoxe Erregung, Parästhesien, Sedierung, undeutliche Sprache, subdurale oder intrakranielle Blutungen, Krampfanfälle, Schwindel und Schwäche.
Flüssigkeit und Elektrolyte
Dehydratation, Hyperkaliämie, metabolische Azidose und respiratorische Alkalose.
Gastrointestinal
Bauchschmerzen, Verstopfung, Durchfall, Dyspepsie, epigastrische Beschwerden, Magenbeschwerden, gastrointestinale Blutungen, Sodbrennen, Hepatitis, Übelkeit, Pankreatitis, Reye-Syndrom, vorübergehende Erhöhungen der Leberenzyme, Ulzeration und Perforation und Erbrechen.
Hämatologisch (siehe auch „Allergisch oder idiosynkratisch“)
Es wurde über Agranulozytose und aplastische Anämie berichtet, obwohl kein kausaler Zusammenhang festgestellt wurde, Koagulopathie, disseminierte intravasale Gerinnung, Exazerbation porphyrischer Symptome, hämolytische Anämie, Eisenmangelanämie, okkulter Blutverlust, Verlängerung der Prothrombinzeit, Thrombozytopenie und thrombozytopenische Purpura.
Muskuloskelettale Erkrankungen
Rhabdomyolyse
Stoffwechsel
Hyperglykämie und Hypoglykämie
Reproduktive Erkrankungen
Verlängerte Schwangerschaft und Wehen, Totgeburten, Säuglinge mit niedrigem Geburtsgewicht und Blutungen vor und nach der Entbindung.
Respiratorisch
Akute Atemwegsobstruktion, Hyperpnoe, Lungenödem und Tachypnoe.
Besondere Sinne
Hörverlust und Tinnitus.
Urogenital
Interstitielle Nephritis, Papillennekrose, Proteinurie und Niereninsuffizienz und -versagen.
Drogenmissbrauch und -abhängigkeit
Körperliche Abhängigkeit, psychische Abhängigkeit und Missbrauch sind aufgetreten. Eine chronische Intoxikation nach längerer Einnahme von meist höheren als den empfohlenen Dosen äußert sich durch Ataxie, undeutliche Sprache und Schwindel. Daher ist eine sorgfältige Überwachung der Dosis und der verordneten Mengen ratsam, ebenso wie die Vermeidung einer längeren Einnahme, insbesondere bei Alkoholikern und anderen Patienten, die bekanntermaßen dazu neigen, übermäßige Mengen von Drogen einzunehmen. Ein plötzliches Absetzen des Arzneimittels nach längerem und übermäßigem Gebrauch kann das Wiederauftreten bereits bestehender Symptome wie Anorexie, Angstzustände oder Schlaflosigkeit oder Entzugserscheinungen wie Ataxie, Verwirrtheit, Halluzinose, Muskelzuckungen, Zittern, Erbrechen und selten auch Krampfanfälle auslösen. Solche Krampfanfälle treten eher bei Personen mit Schädigungen des Zentralnervensystems oder bereits bestehenden oder latenten krampfartigen Störungen auf. Das Auftreten von Entzugserscheinungen erfolgt in der Regel innerhalb von 12 bis 48 Stunden nach Absetzen von Meprobamat; die Symptome klingen in der Regel innerhalb der nächsten 12 bis 48 Stunden ab. Wenn eine übermäßige Dosis über Wochen oder Monate hinweg eingenommen wurde, sollte die Dosis schrittweise über einen Zeitraum von 1 bis 2 Wochen reduziert werden, anstatt sie abrupt abzusetzen. Alternativ kann ein lang wirkendes Barbiturat eingesetzt und dann allmählich abgesetzt werden.
Überdosierung
Die Behandlung einer Überdosierung mit Equagesic ist im Wesentlichen symptomatisch und unterstützend. In Fällen, in denen überhöhte Dosen von Equagesic eingenommen wurden, tritt rasch Schlaf ein, und Blutdruck, Puls und Atemfrequenz sinken auf Basalwerte. Im Magen verbliebene Reste des Arzneimittels sollten entfernt und symptomatisch behandelt werden. Nach Erbrechen und/oder Spülung kann Aktivkohle die Absorption von Aspirin und Meprobamat verringern. Sollte die Atmung oder der Blutdruck beeinträchtigt werden, sollten Atemhilfe, Stimulanzien des zentralen Nervensystems und Druckmittel je nach Bedarf vorsichtig verabreicht werden. Diurese, osmotische (Mannitol-)Diurese, Peritonealdialyse und Hämodialyse wurden erfolgreich zur Entfernung von Aspirin und Meprobamat eingesetzt. Die Alkalisierung des Urins erhöht die Ausscheidung von Salicylaten. Eine sorgfältige Überwachung der Urinausscheidung ist erforderlich, und es sollte darauf geachtet werden, eine Überwässerung zu vermeiden. Rückfälle und Todesfälle nach anfänglicher Genesung wurden auf eine unvollständige Magenentleerung und verzögerte Absorption zurückgeführt. Salicylat-Toxizität kann durch akute Einnahme (Überdosierung) oder chronische Intoxikation entstehen. Zu den Anzeichen und Symptomen gehören Bauchschmerzen, Säure-Basen-Störungen mit Entwicklung einer metabolischen Azidose, Krämpfe, Delirium, Hyperpnoe, Hyperthermie, Hypoprothrombinämie, Unruhe, Tinnitus (Ohrensausen) und Erbrechen. Die ersten Anzeichen einer Salicylüberdosierung (Salicylismus), einschließlich Tinnitus, treten bei Plasmakonzentrationen von annähernd 200 μg/ml auf. Plasmakonzentrationen von Aspirin über 300 μg/ml sind eindeutig toxisch. Schwere toxische Wirkungen treten bei Konzentrationen über 400 μg/ml auf. Die tödliche Einzeldosis von Aspirin bei Erwachsenen ist nicht mit Sicherheit bekannt, aber bei 30 g ist mit dem Tod zu rechnen. Bei tatsächlicher oder vermuteter Überdosierung sollte sofort ein Giftnotrufzentrum kontaktiert werden. Eine sorgfältige medizinische Behandlung ist unerlässlich. Bei einer akuten Überdosierung von Aspirin kann es zu schweren Säure-Basen- und Elektrolytstörungen kommen, die durch Hyperthermie und Dehydratation kompliziert werden. Eine respiratorische Alkalose tritt früh auf, während Hyperventilation vorhanden ist, wird aber schnell von einer metabolischen Azidose gefolgt. Die Behandlung einer Aspirin-Überdosierung besteht in erster Linie in der Unterstützung der Vitalfunktionen, der Steigerung der Salicylatausscheidung und der Korrektur der Säure-Basen-Störung. Es wird empfohlen, den Magen so schnell wie möglich nach der Einnahme zu entleeren und/oder eine Magenspülung durchzuführen, auch wenn der Patient spontan erbrochen hat. Nach der Spülung und/oder dem Erbrechen ist die Verabreichung von Aktivkohle in Form eines Breis von Vorteil, wenn seit der Einnahme weniger als 3 Stunden vergangen sind. Die Adsorption von Aktivkohle sollte nicht vor dem Erbrechen und der Spülung erfolgen.
Der Schweregrad einer Aspirin-Intoxikation wird durch Messung des Salicylatspiegels im Blut bestimmt. Der Säure-Basen-Status sollte durch serielle Blutgas- und Serum-pH-Messungen genau verfolgt werden. Auch das Flüssigkeits- und Elektrolytgleichgewicht sollte aufrechterhalten werden. In schweren Fällen sind Hyperthermie und Hypovolämie unmittelbar lebensbedrohlich. Die Kinder sollten mit lauwarmem Wasser abgetupft werden. Die Ersatzflüssigkeit sollte intravenös verabreicht und mit der Korrektur der Azidose ergänzt werden. Plasmaelektrolyte und pH-Wert sollten überwacht werden, um die alkalische Diurese von Salicylat zu fördern, wenn die Nierenfunktion normal ist. Zur Kontrolle einer Hypoglykämie kann eine Glukoseinfusion erforderlich sein.
Hämodialyse und Peritonealdialyse können durchgeführt werden, um den Wirkstoffgehalt im Körper zu reduzieren. Bei Patienten mit Niereninsuffizienz oder in Fällen lebensbedrohlicher Vergiftungen ist in der Regel eine Dialyse erforderlich. Bei Säuglingen und Kleinkindern kann eine Austauschtransfusion angezeigt sein. Selbstmordversuche mit Meprobamat haben zu Ataxie, Koma, Schläfrigkeit, Lethargie, Schock, Stupor und respiratorischem und vasomotorischem Kollaps geführt. Einige Selbstmordversuche verliefen tödlich. Die folgenden Daten wurden in der Literatur und aus anderen Quellen berichtet. Es ist nicht davon auszugehen, dass diese Daten mit jedem einzelnen Fall korrelieren (unter Berücksichtigung von Faktoren wie der individuellen Empfindlichkeit und der Zeitspanne zwischen Einnahme und Behandlung), sondern sie stellen die übliche Bandbreite dar. Akute einfache Überdosierung (Meprobamat allein): Der Tod wurde bei der Einnahme von nur 12 Gramm Meprobamat und das Überleben bei der Einnahme von bis zu 40 Gramm berichtet.
BLOOD LEVELS
0,5 bis 2 mg Prozent stellen den üblichen Blutspiegelbereich von Meprobamat nach therapeutischen Dosen dar. 3 bis 10 mg Prozent entsprechen in der Regel dem Auftreten von leichten bis mittelschweren Symptomen einer Überdosierung, wie Stupor oder leichtes Koma. 10 bis 20 mg Prozent entsprechen in der Regel einem tieferen Koma, das eine intensivere Behandlung erfordert. Einige Todesfälle treten auf. Bei einer Dosierung von mehr als 20 mg Prozent ist mit mehr Todesfällen als Überlebenden zu rechnen. Akute kombinierte Überdosierung (Meprobamat mit anderen psychotropen ZNS-Medikamenten oder Alkohol): Da die Wirkungen additiv sein können, kann die Einnahme einer niedrigen Dosis Meprobamat zusammen mit einer dieser Substanzen (oder ein relativ niedriger Blut- oder Gewebespiegel) nicht als prognostischer Indikator verwendet werden.
Dosierung und Verabreichung
Die übliche Dosierung von Equagesic ist eine oder zwei Tabletten, jede Tablette enthält Meprobamat, 200 mg, und Aspirin, 325 mg, oral 3 bis 4 mal täglich, je nach Bedarf zur Linderung von Schmerzen bei Anspannung oder Angstzuständen. Equagesic wird für Patienten unter 12 Jahren nicht empfohlen.
Anwendungshinweise
Equagesic® (Meprobamat- und Aspirintabletten) Tabletten, 200 mg Meprobamat und 325 mg Aspirin, sind wie folgt erhältlich: NDC 10551-091-10, rosafarbene und gelbe, zweischichtige, runde, gekerbte Tablette mit der Aufschrift „LP“ und „91“, in Flaschen zu 100 Tabletten.
Bei kontrollierter Raumtemperatur aufbewahren, 20°-25°C (68°-77°F).
Vor Feuchtigkeit schützen.
Dicht verschlossen halten.
Vor Licht schützen.
In einem lichtbeständigen, dichten Behälter aufbewahren.
Hergestellt für:
Leitner Pharmaceuticals™, LLC
Bristol, TN 37620
www.leitnerpharma.com
Hergestellt von:
Mikart, Inc.
Atlanta, GA 30318
1019A00
| Equagesic Meprobamat und Aspirin Tabletten |
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
Etikettierer – Mikart, Inc.