Das desmoplastische Melanom, eine seltene Variante des Melanoms, stellt eine diagnostische Herausforderung für den Kliniker dar, da die Tumoren häufig als unspezifische fleischfarbene oder amelanotische Plaques oder Knötchen auftreten. Sie treten häufiger bei Männern als bei Frauen auf und sind häufig an Kopf und Hals zu finden.1,2 Ihr harmloses Erscheinungsbild kann zu einer Verzögerung der Diagnose führen und erklärt möglicherweise, warum desmoplastische Melanome zum Zeitpunkt der Biopsie oft tief infiltriert sind. Das desmoplastische Melanom entsteht in etwa einem Drittel der Fälle de novo.1 In den übrigen Fällen tritt es in Verbindung mit einem darüber liegenden Melanom in situ auf, meist einem Lentigo-Maligna-Melanom.1 Histologisch sind desmoplastische Melanome durch maligne Spindelzellen in einem dichten fibrotischen Stroma gekennzeichnet (Abbildung 1). Angrenzende lymphatische Aggregate und eine perineurale Beteiligung sind häufige Merkmale,2 während Pigmentierung und atypische Mitosen eher selten vorkommen. Desmoplastische Melanome können je nach Grad der Desmoplasie und Zellularität als gemischt oder rein klassifiziert werden. Innerhalb der gemischten desmoplastischen Melanome gibt es Bereiche, die histologische Merkmale konventioneller Melanome aufweisen, während andere eher typische desmoplastische Merkmale zeigen. Das reine desmoplastische Melanom weist einen höheren Grad an Desmoplasie und weniger Tumorzellen auf als der gemischte Typ.1 Der reine Subtyp ist tendenziell weniger aggressiv und metastasiert seltener in die Lymphknoten.1 Fehlt eine In-situ-Komponente (Abbildung 2), kann das desmoplastische Melanom bei einer routinemäßigen Hämatoxylin- und Eosinfärbung nicht von anderen Spindelzelltumoren unterschieden werden; daher ist in der Regel eine immunhistochemische Färbung erforderlich. Die zuverlässigsten Färbungen zur Bestätigung der Diagnose eines desmoplastischen Melanoms sind S100 und SOX10 (SRY-verwandte HMG-Box 10) (Abbildung 3) (eTabelle).3
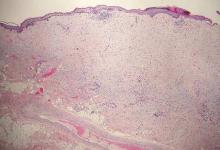
Figure 1. Desmoplastisches Melanom mit Spindelmelanozyten in einem dicht fibrotischen Stroma (H&E, Originalvergrößerung ×40).
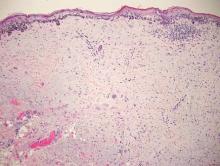
Abbildung 2. Zusammenfluss von atypischen Melanozyten entlang der dermoepidermalen Grenze, die mit einem Melanom in situ über einem desmoplastischen Melanom übereinstimmen (H&E, Originalvergrößerung ×100).

Abbildung 3. SOX10 (SRY-verwandte HMG-Box 10), nukleäre Expression von Spindelmelanozyten in der fibrotischen Dermis und darüber liegende Konfluenz von Melanozyten an der dermoepidermalen Grenzfläche bei desmoplastischem Melanom (Originalvergrößerung ×100).
Das atypische Fibroxathom tritt typischerweise als Knötchen in der Kopf- und Halsregion oder anderen sonnenexponierten Bereichen bei älteren Menschen auf und wird häufiger bei Männern als bei Frauen beobachtet.4 Histologisch bestehen atypische Fibroxanthome aus pleomorphen spindelförmigen, epitheloiden und vielkernigen Riesenzellen mit zahlreichen und atypischen Mitosen (Abbildung 4).5 Das atypische Fibroxanthom gilt als Ausschlussdiagnose; daher müssen andere dermale Spindelzelltumoren ausgeschlossen werden, bevor die Diagnose gestellt werden kann. Atypische Fibroxanthome weisen in der Regel eine negative Färbung für Zytokeratin, S100, SOX10 und Desmin auf, in einigen Fällen findet sich jedoch eine positive fokale Färbung für Glattmuskel-Aktin.4 Mehrere immunhistochemische Marker, darunter CD10, haben eine Reaktivität bei atypischen Fibroxanthomen gezeigt,4 aber keiner dieser Marker hat eine hohe Spezifität für diesen Tumor; daher bleibt es eine Ausschlussdiagnose.
Kutane Angiosarkome sind aggressive Tumoren, die trotz angemessener Behandlung mit chirurgischer Resektion und postoperativer Strahlenbehandlung mit einer hohen Sterblichkeitsrate verbunden sind. Sie treten typischerweise als ekchymotische Flecken oder Knötchen im Gesicht oder auf der Kopfhaut älterer Patienten auf.6,7 Ionisierende Strahlung und chronische Lymphödeme sind Risikofaktoren für kutane Angiosarkome.6 Histologisch gesehen bestehen gut differenzierte kutane Angiosarkome aus unregelmäßigen, anastomosierenden Gefäßkanälen, die die Dermis durchziehen (Abbildung 5).6,7 Weniger gut differenzierte Tumore können Spindelzellen enthalten und keine offensichtlichen Gefäßstrukturen aufweisen; daher ist die Immunhistochemie in diesen Fällen für die korrekte Diagnose unerlässlich. Kutane Angiosarkome weisen typischerweise eine positive Färbung für ERG-Protein (ETS-verwandtes Gen), CD31, CD34 und Faktor VIII auf.6,8 Leider können diese Tumoren gelegentlich auch Zytokeratin anfärben, was zur falschen Diagnose eines Karzinoms führen kann.6

 |
 |
|
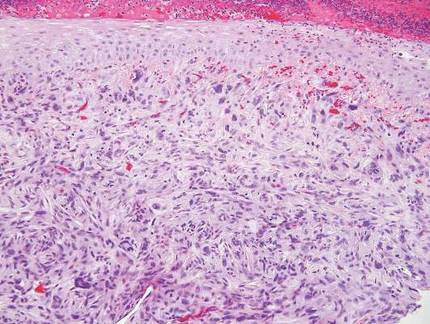
| Abbildung 4. Pleomorphe spindelförmige, epitheloide und vielkernige Riesenzellen mit atypischen Mitosen, die die Dermis in einem atypischen Fibroxanthom ausfüllen (H&E, Originalvergrößerung ×200). |
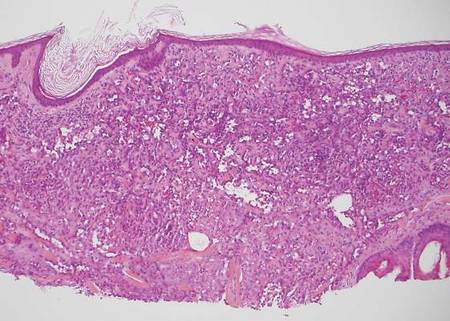
Abbildung 5. Anastamosierende Gefäßkanäle, die die Kollagenbündel durchdringen und die Epidermis bei einem kutanen Angiosarkom verzehren (H&E, Originalvergrößerung ×100). |
Das kutane Leiomyosarkom ist ein Neoplasma der glatten Muskulatur, das von den Musculi arrector pili, den glatten Muskeln der Genitalien oder den glatten Muskeln der Gefäße ausgeht. Es tritt typischerweise als einzelne Plaques oder Knötchen an Armen und Beinen von Personen über 50 Jahren auf.9 Kutane Leiomyosarkome können entweder als dermal, d. h. mindestens 90 % des Tumors sind auf die Dermis beschränkt, oder als subkutan klassifiziert werden; diese Unterscheidung ist wichtig, da der letztere Typ eine höhere Metastasierungsrate und eine schlechtere Prognose aufweist.9 Da dieser Tumor von der glatten Muskulatur abstammt, können gut differenzierte Tumoren Merkmale typischer glatter Muskelzellen aufweisen, darunter zigarrenförmige Zellkerne mit angrenzenden Glykogenvakuolen (Abbildung 6). Wenn die Bildung von Faszikeln beobachtet wird, kann dies ein zusätzlicher Hinweis auf die Diagnose sein. Bei schlecht differenzierten Tumoren ist die Immunhistochemie von unschätzbarem Wert. Leiomyosarkome weisen häufig eine positive Färbung für Glattmuskel-Aktin, muskelspezifisches Aktin, h-Caldesmon, Desmin und Calponin auf.9-11