Chlorid er den hyppigst forekommende anion i den ekstracellulære væske (ECF). Hyperchloræmi er defineret som en stigning i kloridkoncentrationen i plasmavandet. Hyperchloræmi og et relativt overskud af chlorid i kroppen er blevet sat i forbindelse med udvikling af nedsat nyreblodgennemstrømning,1,2 øget interstitiel ødem, herunder i nyrerne og det gastrointestinale system,3 overdreven morbiditet og mortalitet hos kritisk syge patienter,4,5 og nedsat overlevelse og helbredelse hos patienter med akut nyreskade.6 Ligesom natrium og andre kemikalier i ECF-kompartmentet er chloridkoncentrationen reguleret. Det organ, der er ansvarligt for opretholdelsen af kloridbalancen i kroppen, er nyrerne. I denne artikel gennemgås nyrens håndtering af klorid og kliniske situationer, hvor der kan forekomme hyperchloræmi.
Renal håndtering af klorid
Kloridniveauet i plasmaet reguleres af nyren. Nyren filtrerer frit klorid gennem glomeruliens basalmembraner. Den mængde klorid, der udskilles i urinen, bestemmes af det klorid, der filtreres af glomeruli og af en række transportprocesser, der finder sted langs nefronet. Under normale omstændigheder absorberes over 60 % af det filtrerede klorid langs den proximale tubulus. I den tidlige proximale tubulus absorberes natrium sammen med en forholdsmæssig mængde vand, således at natriumkoncentrationen ikke ændres. Derimod absorberes bicarbonat og andre ikke-klorid anioner hurtigt sammen med natrium og fjernes fra filtratet7 (fig. 1A). Efterhånden som natrium og ikke-klorid anioner absorberes i de tidlige proximale tubulussegmenter (S1 og S2), stiger kloridkoncentrationen i lumen af den proximale tubulus. Når den tubulære væske når det sidste segment af den proximale tubulus (S3), er kloridkoncentrationen høj i forhold til plasmakoncentrationen, hvilket gør det muligt at absorbere klorid passivt ned ad koncentrationsgradienten (fig. 1B). Den transepitheliale permeabilitet for klorid er højere end permeabiliteten for bikarbonat, så på trods af den peritubulære-til-lumen gradient for bikarbonat overstiger transporten af klorid, der forlader lumen, den bikarbonat, der kommer ind i tubulærvæsken.

(A) I den tidlige proximale tubulus sker isotonisk natriumabsorption med organiske opløsninger, bicarbonat, fosfat sammen med vand, hvilket resulterer i en stigende kloridkoncentration. (B) Den høje kloridkoncentration i lumen begunstiger også transcellulær og paracellulær transport. Intercellulære junctions i den senere proximale tubulus bliver mere permeable for klorid, hvilket letter den paracellulære transport. Selv når bikarbonatkoncentrationen falder i lumen, spiller Na+-H+-udvekslingen fortsat en rolle i NaCl-reabsorptionen. Transcellulær natriumchloridabsorption kan ske via en kobling af Na+-H+-udveksling med chlorid-organisk anionudveksling (format, oxalat). Den organiske syre (myresyre eller oxalsyre) genanvendes i cellerne.
I den tidlige del af den proximale tubulus sker kloridabsorption også via apikale klorid-anion- (format, oxalat, base) udvekslere, og det forlader cellen via basolaterale membrantransportører8 (fig. 1B). Ved hyperchloræmisk metabolisk acidose på grund af HCl- eller ammoniumchloridbelastning er chloridreabsorptionen i den proximale tubulus reduceret, til dels på grund af reduktionen af organiske aniontransportører, der letter natriumchloridtransporten9 , samt reduktionen af lumen-til-peritubulær gradient for chlorid.
Den tykke ascenderende lem af Henle-løkken (TALH) er et vigtigt sted for chloridreabsorption.10 På dette sted transporteres natrium, kalium og klorid samtidig via en natrium-kalium-2 klorid co-transporter (NKCC2) (fig. 2). Klorid kommer ind i TALH-cellen og forlader dens basolaterale aspekt gennem en elektrogene kloridkanal eller via den elektroneutrale kaliumklorid-cotransporter. Kloridbevægelsen gennem den basolaterale kloridkanal (CLC-NKB) bidrager til dannelsen af en positiv (lumen) til negativ (basolateral) potentialegradient i det transepitheliale potentiale. Det intracellulære positive potentiale, der ville blive skabt af kloridbevægelsen ud af cellen, opvejes af den basolaterale elektrogene Na+-K+ ATPase, der transporterer natrium ud af cellen til gengæld for kalium ind i cellen i et forhold på 3-2. ROMK-kaliumkanaler på den apikale TALH-cellemembran bidrager til det positive lumenpotentiale (intracellulært negative) gennem den ledende bevægelse af kaliumioner fra celle til lumen. Den samlede virkning er, at klorid, natrium og kalium kommer ind i cellen via NKCC2, og for det meste forlader klorid cellen via den basolaterale ClC-NKB-kloridkanal, natrium forlader cellen via Na+-K+ ATPase, og kalium genbruges tilbage til lumen via ROMK-kanalen eller forlader basolateralt via KCl-kotransporteren. Den tætte kobling mellem natrium- og kloridtransport i TALH understreges af en af varianterne af Bartters syndrom, hvor defekter i basolaterale kloridkanaler forstyrrer natriumkloridreabsorptionen og efterligner den nyredefekt, der er observeret med unormale NKCC2-proteiner. Selv om andre transportører på den peritubulære side af TAL-cellen, såsom KCl-kotransporteren, transporterer klorid på en natriumuafhængig måde, er det meste af det klorid, der absorberes af TALH, koblet med natriumreabsorption. Derfor vil faktorer, der øger natriumreabsorptionen i dette segment, også øge kloridreabsorptionen.
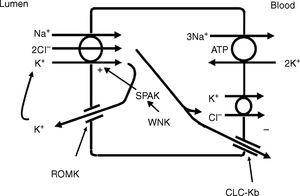
Den tykke opstigende gren af Henle- løkken absorberer klorid via den apikale Na+-K+-2Cl-kotransporter (NKCC2), og klorid forlader cellen via en basolateral kloridkanal og via K+-Cl-kotransport. K+ genanvendelse i lumen og basolateral ledende Cl-udgang via CLC-Kb bidrager til den positive-negative lumen- til basolaterale transepitheliale gradient. Intracellulært klorid kan regulere NKCC2-transporten gennem en klorid-sensitiv WNK-kinase (WNK), der kan aktivere STE20/SPS1-relateret prolin/alaninrig kinase (SPAK) og NKCC2, når det intracellulære Cl-indhold er lavt. På den anden side, når klorid ophobes i cellen på grund af defekter i den basolaterale kloridkanaludgangsvej, er NKCC2-transporten blokeret. Når NKCC2 stimuleres, f.eks. af antidiuretisk hormon, øges kloridindgangen, men den basolaterale Cl-konduktans øges også.
I den distale konvoluted tubulus transporteres natrium og klorid fra lumenet ind i cellen af en natrium-klorid co-transporter (NCC)11 (fig. 3). Drivkraften for flytning af klorid fra lumen ind i cellerne kommer fra den natriumgradient fra lumen til celle, som genereres af den basolaterale Na+-K+ ATPase, der pumper natrium ud af cellen og derved opretholder lave intracellulære natriumkoncentrationer. Yderligere regulering af NCC og NKCC kan ske gennem WNK-kinaser, der kan fungere som kloridsensorer12 og kan regulere disse transportører ved at ændre trafikken eller deres fosforyleringstilstand.13 I senere dele af den distale konvolutterede tubulus kan et negativt lumenpotentiale, der genereres af natriumbevægelse gennem den apikale epitheliale natriumkanal (ENaC), også fungere som drivkraft for passiv kloridreabsorption. Således udviser segmenterne i den distale konvolutterede tubulus direkte kobling af natrium- og kloridtransport via NCC og indirekte kobling af transport via passiv bevægelse ned ad en elektrokemisk gradient.
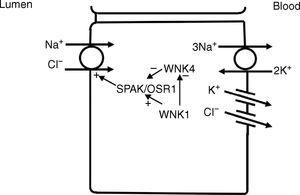
I den distale konvolut-tubulus optages natrium og klorid i lumenet ind i cellen via en Na+-Cl-kotransporter (NCC). Transporten via NCC drives af et lavt intracellulært natrium, der hovedsagelig genereres af den basolaterale Na+-K+ ATPase. WNK1-kinasen kan fungere som en kloridsensor for at blokere hæmning af NCC af WNK4-kinasen.
Samlerkanalen spiller en vigtig rolle i forbindelse med bestemmelsen af kloridindholdet i den endelige urin. Kloridreabsorption i denne del af nefronet bidrager til at bevare klorid som reaktion på lavt kloridindtag og kan bidrage til de hypertensive virkninger af en kost med højt natriumkloridindhold. Det meste af det natrium, der reabsorberes i samlekanalen, sker i hovedcellerne via aldosteronregulerede apikale epitheliale natriumkanaler. Kloridreabsorption i samleleddet kan ske via paracellulær kloridabsorption, der drives af det negative transepitheliale potentiale i lumen, som genereres af natriumstrømmen fra lumen til celle gennem ENaC (Fig. 4A). Desuden kan klorid i interkalerede celler af B-typen og ikke-A-typen ikke-B-typen transporteres via pendrin, en klorid-bicarbonat-udveksler, hvor klorid bevæger sig fra lumen til celle, mens bicarbonat udskilles i lumen (Fig. 4B). Forholdet mellem forskellige natrium- og kloridtransportprocesser i denne del af nefronet blev illustreret i en nylig artikel af Vallet og kolleger.14 Forfatterne udførte en række fysiologiske manøvrer for at bestemme deres virkninger på ENaC- og pendrinproteinniveauerne i nyren. Langvarig NaCl-belastning mindskede signifikant pendrinproteinniveauerne, mens der var et fald i den “aktive” ENaC-γ-indgivelse og en øget β-underenhed. Der blev observeret en dissociation mellem natrium- og kloridtransport, men ved hæmning af natrium-klorid-cotransporteren med hydrochlorthiazid faldt pendrin-niveauerne, men ENaC-niveauerne steg. NaCl-restriktion øgede pendrin-ekspressionen.15 En øget luminal bikarbonatkoncentration, som ville blive skabt af pendrin-medieret bikarbonatudskillelse, påvirker natriumreabsorptionen ved at øge aktiviteten af nedstrøms ENaC.16 Natriumchloridtransport af interkalerede celler kan også forbedres ved tilstedeværelsen af en thiazidfølsom apikal natriumafhængig chlorid-bicarbonat-udveksler (NDCBE, Slc4A8), som transporterer 1 natrium- og 2 bicarbonat-ioner fra lumenet ind i cellen i bytte for 1 chlorid-ion, som forlader cellen. Hvis NDCBE-transporten er koblet med pendrin-medieret klorid-bikarbonat-udveksling, kan de to transportører, der arbejder sammen, resultere i nettonatrium-klorid-reabsorption fra lumen, da bikarbonat genbruges ind og ud af cellen, mens natrium og klorid kommer ind i cellen17 (fig. 4B). Faktorer, der ændrer forholdet mellem mængderne eller aktiviteterne af disse to anionbyttere, kan være afgørende for nettovirkningen på bikarbonatudskillelsen og kloridreabsorptionen. En anden transportør, der kan være involveret i udskillelsen af for meget klorid i kroppen, er Slc26A9-transporteren, der kan fungere som en kloridkanal i de medullære dele af den samlende kanal.18 Den kan modificere virkningen af kloridbelastninger ved at øge kloridsekretionen under forhold med kloridoverskud. Knockout af dette gen resulterer i en prædisponering for hypertension. Mus med mangel på dette protein udvikler hypertension, når de udsættes for en høj natriumkloridbelastning.18 Selv om Slc26a9-transporteren synes at spille en vigtig rolle i håndteringen af store natriumkloridbelastninger, er reguleringen af den native transporteraktivitet som reaktion på varierende natriumkloridbelastninger fortsat ukendt.

(A) Klorid kan udskilles eller reabsorberes i samleleddet. En del af kloridabsorptionen drives af et negativt lumenpotentiale og paracellulær bevægelse. (B) Transcellulær reabsorption af klorid kan også ske via kobling af den apikale Pendrin klorid-bikarbonat-udveksler til den SLCA48 natriumafhængige klorid-2-bikarbonat-udveksler (NDCBE). To cykler af Pendrin vil resultere i, at der kommer to klorider ind i cellen i bytte for to bikarbonater, mens NDCBE vil transportere et natrium og to bikarbonater i bytte for et klorid ud. Nettoresultatet vil være transport af 1 natrium og 1 klorid ind i cellen. Forskelle i de apikale Pendrin- og NDCBE-aktiviteter kunne afgøre, om Cl- sekretion eller absorption dominerer.
Kloridkoncentration og hyperchloræmi
Serumkloridniveauet måles generelt som en koncentration af klorid i et serumvolumen. Den biologisk aktive kloridkoncentration er koncentrationen af frit klorid i plasmavandet. Klorid måles oftest ved hjælp af en sølvkloridelektrode enten i en direkte eller fortyndet serumprøve.19 Automatiserede metoder, som findes i mange laboratorier, indebærer fortynding af serumprøven med reagens, således at prøvens volumen antages at have et normalt vandindhold, og der foretages skøn baseret på en antagelse om en normal fortyndingsfaktor. Når serummets faste bestanddele er meget høje, som det kan forekomme ved hypertriglyceridæmi og multipel myelom, kan der opstå pseudohypokloræmi. Pseudohyperchloræmi kan også ses i forbindelse med bromid- eller jodidforgiftning. Interaktionen mellem bromid eller jodid og sølv-chlorid-elektroden genererer en større spændingsændring end chlorid, hvilket giver indtryk af for meget chlorid i blodet.20,21
Orsager til ægte hyperchloræmiHyperchloræmi på grund af vandtab
Hyperchloræmi kan skyldes en række mekanismer (tabel 1). Vandtab, der overstiger chloridtab, kan øge chloridkoncentrationen.22 Ved dehydrering er den renale reaktion at bevare vand og sænke urinproduktionen. Da der også kan være en komponent af volumenudtømning ved sværere grader af dehydrering, sker bevarelse af klorid såvel som natrium via øget proximal tubulusreabsorption af klorid og andre solutater og reduceret tilførsel af klorid og natrium til mere distale nefronsegmenter. Den øgede proximale tubulære reabsorption af tubulær væske og dens indhold vil ikke nødvendigvis ændre kloridkoncentrationen, da absorptionen af væske sker isotonisk. Behandlingen af vandmangel består i en fornuftig administration af elektrolytfrit vand, som vil reducere både natrium- og kloridkoncentrationerne.
Orsager til hyperchloræmi.
Pseudohyperchloræmi
Høje mængder serumfedtstoffer (lipider eller proteiner) ved analyser, der involverer prøvefortynding anvendes
Bromid- eller jodidforgiftning
Overdreven kloridadministration
Administration af store mængder af 0.9% (normal) natriumkloridopløsning
Givelse af hypertonisk saltvand
Saltvandsdrypning
Nettovandtab
Feber
Svedlugt
Utilstrækkeligt vand indtag (dårlig tørst eller adgang til vand)
Diabetes insipidus
Vandtab ved overdreven elektrolytter
Visse former for diarré
Osmotisk diurese
Visse tilfælde af postobstruktiv diurese
Associeret med metabolisk acidose
Visse former for diarré
Renal tubulær acidose
Kulsyreanhydrasehæmmere
Ureteral diversion (e.g., ilealblære)
Ammoniumkloridadministration
Arginin- eller lysinhydrochloridadministration
Visse tilfælde af kronisk nyresygdom
Organisk acidose, hvor syreanionerne udskilles hurtigt (f.eks, overdosis af toluen)
Respiratorisk alkalose
Hyperchloræmi som følge af overdreven kloridexposition
Hyperchloræmi kan forekomme, når kroppen udsættes for væsker med et højt kloridindhold. Et ekstremt eksempel herpå er saltvandsdrykning/ingestion af saltvand. Den pludselige store tilførsel af havvand (det gennemsnitlige saltindhold er 3,5 %) overvælder nyrernes evne til at udskille natriumkloridbelastningen, og hypernatriæmi og hyperchloræmi er almindelige.23 Ikke desto mindre kommer en del af den hypernatriæmi og hyperchloræmi, der er forbundet med overdreven saltvandsindtagelse, fra væsketab i forbindelse med diarré og urintab.23 Behandlingen af patienter med hyperchloræmi som følge af saltvandsdøning vil afhænge af patientens volumenstatus samt skøn over igangværende væske- og elektrolyttab og den fornuftige udskiftning af vand og elektrolytter efter behov.
Et mindre ekstremt eksempel på hyperchloræmi med en overdreven natriumchloridbelastning er indgift af store mængder isotonisk (0,9 %) natriumchloridopløsning (normal saltvand), der ofte anvendes til volumenoplivning af patienter. Det er bemærkelsesværdigt, at når en normal person får en stor bolus af isotonisk saltvand, kan det tage op til 2 dage at vende tilbage til natrium- og kloridbalancen før behandlingen.24 Denne tilbageholdelse af klorid sker ved eksponering for de suprafysiologiske niveauer af klorid i normal saltvand. Den normale kloridkoncentration i plasma ligger i intervallet 95-110meq/L, mens normal saltvand har en kloridkoncentration på 154meq/L. Det forholdsvis langsomme udskillelsesrespons på isotonisk saltvand kan være relateret til virkningerne af kloridbelastningen på den renale blodgennemstrømning og på den glomerulære filtration (tubuloglomerulær feedback). Selv om nedregulering af chloridreabsorberende transporteraktiviteter forekommer ved natriumchloridbelastning,14,25,26 er hastigheden af reduktionen af disse transportører ikke veldefineret.
Med isotonisk saltvandsindgift kan bikarbonatkoncentrationen også falde i takt med, at chloridkoncentrationen stiger. Ud over fortynding af plasmabicarbonat ved administration af suprafysiologiske kloridholdige, basefri opløsninger som f.eks. normal saltvand kan andre faktorer spille en rolle i faldet i bikarbonat- og stigningen i kloridniveauet. Urinbicarbonattab kan bidrage til faldet i serumbicarbonatniveauet, da der kan være en reduktion i den reabsorptive tærskel for bicarbonat ved volumenudvidelse.27 Dette tab af bicarbonat kan forekomme, selv når serumbicarbonatkoncentrationen er lav.27 I undersøgelser på mennesker er tabet af natrium og kalium i løbet af de første 24 timer efter at der er givet en infusion af isotonisk saltvand større end tabet af chlorid i løbet af de første 24 timer efter at der er givet en infusion af isotonisk saltvand. Den reducerede udskillelse af klorid i forhold til natrium og kalium tyder på urintab af andre anioner som f.eks. bikarbonat og andre organiske anioner, der også kan bidrage til et fald i serumbikarbonatkoncentrationen.24 Anvendelse af afbalancerede elektrolytopløsninger, der indeholder base eller baseækvivalenter og kloridkoncentrationer, der er mere fysiologiske, kan ikke blot forhindre udvikling af hyperchloræmisk acidose, men kan også undgå nogle af de mulige skadelige virkninger, der er forbundet med hyperchloræmiske opløsninger som f.eks. normal saltvand.28,29 I sammenligning med afbalancerede, baseholdige saltopløsninger resulterede administration af normal saltvand til raske mennesker i et fald i renal blodgennemstrømning og kortikal perfusion30 , hvilket giver anledning til bekymring om overdreven administration af normal saltvand i forbindelse med volumenoplivning hos patienter. Ikke desto mindre kan visse kliniske situationer begunstige brugen af normal saltvand, herunder hos patienter med hypokloræmisk metabolisk alkalose eller patienter med cerebralt ødem.
Hyperchloræmi med metabolisk acidose
Hyperchloræmi opstår også, når der tilsættes saltsyre (HCl) til blodet. HCl gives sjældent som et direkte surhedsfremmende middel, men kan dannes fra metabolismen af ammoniumchlorid eller kationiske aminosyrer som lysin og argininin31 . Generering af HCl fører til reaktion af H+ med HCO3-, der resulterer i CO2-produktion og et nettotab af HCO3- og stigning i kloridkoncentrationen.
Med respirationen tabes titreret bicarbonat fra kroppen som CO2.
Så for hvert milliekvivalent HCl, der tilsættes, forbruges et milliekvivalent bikarbonat og omdannes til CO2, således at kloridniveauet stiger i samme omfang, som bikarbonatniveauet falder.
Renale tubulære acidoser (proximal type 2 RTA og distal type 1 eller 4 RTA) resulterer i hyperchloræmisk metabolisk acidose. Ved proximal RTA (type 2) er bikarbonatreabsorptionen i den proximale tubulus nedsat, hvilket resulterer i øget tab af bikarbonat ud af dette segment. Der er også en vis forstyrrelse af chloridreabsorptionen, fordi den manglende ekstraktion af bicarbonat forhindrer den normale stigning i den luminale chloridkoncentration. I proximal RTA er reduktionen i bikarbonattransporten dog større end reduktionen i kloridtransporten, således at der reabsorberes relativt mere klorid end bikarbonat. Hvis kulsyreanhydrasehæmning anvendes som model for proximal RTA, synes kloridreabsorptionen at være mindre nedsat end bikarbonatreabsorptionen, hvilket afspejles af en relativt beskeden stigning i kloridudskillelseshastigheden i urinen, mens udskillelseshastigheden af natrium, kalium og formodentlig bikarbonat er markant forøget32 .
I klassisk distal RTA (type 1) eller type 4 RTA forhindrer reduktionen i nettosyresekretion den renale dannelse af nyt bikarbonat ved at forringe ammonium- og/eller titrerbar syreudskillelse. Som følge heraf resulterer det HCl, der dannes ved metabolisme, i et fald i bikarbonat, som ikke kompenseres af dannelsen og bevarelsen af bikarbonat og udskillelsen af klorid. Så længe nyrefunktionen er bevaret, ophobes der ikke-chloridsyreanioner ikke i det systemiske kredsløb, hvorved der opretholdes et relativt normalt aniongab. Faktisk stimuleres den renale udskillelse af fosfat- og sulfatanioner, der genereres fra metabolismen af fosfor- og svovlholdige aminosyrer31 , faktisk af acidose.33
En anden årsag til hyperchloræmisk metabolisk acidose forekommer ved diarré. I mange segmenter af mave-tarmkanalen og tilknyttede exokrine organer, såsom pancreas, udskilles bikarbonat i tarmen i bytte for klorid, således at tab af bikarbonat, især i sekretoriske former for diarré, kan være forbundet med bikarbonattab, som er forbundet med kloridretention34 .
Reparation af hyperchloræmiske former for metabolisk acidose indebærer, at man stopper den igangværende årsag til bikarbonattab eller HCl-generering, mens man giver patienten bikarbonat eller baseækvivalenter (f.eks. citrat) eller tillader patientens nyrer at regenerere bikarbonat, hvis nyrefunktionen er relativt normal. Under dannelsen af metabolisk acidose er der indledningsvis nettonatriumtab og volumenkontraktion. Ved mere langvarig acidose kan der forekomme natriumretention på grund af høje aldosteronniveauer og opregulering af ENaC i samleleddet.35 Ved tilførsel af bikarbonat til korrektion af acidosen tilbageholdes bikarbonat i den proximale tubulus, og den normale kloridreabsorption genetableres også. Den tilknyttede volumenreekspansion med bicarbonat kan bidrage til faldet i chlorid. Når nyrerne reparerer den metaboliske acidose, udskilles ammoniumklorid i urinen, mens bicarbonat, der dannes i den proximale tubulus som et biprodukt af glutaminmetabolismen, returneres til blodet.
Liste over nøglepunkter
-
Nyren spiller en central rolle i opretholdelsen af kloridbalancen i kroppen. Selv om renal kloridtransport er koblet med natriumtransport, kan kloridtransporten undertiden afvige fra natriumtransporten.
-
Hyperchloræmi kan skyldes en række forskellige tilstande, herunder vandmangel, overdreven klorideksponering og metabolisk acidose.
-
Den patogene årsag til hyperchloræmi vil give vejledning om, hvordan forstyrrelsen skal behandles: vanddepletion behandles med fornuftig vandtilførsel; overdreven kloridtilførsel ved at tilbageholde yderligere kloridtilførsel; og hyperchloræmisk metabolisk acidose ved at give bicarbonat.
Interessekonflikt
Forfatteren erklærer ingen interessekonflikter.