Generisk navn: meprobamat og aspirin
Doseringsform: tabletter
Medicinsk gennemgået af Drugs.com. Sidst opdateret den 22. dec. 2020.
- Overblik
- Bivirkninger
- Dosering
- Professionel
- Interaktioner
- Billeder
- Mere
Kode 1019A00
Rev. 09/06
Kun på recept
- Equagesic Beskrivelse
- Equagesic – Klinisk farmakologi
- Indikationer og anvendelse for Equagesic
- Kontraindikationer
- Advarsler
- Forsigtighedsregler
- Generelt
- Informationer til patienter
- Lægemiddelinteraktioner
- Laboratorieprøveinteraktioner
- Carcinogenese, Mutagenese Forringet fertilitet
- Graviditet: Teratogene virkninger. Graviditetskategori X.
- Laboration og fødsel
- Sygeplejersker
- Pædiatrisk brug
- Geriatrisk brug
- Bivirkninger
- Misbrug og afhængighed
- Overdosering
- Dosering og administration
- Sådan leveres
Equagesic Beskrivelse
På hver tablet Equagesic, til oral indgift, er der 200 mg meprobamat og 325 mg aspirin. Kemisk set er meprobamat 2-methyl-2-propyl-1,3- propanedioldicarbamat. Dets molekylformel er C9H18N2O4 med en molekylvægt på 218,25.
Cemisk set er aspirin benzoesyre 2-(acetyloxy)-. Dens molekylformel er C9H8O4 med en molekylvægt på 180,16. Det forekommer som et lugtfrit hvidt, nåleagtigt krystallinsk eller pulverformigt stof. Når aspirin udsættes for fugt, hydrolyseres det til salicylsyre og eddikesyre og afgiver en eddikeagtig lugt. Det er meget lipidopløseligt og let opløseligt i vand. Strukturformlerne for meprobamat og aspirin er:
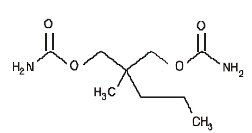
MEPROBAMAT
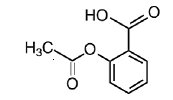
ASPIRIN
De tilstedeværende inaktive ingredienser er D&C Yellow 10, FD&C Red 3, FD&C Yellow 6, hydrogeneret vegetabilsk olie, magnesiumstearat, mikrokrystallinsk cellulose, polacrilinkalium og stivelse.
Equagesic – Klinisk farmakologi
Meprobamat er et carbamatderivat, som har vist sig (i dyre- og/eller humane undersøgelser) at have virkninger på flere steder i centralnervesystemet, herunder i thalamus og det limbiske system. Aspirin er et ikke-narkotisk analgetikum med febernedsættende og antiinflammatoriske egenskaber.
Indikationer og anvendelse for Equagesic
Som et supplement til kortvarig behandling af smerter ledsaget af spændinger og/eller angst hos patienter med muskuloskeletale sygdomme. Kliniske forsøg har vist, at smertelindringen i disse situationer er noget større end med aspirin alene. Equagesic er ikke beregnet til brug i mere end 10 dage.
Kontraindikationer
Anvendelse under graviditet og amning
En øget risiko for medfødte misdannelser i forbindelse med brug af mindre beroligende midler (meprobamat, chlordiazepoxid og diazepam) i første trimester af graviditeten er blevet antydet i flere undersøgelser. Da brugen af disse lægemidler sjældent er et akut problem, bør brugen af dem i denne periode næsten altid undgås.
På grund af den kendte virkning af ikke-steroide antiinflammatoriske lægemidler (NSAID’er) på fostrets hjerte-kar-system (lukning af ductus arteriosus) bør brugen i tredje trimester af graviditeten undgås. Salicylatprodukter er også blevet forbundet med ændringer i maternelle og neonatale hæmostase-mekanismer, nedsat fødselsvægt og perinatal mortalitet. Muligheden for, at en kvinde i fødedygtig alder kan være gravid på det tidspunkt, hvor behandlingen iværksættes, bør overvejes. Patienterne bør informeres om, at hvis de bliver gravide under behandlingen eller har til hensigt at blive gravide, bør de kommunikere med deres læge om det ønskelige i at afbryde medicinen. Meprobamat passerer placentabarrieren. Det er til stede både i navlestrengsblod i eller tæt på moderens plasmaniveauer og i modermælk fra ammende mødre i koncentrationer to til fire gange højere end moderens plasmaniveauer. Når man overvejer at anvende meprobamat til ammende patienter, skal man tage hensyn til lægemidlets højere koncentrationer i modermælk sammenlignet med moderens plasmaniveauer.
Equagesic er kontraindiceret hos patienter med akut intermitterende porfyri og hos patienter med allergiske eller idiosynkratiske reaktioner på aspirin, meprobamat eller beslægtede forbindelser, såsom carbromal, carisoprodol, mebutamat, ikke-steroide antiinflammatoriske lægemidler, salicylater eller tybamat. Equagesic er også kontraindiceret hos patienter med syndrom med astma, rhinitis og næsepolypper. Aspirinkomponenten i Equagesic kan forårsage alvorligt angioødem, bronkospasme (astma) eller urticaria. Reye’s syndrom: Aspirin bør ikke anvendes til børn eller teenagere ved virusinfektioner, med eller uden feber, på grund af risikoen for Reyes syndrom ved samtidig brug af aspirin ved visse virussygdomme.
Advarsler
Equagesic bør ordineres med forsigtighed og i små mængder til patienter med selvmordstendenser.
Tilsætningsstoffer: Aspirin bør anvendes med forsigtighed og i små mængder til patienter med selvmordstanker: Da CNS-dæmpende virkninger af meprobamat og alkohol eller meprobamat og andre psykofarmaka kan være additive, skal der udvises passende forsigtighed over for patienter, der tager mere end et af disse midler samtidig.
Advarsel om alkohol: Patienter, der indtager tre eller flere alkoholiske drikkevarer hver dag, bør rådgives om de blødningsrisici, der er forbundet med kronisk, kraftigt alkoholforbrug, mens de tager aspirin.
Koagulationsanomalier: Selv lave doser af aspirin kan hæmme trombocytfunktionen, hvilket fører til en forøgelse af blødningstiden. Dette kan have negativ indflydelse på patienter med arvelige (hæmofili) eller erhvervede (leversygdom eller vitamin K-mangel) blødningsforstyrrelser.
Gastrointestinale bivirkninger (GI): GI-bivirkninger omfatter grove GI-blødninger, halsbrand, kvalme, mavesmerter og opkastninger. Selv om mindre øvre GI-symptomer, såsom dyspepsi, er almindelige og kan forekomme når som helst under behandlingen, skal læger forblive opmærksomme på tegn på ulceration og blødning, selv i fravær af tidligere GI-symptomer. Lægerne bør informere patienterne om tegn og symptomer på GI-bivirkninger og om, hvilke skridt de skal tage, hvis de opstår.
Peptisk ulcersygdom: Patienter med en fortid med aktiv mavesårssygdom bør undgå at bruge aspirin, som kan forårsage irritation af maveslimhinden og blødning.
Potentielt farlige opgaver
Patienter skal advares om, at meprobamat kan nedsætte de mentale og/eller fysiske evner, der er nødvendige for udførelse af potentielt farlige opgaver, såsom at føre motorkøretøj eller betjene maskiner. Sådanne opgaver bør undgås, mens man tager dette produkt.
Forsigtighedsregler
Generelt
Equagesic bør ordineres med forsigtighed til visse særlige risikopopulationer, såsom ældre eller svækkede patienter og patienter med akutte abdominale tilstande, Addisons sygdom, koagulationsforstyrrelser, forhøjet intrakranielt tryk, hovedskader, hypothyroidisme, nedsat lever- eller nyrefunktion, prostatahypertrofi eller urethral striktur. Meprobamat metaboliseres i leveren og udskilles af nyrerne. For at undgå overdreven ophobning skal der udvises forsigtighed ved indgift til patienter med nedsat lever- eller nyrefunktion. Meprobamat kan lejlighedsvis fremskynde kramper hos epileptiske patienter.
Informationer til patienter
Patienterne skal informeres om, at Equagesic indeholder aspirin og ikke bør tages af patienter med aspirinallergi.
Patienter med disposition for gastrointestinale blødninger skal advares om, at samtidig brug af medicin, der indeholder aspirin og/eller alkohol, kan have en additiv virkning i denne henseende.
Lægemiddelinteraktioner
Angiotensin Converting Enzyme (ACE)-hæmmere: De hyponatremiske og hypotensive virkninger af ACE-hæmmere kan formindskes ved samtidig indgift af aspirin på grund af dets indirekte virkning på reninangiotensin-konverteringsvejen.
Acetazolamid: Samtidig brug af aspirin og acetazolamid kan føre til høje serumkoncentrationer af acetazolamid (og toksicitet) på grund af konkurrence ved nyretubuli om sekretion.
Alkohol, generelle anæstetika, narkotiske analgetika, beroligende hypnotika, beroligende midler som Chlordiazepoxid eller andre CNS-depressive midler: Virkningerne af disse stoffer kan forstærkes og forårsage øget CNS-depression.
Anticoagulerende behandling (Heparin og Warfarin): Patienter i antikoagulationsbehandling har øget risiko for blødning på grund af lægemiddel-interaktioner og virkningen på blodpladerne. Aspirin kan fortrænge warfarin fra proteinbindingssteder, hvilket fører til forlængelse af både protrombintiden og blødningstiden. Aspirin kan øge den antikoagulerende aktivitet af heparin, hvilket øger blødningsrisikoen.
Antikonvulsiva: Salicylater kan fortrænge proteinbundet phenytoin og valproinsyre, hvilket fører til et fald i den samlede koncentration af phenytoin og en stigning i serumvalproinsyrekoncentrationen.
Betablokkere: De hypotensive virkninger af betablokkere kan mindskes ved samtidig indgift af aspirin på grund af hæmning af renale prostaglandiner, hvilket fører til nedsat nyreblodgennemstrømning og salt- og væskeretention.
Cortikosteroider: Hos patienter, der samtidig modtager kortikosteroider og kronisk brug af medicin, der indeholder aspirin, kan ophør af kortikosteroider resultere i salicylisme, fordi kortikosteroider øger den renale clearance af salicylater, og deres ophør efterfølges af en tilbagevenden til normale renale clearancehastigheder.
Diuretika: Effekten af diuretika hos patienter med underliggende nyre- eller kardiovaskulær sygdom kan nedsættes ved samtidig indgift af aspirin på grund af hæmning af renale prostaglandiner, hvilket fører til nedsat renal blodgennemstrømning og salt- og væskeretention.
6-Mercaptopurin og methotrexat: Knoglemarvstoksicitet og bloddyskrasi kan skyldes, at disse lægemidler fortrænges fra sekundære bindingssteder og i tilfælde af methotrexat også reducerer dets udskillelse.
Nonsteroide antiinflammatoriske lægemidler (NSAID’er): Samtidig brug af aspirin med andre NSAID’er bør undgås, da dette kan øge blødningen eller føre til nedsat nyrefunktion.
Orale hypoglykæmiske midler: Moderate doser af aspirin kan øge effektiviteten af orale hypoglykæmiske lægemidler, hvilket kan føre til hypoglykæmi.
Uricosuriske midler (Probenicid og Sulfinpyrazon): Salicylater antagoniserer den uricosuriske virkning, hvilket reducerer deres effektivitet i behandlingen af gigt. Aspirin konkurrerer med disse midler om proteinbindingssteder.
Laboratorieprøveinteraktioner
Aspirin kan interferere med følgende laboratoriebestemmelser i blod: blodurinstofnitrogen, kolesterol, forhøjede leverenzymer, herunder aspartataminotransferase (AST), fastende blodglukose, hyperkaliæmi, forlænget blødningstid, protein, protrombintid, serumamylase, serumkreatinin og urinsyre. Aspirin kan interferere med følgende laboratoriebestemmelser i urin: 5-hydroxyindoleeddikesyre, diaeddikesyre, Gerhardt-keton, glukose, proteinuri, urinsyre, spektrofotometrisk påvisning af barbiturater og vanillylmandelinsyre (VMA).
Carcinogenese, Mutagenese Forringet fertilitet
Administration af aspirin i 68 uger ved 0,5 procent i foderet til rotter var ikke kræftfremkaldende. I Ames Salmonella-assayet var aspirin ikke mutagent; aspirin inducerede imidlertid kromosomaberrationer i dyrkede humane fibroblaster.
Graviditet: Teratogene virkninger. Graviditetskategori X.
Se Kontraindikationer
Laboration og fødsel
Aspirin bør undgås i tredje trimester af graviditeten og under fødsel, da det kan resultere i overdrevent blodtab ved fødslen. Der er rapporteret om forlænget gestation og forlænget fødsel på grund af prostaglandinhæmning.
Sygeplejersker
Sygeplejersker bør undgå at bruge aspirin, fordi salicylat udskilles i modermælken. Brug af høje doser kan føre til udslæt, trombocytanormaliteter og blødning hos ammende spædbørn. På grund af potentialet for alvorlige bivirkninger hos ammende spædbørn bør der træffes en beslutning om, hvorvidt amningen skal afbrydes eller om lægemidlet skal seponeres, under hensyntagen til lægemidlets betydning for moderen ( Se også Kontraindikationer).
Pædiatrisk brug
Sikkerheden og effektiviteten er ikke blevet fastlagt for pædiatriske patienter under 12 år (se Kontraindikationer).
Geriatrisk brug
Kliniske undersøgelser af meprobamat med aspirin omfattede ikke et tilstrækkeligt antal forsøgspersoner på 65 år og derover til at afgøre, om de reagerer anderledes end yngre forsøgspersoner. Generelt bør dosisvalg til en ældre patient være forsigtigt og normalt starte i den lave ende af doseringsområdet, hvilket afspejler den større hyppighed af nedsat lever-, nyre- eller hjertefunktion og af samtidige sygdomme eller anden lægemiddelbehandling.
Bivirkninger
Kroppen som helhed
Fever, hypotermi, tørst.
Allergiske eller idiosynkratiske
Sværere overfølsomhedsreaktioner, herunder anafylaksi, angioneurotisk ødem, anuri, astma, bronkospasme, bulløs dermatitis, kuldegysninger, erythema multiforme, eksfoliativ erythrodermi, larynxødem, oliguri, proctitis, purpura, Stevens-Johnsons syndrom, stomatitis og urticaria. Mindre reaktioner er karakteriseret ved et kløende, erytematøst makulopapuløst eller urticarielt udslæt, som kan være generaliseret eller begrænset til lysken. Andre reaktioner har omfattet akut ikke-trombocytopenisk purpura, adenopati, krydsoverfølsomhed mellem meprobamat/mebutamat og meprobamat/carbromal, ekchymoser, eosinofili, fixed-drug eruption med krydsreaktion på carisoprodol, leukopeni, perifere ødemer og petechiae.
Kardiovaskulær
Varierende former for arytmi, hypotension, palpitation, synkope, takykardi og forbigående EKG-ændringer.
Centralnervesystemet
Agitation, ataksi, cerebralt ødem, koma, forvirring, svimmelhed, døsighed, dysphori, eufori, hurtig EEG-aktivitet, hovedpine, nedsat synsakkommodation, lethargi, overstimulering, paradoksal ophidselse, paræstesier, sedation, sløret tale, subdural eller intrakraniel blødning, kramper, svimmelhed og svaghed.
Væske og elektrolytter
Dehydrering, hyperkaliæmi, metabolisk acidose og respiratorisk alkalose.
Gastrointestinale
Abdominalsmerter, obstipation, diarré, dyspepsi, epigastrisk ubehag, mavebesvær, gastrointestinal blødning, halsbrand, hepatitis, kvalme, pancreatitis, Reyes syndrom, forbigående forhøjelser af leverenzymer, ulceration og perforation og opkastninger.
Hæmatologisk (se også “Allergisk eller Idiosynkratisk”)
Agranulocytose og aplastisk anæmi er blevet rapporteret, selv om der ikke er blevet fastslået nogen årsagssammenhæng, koagulopati, dissemineret intravaskulær koagulation, forværring af porfyre-symptomer, hæmolytisk anæmi, jernmangelanæmi, okkult blodtab, forlængelse af protrombintiden, trombocytopeni og trombocytopenisk purpura.
Muskuloskeletalt
Rhabdomyolyse
Metabolisme
Hyperglykæmi og hypoglykæmi
Reproduktivt
Langvarig graviditet og fødsel, dødfødsler, spædbørn med lavere fødselsvægt samt blødninger før og efter fødslen.
Respiratorisk
Akut luftvejsobstruktion, hyperpnø, lungeødem og tachypnø.
Specielle sanser
Høretab og tinnitus.
Urogenitalt
Interstitiel nefritis, papillær nekrose, proteinuri og nyreinsufficiens og nyresvigt.
Misbrug og afhængighed
Fysisk afhængighed, psykologisk afhængighed og misbrug er forekommet. Kronisk forgiftning efter langvarig indtagelse af, sædvanligvis, større doser end anbefalet, viser sig ved ataksi, sløret tale og svimmelhed. Derfor tilrådes omhyggeligt tilsyn med dosis og ordinerede mængder samt undgåelse af langvarig indtagelse, især til alkoholikere og andre patienter med en kendt tilbøjelighed til at indtage for store mængder medicin. Pludselig tilbagetrækning af lægemidlet efter længerevarende og overdreven brug kan fremskynde tilbagefald af allerede eksisterende symptomer, såsom anoreksi, angst eller søvnløshed, eller abstinensreaktioner, såsom ataksi, forvirringstilstande, hallucinationer, muskeltrækninger, rysten, opkastninger og sjældent krampeanfald. Sådanne krampeanfald er mere sandsynlige at forekomme hos personer med skader på centralnervesystemet eller præeksisterende eller latente krampetilstande. Begyndelse af abstinenssymptomer forekommer normalt inden for 12 til 48 timer efter ophør med meprobamat; symptomerne ophører normalt inden for den næste 12 til 48 timers periode. Når overdreven dosering har stået på i uger eller måneder, bør dosis reduceres gradvist over en periode på 1 til 2 uger i stedet for pludseligt at blive stoppet. Alternativt kan et langtidsvirkende barbiturat erstattes og derefter gradvist trækkes tilbage.
Overdosering
Behandlingen af overdosering med Equagesic er i det væsentlige symptomatisk og støttende. I tilfælde, hvor der er blevet indtaget for store doser Equagesic, indtræder der hurtigt søvn, og blodtryk, puls og respirationsfrekvens reduceres til basalniveau. Eventuelt tilbageværende lægemiddel i maven skal fjernes, og der skal gives symptomatisk behandling. Efter emesis og/eller skylning kan aktivt kul reducere absorptionen af både aspirin og meprobamat. Hvis åndedrættet eller blodtrykket bliver svækket, skal respiratorisk assistance, stimulanser til centralnervesystemet og pressormidler administreres med forsigtighed som angivet. Diurese, osmotisk (mannitol) diurese, peritonealdialyse og hæmodialyse er blevet anvendt med succes til fjernelse af både aspirin og meprobamat. Alkalinisering af urinen øger udskillelsen af salicylater. Det er nødvendigt med omhyggelig overvågning af urinproduktionen, og man skal være forsigtig med at undgå overhydrering. Tilbagefald og død efter indledende bedring er blevet tilskrevet ufuldstændig gastrisk tømning og forsinket absorption. Salicylatforgiftning kan skyldes akut indtagelse (overdosis) eller kronisk forgiftning. Tegn og symptomer omfatter mavesmerter, syre-baseforstyrrelser med udvikling af metabolisk acidose, kramper, delirium, hyperpnø, hypertermi, hypoprothrombinæmi, rastløshed, Tinnitus (ringen i ørerne) og opkastninger. De tidlige tegn på salicylisk overdosis (salicylisme), herunder tinnitus, forekommer ved plasmakoncentrationer, der nærmer sig 200 μg/mL. Plasmakoncentrationer af aspirin på over 300 μg/mL er klart toksiske. Alvorlige toksiske virkninger er forbundet med koncentrationer over 400 μg/mL. En enkelt dødelig dosis aspirin hos voksne kendes ikke med sikkerhed, men døden kan forventes ved 30 g. Ved reel eller formodet overdosering skal der straks tages kontakt til et giftkontrolcenter. En omhyggelig medicinsk behandling er afgørende. Ved akut aspirinoverdosering kan der opstå alvorlige syre-base- og elektrolytforstyrrelser, som kompliceres af hypertermi og dehydrering. Respiratorisk alkalose opstår tidligt, mens hyperventilation er til stede, men efterfølges hurtigt af metabolisk acidose. Behandlingen af aspirinoverdosering består primært i at støtte vitale funktioner, øge salicylatudskillelsen og korrigere syre-baseforstyrrelsen. Gastrisk tømning og/eller skylning anbefales så hurtigt som muligt efter indtagelse, selv om patienten har kastet op spontant. Efter skylning og/eller emesis er det gavnligt at indgive aktivt kul i form af en opslæmning, hvis der er gået mindre end 3 timer siden indtagelsen. Der bør ikke anvendes kul adsorption før emesis og skylning.
Sværhedsgraden af aspirinforgiftning bestemmes ved at måle salicylatniveauet i blodet. Syre-base-status bør følges nøje med serielle blodgas- og serum-pH-målinger. Væske- og elektrolytbalancen bør også opretholdes. I alvorlige tilfælde er hypertermi og hypovolæmi de umiddelbare trusler mod livet. Børnene bør svampes med lunkent vand. Der bør gives erstatningsvæske intravenøst og suppleres med korrektion af acidose. Plasmaelektrolytter og pH-værdi bør overvåges for at fremme alkalisk diurese af salicylat, hvis nyrefunktionen er normal. Infusion af glukose kan være nødvendig for at kontrollere hypoglykæmi.
Hemodialyse og peritonealdialyse kan udføres for at reducere kroppens stofindhold. Hos patienter med nyreinsufficiens eller i tilfælde af livstruende forgiftning er dialyse normalt påkrævet. Udvekslingstransfusion kan være indiceret hos spædbørn og småbørn. Selvmordsforsøg med meprobamat har resulteret i ataksi, koma, døsighed, sløvhed, sløvhed, chok, stupor og respiratorisk og vasomotorisk kollaps. Nogle selvmordsforsøg har været fatale. Følgende data er blevet rapporteret i litteraturen og fra andre kilder. Disse data forventes ikke at korrelere med hvert enkelt tilfælde (under hensyntagen til faktorer som individuel modtagelighed og tidsrum fra indtagelse til behandling), men repræsenterer de sædvanlige rapporterede intervaller. Akut simpel overdosis (meprobamat alene): Der er rapporteret om død ved indtagelse af så lidt som 12 gram meprobamat og overlevelse ved indtagelse af så meget som 40 gram.
Blodniveauer
0,5 til 2 mg procent repræsenterer det sædvanlige blodniveauområde for meprobamat efter terapeutiske doser. 3 til 10 mg procent svarer normalt til fund af milde til moderate symptomer på overdosering, såsom stupor eller let koma. 10 til 20 mg procent svarer normalt til dybere koma, der kræver en mere intensiv behandling. Nogle dødsfald forekommer. Ved niveauer på over 20 mg procent kan der forventes flere dødsfald end overlevelser. Akut kombineret overdosis (meprobamat sammen med andre CNS-psykofarmaka eller alkohol): Da virkningerne kan være additive, kan en anamnese om indtagelse af en lav dosis meprobamat plus et af disse stoffer (eller et relativt lavt blod- eller vævsspejl) ikke anvendes som prognostisk indikator.
Dosering og administration
Den sædvanlige dosis af Equagesic er en eller to tabletter, hver tablet indeholder meprobamat, 200 mg, og aspirin, 325 mg, oralt 3 til 4 gange dagligt efter behov til lindring af smerter ved spændinger eller ængstelse. Equagesic anbefales ikke til patienter på 12 år og derunder.
Sådan leveres
Equagesic® (meprobamat- og aspirintabletter) Tabletter, 200 mg meprobamat og 325 mg aspirin, fås som følger: NDC 10551-091-10, lyserød og gul, dobbeltlaget, rund, rillet tablet mærket “LP” og “91”, i flasker med 100 tabletter.
Lagres ved kontrolleret rumtemperatur, 20°-25°C (68°-77°F).
Beskyttes mod fugt.
Holdes tæt lukket.
Beskyttes mod lys.
Dispensér i lysbestandig, tæt beholder.
Fremstillet for:
Leitner Pharmaceuticals™, LLC
Bristol, TN 37620
www.leitnerpharma.com
Fremstillet af:
Mikart, Inc.
Atlanta, GA 30318
1019A00
| Equagesic meprobamat og aspirin tablet |
||||||||||||
|
||||||||||||
| Virksomt indholdsstof/virksomt stof | ||
| Ingrediens navn | Styrkebasis | Styrke |
| meprobamat (meprobamat) | meprobamat | 200 mg |
| aspirin (aspirin) | aspirin | 325 mg |
| Inaktive bestanddele | ||
| Ingrediens navn | Styrke | |
| D&C Gul 10 | ||
| FD&C Rød 3 | ||
| FD&C Gul 6 | ||
| hydreret vegetabilsk olie | ||
| magnesiumstearat | ||
| mikrokrystallinsk cellulose | ||
| polacrilin-kalium | ||
| stivelse | ||
| Produktegenskaber | ||||
| Farve | GUL, PINK | Score | 2 stykker | |
| Form | RUND | Størrelse | 11mm | |
| Smag | Drykkode | LP;91 | ||
| Indeholder | ||||
| Beklædning | falsk | Symbol | falsk | |
| Pakning | |||
| # | Artikelkode | Pakkebeskrivelse | |
| 1 | NDC:10551-091-10 | 100 TABLET (100 TABLET) i 1 FLASKE, PLASTIK | |
Etiketteringsmaskine – Mikart, Inc.