Venerinen nimi: loperamidihydrokloridi
Asennusmuoto: kapselit
Lääketieteellisesti tarkistanut Drugs.com. Viimeksi päivitetty 22. tammikuuta 2021.
- Yleiskatsaus
- Haittavaikutukset
- Adostus
- Profiili
- Vuorovaikutukset
- Lisätiedot
- Imodium Kuvaus
- Imodium – Kliininen farmakologia
- Imodiumin käyttöaiheet ja käyttö
- Vasta-aiheet
- Varoitukset
- Varotoimet
- Yleistä
- Tietoa potilaille
- Lääkeinteraktiot
- Karsinogeneesi, mutageenisuus, hedelmällisyyden heikentyminen
- Raskaus
- Raskausluokka C
- Imettävät äidit
- Pediatrinen käyttö
- Haittavaikutukset
- Tiedot kliinisistä tutkimuksista
- Kokemukset markkinoille tulon jälkeen
- Lääkkeiden väärinkäyttö ja riippuvuus
- Väärinkäyttö
- Riippuvuus
- Yliannostus
- Imodiumin annostus ja antotapa
- Akuutti ripuli
- Krooninen ripuli
- Lapset alle 2-vuotiaana
- Iäkkäät
- Munuaisten vajaatoiminta
- Maksan vajaatoiminta
- Miten Imodiumia annetaan
- Tiheästi kysytyt kysymykset
- Lisätietoa Imodiumista (loperamidi)
- Kuluttajan resurssit
- Professionaaliset resurssit
- Muut valmisteet
- Hoito-oppaat
Imodium Kuvaus
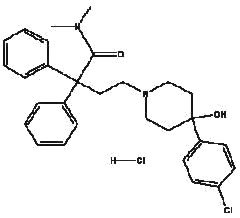
Imodium® (loperamidihydrokloridi), 4-(p-kloorifenyyli)-4-hydroksi-N,N-dimetyyli-a,a-difenyyli-1-piperidiinibutyramidimonohydrokloridi, on synteettinen ripulilääke suun kautta käytettäväksi.
Imodium® on saatavana 2 mg:n kapseleina.
Epäaktiiviset aineet ovat: Laktoosi, maissitärkkelys, talkki ja magnesiumstearaatti. Imodium®-kapselit sisältävät FD&C Yellow No. 6.
Imodium – Kliininen farmakologia
In vitro- ja eläinkokeet osoittavat, että Imodium® (loperamidihydrokloridi) vaikuttaa hidastamalla suolen motiliteettia ja vaikuttamalla veden ja elektrolyyttien liikkeisiin suolen läpi. Loperamidi sitoutuu opiaattireseptoriin suolen seinämässä. Näin ollen se estää asetyylikoliinin ja prostaglandiinien vapautumista, mikä vähentää peristaltiikkaa ja pidentää suolen läpimenoaikaa. Loperamidi lisää peräaukon sulkijalihaksen tonusta, mikä vähentää inkontinenssia ja kiireellisyyttä.
Miehellä Imodium® pidentää suolen sisällön läpimenoaikaa. Se vähentää päivittäistä ulostemäärää, lisää viskositeettia ja irtotiheyttä sekä vähentää neste- ja elektrolyyttihäviötä. Sietokykyä ripulilääkkeelle ei ole havaittu. Kliiniset tutkimukset ovat osoittaneet, että loperamidin näennäinen eliminaation puoliintumisaika ihmisellä on 10,8 tuntia ja vaihteluväli on 9,1 – 14,4 tuntia. Muuttumattoman lääkeaineen pitoisuudet plasmassa pysyvät alle 2 nanogramman millilitrassa 2 mg:n Imodium®-kapselin ottamisen jälkeen. Plasman pitoisuudet ovat korkeimmillaan noin viisi tuntia kapselin ottamisen jälkeen ja 2,5 tuntia nesteen ottamisen jälkeen. Loperamidin huippupitoisuudet plasmassa olivat samanlaiset molemmilla valmisteilla. Loperamidin poistuminen tapahtuu pääasiassa oksidatiivisen N-demetylaation kautta. Sytokromi P450 (CYP450) -isoentsyymeillä, CYP2C8 ja CYP3A4, uskotaan olevan tärkeä rooli loperamidin N-demetyloitumisprosessissa, koska kversetiini (CYP2C8:n estäjä) ja ketokonatsoli (CYP3A4:n estäjä) estivät N-demetyloitumisprosessia in vitro merkittävästi 40 %:lla ja 90 %:lla. Lisäksi CYP2B6:lla ja CYP2D6:lla näyttää olevan vähäinen rooli loperamidin N-demetylaatiossa. Muuttumattoman loperamidin ja sen metaboliittien erittyminen tapahtuu pääasiassa ulosteen kautta. Niillä potilailla, joilla biokemiallisia ja hematologisia parametreja seurattiin kliinisten tutkimusten aikana, Imodium®-hoidon aikana ei havaittu poikkeavuustrendejä. Samoin virtsakokeissa, EKG:ssä ja kliinisissä silmätutkimuksissa ei havaittu poikkeavuuden suuntauksia.
Imodiumin käyttöaiheet ja käyttö
Imodium® (loperamidihydrokloridi) on tarkoitettu akuutin epäspesifisen ripulin ja tulehdukselliseen suolistosairauteen liittyvän kroonisen ripulin hallintaan ja oireiden lievittämiseen. Imodium® on myös tarkoitettu vähentämään ileostomioista tulevan eritteen määrää.
Vasta-aiheet
Imodium on vasta-aiheinen potilaille, joilla on tunnettu yliherkkyys loperamidihydrokloridille tai jollekin apuaineelle.
Imodium on vasta-aiheinen potilaille, joilla on vatsakipua ilman ripulia.
Imodiumia ei suositella alle 24 kuukauden ikäisille imeväisille.
Imodiumia ei tule käyttää ensisijaisena hoitona:
– potilailla, joilla on akuutti punatauti, jolle on ominaista veri ulosteessa ja korkea kuume, – potilailla, joilla on akuutti haavainen paksusuolen tulehdus, – potilailla, joilla on invasiivisten organismien, kuten salmonellan, shigellan ja kampylobakteerin, aiheuttama bakteeriperäinen suolistotulehdus, – potilailla, joilla on leveävaikutteisten antibioottien käytön yhteydessä esiintyvä pseudokalvoperäinen koliitti.
Varoitukset
Neste- ja elektrolyyttivajetta esiintyy usein potilailla, joilla on ripuli. Tällaisissa tapauksissa asianmukaisen nesteen ja elektrolyyttien antaminen on erittäin tärkeää. Imodium®:n käyttö ei sulje pois asianmukaisen neste- ja elektrolyyttihoidon tarvetta.
Yleisesti Imodiumia ei pidä käyttää silloin, kun halutaan välttää peristaltiikan estämistä merkittävien seurausoireiden, kuten ileuksen, megakoolonin ja toksisen megakoolonin, mahdollisen riskin vuoksi. Imodium on lopetettava välittömästi, kun ummetus, vatsan turvotus tai ileus kehittyy.
Ripulin hoito Imodiumilla on vain oireenmukaista. Aina kun taustalla oleva etiologia voidaan määrittää, on annettava spesifistä hoitoa, kun se on asianmukaista (tai kun se on indikoitu).
Imodiumilla ripulin vuoksi hoidettujen AIDS-potilaiden hoito on lopetettava aikaisimpien vatsan turvotuksen merkkien ilmaantuessa. Loperamidihydrokloridilla hoidetuilla AIDS-potilailla, joilla on ollut sekä virus- että bakteeripatogeeneista johtuva infektiivinen paksusuolen tulehdus, on ollut yksittäisiä raportteja myrkyllisestä megakoolonista.
Imodium®-valmistetta on käytettävä erityistä varovaisuutta noudattaen pienille lapsille, koska vaste vaihtelee enemmän tässä ikäryhmässä. Dehydraatio, erityisesti nuoremmilla lapsilla, voi edelleen vaikuttaa Imodium®-vasteen vaihteluun.
Varotoimet
Yleistä
Erittäin harvinaisia allergisia reaktioita, mukaan lukien anafylaksia ja anafylaktinen sokki, on raportoitu. Akuutissa ripulissa, jos kliinistä paranemista ei havaita 48 tunnin kuluessa, Imodium®:n (loperamidihydrokloridi) anto on lopetettava ja potilaita on kehotettava ottamaan yhteyttä lääkäriin. Vaikka farmakokineettisiä tietoja maksan vajaatoimintaa sairastavista potilaista ei ole saatavilla, Imodiumia on käytettävä varoen tällaisille potilaille heikentyneen ensiaineenvaihdunnan vuoksi. Potilaita, joilla on maksan toimintahäiriö, on seurattava tarkasti CNS-toksisuuden merkkien varalta. Farmakokineettisiä tietoja ei ole saatavilla potilailla, joilla on munuaisten vajaatoiminta. Koska on raportoitu, että suurin osa lääkeaineesta metaboloituu ja metaboliitit tai muuttumaton lääkeaine erittyy pääasiassa ulosteisiin, annoksen säätäminen munuaisten vajaatoimintaa sairastavilla potilailla ei ole tarpeen. Virallisia tutkimuksia loperamidin farmakokinetiikan arvioimiseksi iäkkäillä henkilöillä ei ole tehty. Kahdessa tutkimuksessa, joihin osallistui iäkkäitä potilaita, ei kuitenkaan havaittu merkittäviä eroja lääkkeen dispositiossa iäkkäillä potilailla, joilla oli ripuli, verrattuna nuoriin potilaisiin.
Tietoa potilaille
Potilaita on kehotettava ottamaan yhteyttä lääkäriin, jos ripuli ei parane 48 tunnissa tai jos he huomaavat verta ulosteessa, heille nousee kuumetta tai heille kehittyy vatsan turvotus. Väsymystä, huimausta tai uneliaisuutta voi esiintyä Imodiumilla hoidettujen ripulioireyhtymien yhteydessä. Siksi on syytä noudattaa varovaisuutta autoa ajettaessa tai koneita käytettäessä. (ks. Haittavaikutukset).
Lääkeinteraktiot
Nonkliiniset tiedot ovat osoittaneet, että loperamidi on P-glykoproteiinisubstraatti. Loperamidin (16 mg:n kerta-annos) ja 600 mg:n kerta-annoksen samanaikainen anto joko kinidiinin tai ritonaviirin, jotka molemmat ovat P-glykoproteiinin estäjiä, kanssa johti loperamidin plasmapitoisuuksien 2- 3-kertaiseen nousuun. Koska keskushermostovaikutukset voivat voimistua, kun loperamidia annetaan samanaikaisesti kinidiinin ja ritonaviirin kanssa, on noudatettava varovaisuutta, kun loperamidia annetaan suositelluilla annoksilla (2 mg, enintään 16 mg:n enimmäisvuorokausiannos) P-glykoproteiinin estäjien kanssa.
Kun 16 mg:n kerta-annos loperamidia annettiin samanaikaisesti 600 mg:n kerta-annoksen sakinaviirin kanssa, loperamidi vähensi sakinaviirialtistusta 54 %, millä voi olla kliinistä merkitystä sakinaviirin terapeuttisen tehon vähenemisen vuoksi. Sakinaviirin vaikutus loperamidiin on vähemmän kliinisesti merkittävä. Siksi kun loperamidia annetaan yhdessä sakinaviirin kanssa, sakinaviirin terapeuttista tehoa on seurattava tarkoin.
Karsinogeneesi, mutageenisuus, hedelmällisyyden heikentyminen
188 kuukautta kestäneessä rotilla tehdyssä tutkimuksessa, jossa oraaliset annokset olivat enintään 40 mg/kg/vrk (21-kertainen ihmisen enimmäisannos 16 mg/vrk kehon pinta-ala-vertailun perusteella), ei ollut viitteitä karsinogeneesistä.
Loperamidi ei ollut genotoksinen Amesin testissä, SOS-kromotestissä E. coli -bakteerissa, dominoivassa tappotestissä naarashiirillä tai hiiren alkion solujen transformaatiomäärityksessä.
Fertiliteettiä ja lisääntymiskykyä arvioitiin rotilla käyttäen oraalisia annoksia 2,5, 10 ja 40 mg/kg/vrk (vain naaraat) toisessa tutkimuksessa. Suun kautta annetut annokset 20 mg/kg/vrk (noin 11-kertainen ihmisannos kehon pinta-alavertailun perusteella) ja suuremmat annokset aiheuttivat naaraiden hedelmällisyyden voimakasta heikkenemistä. Naarasrotille suun kautta annetulla enintään 10 mg/kg/vrk:n annoksella (noin 5-kertainen ihmisannokseen verrattuna kehon pinta-alan vertailun perusteella) ei ollut vaikutusta hedelmällisyyteen. Hoito urosrotilla 40 mg/kg/vrk suun kautta (noin 21 kertaa ihmisannos kehon pinta-alan vertailun perusteella) aiheutti urosten hedelmällisyyden heikkenemistä, kun taas enintään 10 mg/kg/vrk (noin 5 kertaa ihmisannos kehon pinta-alan vertailun perusteella) antamisella ei ollut vaikutusta.
Raskaus
Teratogeeniset vaikutukset
Raskausluokka C
Teratologisia tutkimuksia on tehty rotilla käyttäen oraalisia annoksia 2,5, 10 ja 40 mg/kg/vrk ja kaneilla käyttäen oraalisia annoksia 5, 20 ja 40 mg/kg/vrk. Näissä tutkimuksissa ei ole ilmennyt viitteitä hedelmällisyyden heikkenemisestä tai sikiölle aiheutuneista haitoista annoksilla, jotka olivat rotilla enintään 10 mg/kg/vrk (5 kertaa ihmisen annos kehon pinta-alan vertailun perusteella) ja kaneilla 40 mg/kg/vrk (43 kertaa ihmisen annos kehon pinta-alan vertailun perusteella). Rotille suun kautta annettu 40 mg/kg/vrk (21-kertainen ihmisannos kehon pinta-alavertailuun perustuvaan ihmisannokseen verrattuna) aiheutti merkittävää hedelmällisyyden heikkenemistä. Tutkimukset eivät tuottaneet näyttöä teratogeenisesta vaikutuksesta. Riittäviä ja hyvin kontrolloituja tutkimuksia raskaana olevilla naisilla ei ole. Loperamidia tulee käyttää raskauden aikana vain, jos mahdollinen hyöty oikeuttaa sikiölle mahdollisesti aiheutuvan riskin.
Ei-teratogeeniset vaikutukset
Rotilla tehdyssä peri- ja postnataalisessa lisääntymistutkimuksessa 40 mg/kg/vrk suun kautta annettu annos aiheutti jälkeläisten kasvun ja eloonjäämisen heikkenemistä.
Imettävät äidit
Pieniä määriä loperamidia saattaa esiintyä ihmisen rintamaidossa. Siksi Imodiumia ei suositella imetyksen aikana.
Pediatrinen käyttö
Katso kohta ”Varoitukset” saadaksesi tietoa vasteen suuremmasta vaihtelusta tässä ikäryhmässä. Jos lapset ottavat Imodium®-valmistetta vahingossa yliannostuksen, katso hoitosuositukset kohdasta ”Yliannostus”.
Haittavaikutukset
Tiedot kliinisistä tutkimuksista
Imodium®-valmisteen (loperamidihydrokloridi) kliinisten tutkimusten aikana raportoituja haittavaikutuksia on vaikea erottaa ripulioireyhtymään liittyvistä oireista. Imodium®:lla tehtyjen kliinisten tutkimusten aikana kirjatut haittavaikutukset olivat yleensä luonteeltaan vähäisiä ja itsestään rajoittuvia. Niitä havaittiin yleisemmin kroonisen ripulin hoidon aikana.
Raportoiduista haittatapahtumista on tehty yhteenveto riippumatta tutkijoiden kausaliteettiarviosta.
1) Haittavaikutukset neljästä lumelääkekontrolloidusta tutkimuksesta akuuttia ripulia sairastavilla potilailla
Haittatapahtumat, joiden ilmaantuvuus oli 1.0 % tai enemmän, joita raportoitiin vähintään yhtä usein loperamidihydrokloridia saaneilla potilailla kuin lumelääkettä saaneilla, on esitetty alla olevassa taulukossa.
| Akuutti ripuli | |||
|---|---|---|---|
| Loperamidihydrokloridi | Paikkalääke | ||
| Ei. 8 % | |||
Haittavaikutukset, joiden esiintyvyys oli 1,0 % tai suurempi ja joita raportoitiin useammin lumelääkettä kuin loperamidihydrokloridia saaneilla potilailla, olivat: suun kuivuminen, ilmavaivat, vatsakrampit ja koliikki.
2) Haittavaikutukset kroonista ripulia sairastavilla potilailla tehdyistä 20 lumekontrolloidusta tutkimuksesta
Haittavaikutukset, joiden esiintyvyys oli 1,0 % tai suurempi ja joita raportoitiin vähintään yhtä usein loperamidihydrokloridia saaneilla potilailla kuin lumelääkettä saaneilla potilailla, on esitetty alla olevassa taulukossa.
| Krooninen ripuli | |||
|---|---|---|---|
| Loperamidihydrokloridi | Paikkalääke | ||
| Ei. 3 % | 0,0 % | ||
| Keskus- ja ääreishermosto AE% | |||
| Huimaus | 1,4 % | 0,7 % | |
Haittatapahtumat, joiden ilmaantuvuus oli 1.0 % tai enemmän, joita raportoitiin useammin lumelääkettä kuin loperamidihydrokloridia saaneilla potilailla, olivat: pahoinvointi, oksentelu, päänsärky, meteorismi, vatsakipu, vatsakrampit ja koliikki.
3) Haittavaikutukset seitsemästäkymmenestäkuusi kontrolloidusta ja kontrolloimattomasta tutkimuksesta, jotka koskivat potilaita, joilla oli akuutti tai krooninen ripuli,
Haittavaikutukset, joiden ilmaantuvuus oli 1.0 % tai enemmän potilailla kaikista tutkimuksista on esitetty alla olevassa taulukossa.
| Akuutti ripuli | Krooninen ripuli | Kaikki tutkimukset * | |||
|---|---|---|---|---|---|
| * Kaikkien tutkimusten kaikki potilaat, mukaan lukien ne tutkimukset, joissa ei ollut täsmennetty, ilmenivätkö haittatapahtumat potilailla, joilla oli akuutti vai krooninen ripuli. | |||||
| Nro. hoidetuista potilaista | 1913 | 1371 | 3740 | ||
| Gastrointestinaalinen AE% | |||||
| Nausea | 0,7 % | 3,2 % | 1.8 % | ||
| Suolikanavan ummetus | 1.6 % | 1.9 % | 1.7 % | ||
| Vatsakrampit | 0.5 % | 3,0 % | 1,4 % | ||
Kokemukset markkinoille tulon jälkeen
Seuraavia haittavaikutuksia on raportoitu:
Ihon ja ihonalaisen kudoksen häiriöt
Ihottuma, kutina, nokkosihottuma, angioödeema ja erittäin harvinaisissa tapauksissa bullomainen eruptio, mukaan lukien erythema multiforme, Stevens-Johnsonin oireyhtymää ja toksista epidermaalista nekrolyysiä on raportoitu Imodiumin käytön yhteydessä
Immuunijärjestelmän häiriöt
Imodiumin käytön yhteydessä on raportoitu yksittäisiä allergisia reaktioita ja joissakin tapauksissa vakavia yliherkkyysreaktioita, mukaan lukien anafylaktinen sokki ja anafylaktoidiset reaktiot.
Ruuansulatuskanavan häiriöt
Suun kuivuminen, vatsakipu, turvotus tai epämukavuus, pahoinvointi, oksentelu, ilmavaivat, dyspepsia, ummetus, paralyyttinen ileus, megakoolon, mukaan lukien toksinen megakoolon (ks. kohta Vasta-aiheet ja varoitukset).
Munuaisten ja virtsateiden toimintahäiriöt
Virtsaretentio
Hermoston toimintahäiriöt
Uneliaisuus, huimaus
Yleishäiriöt ja hallinnolliset sairaudet
Väsymys
Joukko loperamidin kliinisten tutkimusten ja markkinoille tulon jälkeisen kokemuksen aikana raportoiduista haittavaikutuksista on usein taustalla olevan ripulioireyhtymän oireita (vatsakivut/vatsavaivat, pahoinvointi, oksentelu, suun kuivuminen, väsymys, uneliaisuus, huimaus, ummetus ja ilmavaivat). Näitä oireita on usein vaikea erottaa ei-toivotuista lääkevaikutuksista.
Lääkkeiden väärinkäyttö ja riippuvuus
Väärinkäyttö
Erityisessä kliinisessä tutkimuksessa, joka suunniteltiin loperamidin väärinkäyttöpotentiaalin arvioimiseksi suurilla annoksilla, todettiin, että väärinkäyttöpotentiaali on erittäin pieni.
Riippuvuus
Morfiiniriippuvaisilla apinoilla tehdyt tutkimukset osoittivat, että loperamidihydrokloridi ihmisille suositeltuja annoksia suuremmilla annoksilla esti morfiinin vieroitusoireita. Ihmisillä naloksoni-haastepupillitesti, joka positiivisena osoittaa opiaatin kaltaisia vaikutuksia, suoritettuna yksittäisen suuren annoksen jälkeen tai Imodium®:n (loperamidihydrokloridi) yli kahden vuoden terapeuttisen käytön jälkeen, oli kuitenkin negatiivinen. Suun kautta annettu Imodium® (magnesiumstearaattiin formuloitu loperamidi) on sekä hyvin liukenematon että tunkeutuu huonosti keskushermostoon.
Yliannostus
Yliannostustapauksissa (mukaan lukien maksan toimintahäiriöstä johtuva suhteellinen yliannostus) voi esiintyä virtsanpidätyskykyä, paralyyttistä ileusta ja keskushermoston lamaa. Lapset saattavat olla herkempiä CNS-vaikutuksille kuin aikuiset. Kliiniset tutkimukset ovat osoittaneet, että välittömästi loperamidihydrokloridin nauttimisen jälkeen annosteltu aktiivihiilen liete voi vähentää systeemiseen verenkiertoon imeytyvän lääkkeen määrää jopa yhdeksänkertaisesti. Jos oksennusta esiintyy spontaanisti nielemisen jälkeen, 100 g aktiivihiiltä sisältävä liete on annettava suun kautta heti, kun nesteitä voidaan pidättää.
Jos oksennusta ei ole esiintynyt, on suoritettava mahahuuhtelu ja sen jälkeen annettava 100 g aktiivihiiltä sisältävää lietettä mahaletkun kautta. Yliannostustapauksessa potilaita on seurattava keskushermoston lamaantumisen merkkien varalta vähintään 24 tunnin ajan.
Jos yliannostuksen oireita ilmenee, vastalääkkeenä voidaan antaa naloksonia. Jos potilas reagoi naloksoniin, elintoimintoja on seurattava huolellisesti lääkkeen yliannostuksen oireiden uusiutumisen varalta vähintään 24 tunnin ajan viimeisen naloksoniannoksen jälkeen.
Loperamidin pitkäkestoisen vaikutuksen ja naloksonin lyhyen vaikutusajan (yhdestä kolmeen tuntiin) vuoksi potilasta on seurattava tarkoin ja hoidettava toistuvasti naloksonilla tarpeen mukaan. Koska lääkettä erittyy virtsaan suhteellisen vähän, pakotetun diureesin ei odoteta tehoavan Imodium®:n (loperamidihydrokloridi) yliannostukseen.
Kliinisissä tutkimuksissa aikuinen, joka otti kolme 20 mg:n annosta 24 tunnin aikana, pahoinvoi toisen annoksen jälkeen ja oksensi kolmannen annoksen jälkeen. Tutkimuksissa, joiden tarkoituksena oli tutkia mahdollisia haittavaikutuksia, enintään 60 mg loperamidihydrokloridin tahallinen nauttiminen kerta-annoksena terveille koehenkilöille ei johtanut merkittäviin haittavaikutuksiin.
Imodiumin annostus ja antotapa
(1 kapseli = 2 mg)
Potilaiden on saatava asianmukaista neste- ja elektrolyyttikorvaushoitoa tarpeen mukaan.
Akuutti ripuli
Aikuiset: Suositeltu aloitusannos on 4 mg (kaksi kapselia) ja sen jälkeen 2 mg (yksi kapseli) jokaisen muodostumattoman ulosteen jälkeen. Vuorokausiannos ei saa ylittää 16 mg (kahdeksan kapselia). Kliininen paraneminen havaitaan yleensä 48 tunnin kuluessa.
Lapset: 2-5-vuotiaille lapsille (enintään 20 kg) tulee käyttää reseptivapaata nestemäistä formulaatiota (Imodium® A-D 1 mg/7,5 ml). 6-12-vuotiaille voidaan käyttää joko Imodium®-kapseleita tai Imodium® A-D-nestettä. 2-12-vuotiaille lapsille seuraava kapseleiden tai nesteen annosteluaikataulu täyttää yleensä aloitusannostusvaatimukset:
Suositeltu ensimmäisen päivän annosteluaikataulu
Kahdesta viiteen vuotta: (3 mg vuorokausiannos) (13-20 kg)
Kuusi-kahdeksan vuotta: 2 mg b.i.d. (4 mg vuorokausiannos) (20-30 kg)
Kahdeksasta kahteentoista vuoteen: 2 mg t.i.d.. (6 mg:n vuorokausiannos) (yli 30 kg)
Suositeltu seuraava vuorokausiannos
Ensimmäisen hoitopäivän jälkeen suositellaan, että seuraavat Imodium®-annokset (1 mg/10 kg ruumiinpainoa) annetaan vasta löysän ulosteen jälkeen. Kokonaisvuorokausiannos ei saa ylittää ensimmäisen päivän suositeltuja annoksia.
Krooninen ripuli
Lapset: Vaikka Imodium® -valmistetta on tutkittu rajoitetulla määrällä kroonista ripulia sairastavia lapsia; terapeuttista annosta kroonisen ripulin hoitoon pediatrisessa väestössä ei ole vahvistettu.
Aikuiset: Suositeltu aloitusannos on 4 mg (kaksi kapselia), jonka jälkeen 2 mg (yksi kapseli) jokaisen epämuodostuneen ulosteen jälkeen, kunnes ripuli on hallinnassa, minkä jälkeen Imodium®-annosta on pienennettävä yksilöllisten tarpeiden mukaan. Kun optimaalinen vuorokausiannos on määritetty, tämä määrä voidaan sen jälkeen antaa kerta-annoksena tai jaettuina annoksina.
Keskimääräinen päivittäinen ylläpitoannos kliinisissä tutkimuksissa oli 4-8 mg (kahdesta neljään kapselia). Annos 16 mg (kahdeksan kapselia) ylittyi harvoin. Jos kliinistä paranemista ei havaita sen jälkeen, kun hoitoa on annettu 16 mg:lla päivässä vähintään 10 päivän ajan, oireet eivät todennäköisesti pysy kurissa jatkohoidolla. Imodium®-valmisteen antoa voidaan jatkaa, jos ripulia ei saada riittävästi hallintaan ruokavaliolla tai erityishoidolla.
Lapset alle 2-vuotiaana
Imodiumin käyttöä alle 2-vuotiaille lapsille ei suositella. On ollut harvinaisia raportteja paralyyttisestä ileuksesta, joka on liittynyt vatsan turvotukseen. Useimmat näistä raporteista esiintyivät akuutin punataudin, yliannostuksen yhteydessä ja hyvin pienillä, alle kaksivuotiailla lapsilla.
Iäkkäät
Iäkkäillä koehenkilöillä ei ole tehty virallisia farmakokineettisiä tutkimuksia. Iäkkäillä potilailla, joilla on ripuli, ei kuitenkaan raportoitu merkittäviä eroja lääkkeen dispositiossa suhteessa nuoriin potilaisiin. Annoksen säätäminen ei ole tarpeen iäkkäillä henkilöillä.
Munuaisten vajaatoiminta
Farmakokineettisiä tietoja ei ole saatavilla potilailla, joilla on munuaisten vajaatoiminta. Koska metaboliitit ja muuttumaton lääkeaine erittyvät pääasiassa ulosteeseen, munuaisten vajaatoimintaa sairastavilla potilailla ei tarvita annostuksen mukauttamista (ks. kohta KÄYTTÖOHJEET).
Maksan vajaatoiminta
Vaikka farmakokineettisiä tietoja ei ole saatavissa maksan vajaatoimintaa sairastavilla potilailla, Imodiumia on käytettävä varoen näillä potilailla vähentyneen ensiaineenvaihdunnan vuoksi. (ks. kohta Varotoimet).
Miten Imodiumia annetaan
Kapselit – kukin kapseli sisältää 2 mg loperamidihydrokloridia. Kapseleissa on vaaleanvihreä runko ja tummanvihreä korkki, jonka yhteen segmenttiin on painettu ”JANSSEN” ja toiseen segmenttiin ”Imodium”. Imodium®-kapselit toimitetaan 100 kapselin pulloissa.
NDC 50458-400-10
(100 KAPSELIA)
Säilytä 15°-25°C:ssa (59°-77°F).
Parannettu syyskuussa 1996, heinäkuussa 1998, huhtikuussa 2004
Hyväksytty lokakuussa 2005
©Janssen Pharmaceutica Inc. 1998
Rx Only
Printed in USA
U.S. Patentti 3, 714,159
| Imodium loperamidihydrokloridikapseli |
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
Etiketöintilaite -. McNeil Consumer Healthcare
Tiheästi kysytyt kysymykset
- Miten ripuli saadaan loppumaan – onko lääke- tai lääke-ehdotuksia?
Lisätietoa Imodiumista (loperamidi)
- Haittavaikutukset
- Raskauden tai imetyksen aikana
- Dositus Tietoa
- Lääkekuvat
- Lääkkeiden yhteisvaikutukset
- Vertaile vaihtoehtoja
- Tukiryhmä
- 24 arvostelua
- Lääkeryhmä:
- FDA varoitukset (2)
Kuluttajan resurssit
- Advanced Reading
Professionaaliset resurssit
- Reseptitiedot
- Loperamidi oraaliliuos (FDA)
Muut tuotemerkit Anti-Diarrheal, Up and Up ripulilääke liuos
Muut valmisteet
- Imodium A-D
Hoito-oppaat
- Ripuli, Akuutti
- Ripuli, krooninen
- Matkailijan ripuli
- Ripuli
Lääketieteellinen vastuuvapauslauseke