Obsah
- 1 Funkce
- 2 Mechanismus pro vlákno-.transfer inhibice actio
- 3 HIV a AIDS
- 4 Vliv struktury
- 5 Krystalizace PFV v intaktní struktuře
- 5.1 Krystalizační technika
- 5.2 Krystalografické a zpřesňující statistiky
- 6 Celková architektura & Součásti
- 6.1 Struktura
- 6.2 Interakce mezi integrázou a DNA
- 6.3 Aktivní místo
- 7 Inhibitory integrázy
- 7.1 Další zdroje
- 8 3D struktury retrovirální integrázy
Funkce
Retrovirální integráza je základní retrovirální enzym, který se váže na virovou DNA a vkládá ji do chromozomu hostitelské buňky. Do genomu hostitelské buňky vkládá reverzně přepsanou cDNA viru lidské imunodeficience typu 1 (HIV-1) za účelem zvýšení zdatnosti a virulence patogenu. Integráza je produkována třídou retrovirů (jako je HIV) a virus ji používá k začlenění svého genetického materiálu do DNA hostitelské buňky. Hostitelský buněčný mechanismus pak z inkorporovaného genetického materiálu produkuje mRNA a následně protein, čímž dochází k replikaci viru. Ačkoli bylo zkoumáno několik léků inhibujících integrázu, mechanismus odpovědný za účinek inhibice přenosu řetězce není dosud objasněn . Hare el al (2010) však stanovili strukturní složky retrovirální integrace. Další objasnění kompletní struktury retrovirové integrázy a její použití k regulaci funkčních a enzymatických aktivit by potenciálně mohlo výzkumníkům umožnit oddálit progresi retrovirových onemocnění. Studium integrace HIV-1 by navíc mohlo vést k nalezení nového slibného cíle a přispět k vytvoření farmakoforem pro antivirovou terapii.
Inhibitory integrázy HIV: Raltegravir, prodávaný pod názvem Isentress, je v současné době schválen jako terapeutický inhibitor HIV integrázy. Byl schválen 12. října 2007. fágová integráza viz Fágová integráza.
Mechanismus inhibice řetězce actio
Caption
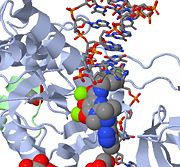
Nahoře je obrázek JMOL MK-0518 blokující 3′ konec virové DNA od vazby na aktivní místo. Všimněte si kovových chelatačních atomů kyslíku v MK-0518, které interagují s hořečnatými kationty nacházejícími se v aktivním místě.
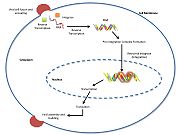
HIV integráza typu 1 je relativně novým a neotřelým cílem pro inhibitory. V roce 2007 byl FDA schválen první inhibitor HIV-1 integrázy, Raltegravir, pro použití u HIV-1 jako kombinovaná terapie . Inhibitory přenosu řetězce fungují tak, že zabraňují koordinované integraci virové DNA do hostitelského chromozomu. Po vstupu viru do hostitelské buňky přeměňuje reverzní transkriptáza virovou ssRNA na dsDNA. V tomto okamžiku integráza vytvoří komplex s virovou DNA a vytvoří předintegrační komplex (intasom). Preintegrační komplex je poté chaperonem dopraven do jádra, kde jsou z 3′ konce vyříznuty dva nukleotidy. Poté je DNA kovalentně integrována do hostitelské DNA. Inhibitory přenosu řetězce tento proces přeruší a zabrání integraci virové DNA do hostitelského chromozomu. Inhibitory přenosu řetězce fungují tak, že se zapojují do kofaktorů kovových iontů, které se nacházejí v aktivním místě retrovirální integrázy. Atomy kyslíku chelatující kovy, které se v inhibitorech nacházejí, interagují přímo s kovovými kofaktory, zatímco halobenzylová skupina zapadá do kapsy vytvořené přemístěnou 3′ virovou DNA v aktivním místě.
HIV a AIDS

V roce 2010 zemřelo na AIDS více než 25 milionů lidí a odhaduje se, že s HIV žije přibližně 33 milionů lidí.
K dnešnímu dni zemřelo na AIDS více než 25 milionů lidí a odhaduje se, že s HIV dnes žije přibližně 33 milionů lidí. Inhibitory retrovirální integrázy viz Raltegravir a Farmakokinetika inhibitorů retrovirální integrázy.
Vliv struktury
Třírozměrné struktury některých proteinů hostitelské buňky, které mají zásadní význam pro pochopení mechanismu infekce HIV a virulence, vznikly na základě rentgenových krystalografických analýz. Struktury HIV proteázy a integrázy patří mezi nejvýše hodnocené struktury, které přispěly k záchraně mnoha životů a přispěly ke kvalitě života mnoha jedinců postižených HIV. Uplatňují se při návrhu léků na základě struktury při vývoji inhibitorů proteázy a inhibitorů integrázy a používají se jako významná součást vysoce aktivní antiretrovirové terapie (HAART).
Ačkoli stávající antiretrovirové přípravky zlepšují kvalitu života a také prodlužují život mnoha pacientů, nedaří se jim nemoc vymýtit. Studie u inhibitorů integrázy ukazují, že kombinace s jinými antiretrovirovými léky snižuje adaptaci viru a může mít potenciál k využití pro záchrannou léčbu pacientů, kteří získali rezistenci na jiné léky. Více informací naleznete v části
- AIDS před inhibitory proteázy & Inhibitory HIV proteázy: Průlom
- Léčba: Farmakokinetika inhibitorů retrovirální integrázy Odkazy:
Krystalizace intasomu PFV
K napodobení konců virové DNA HIV-1 použili Hare et al (2010) rozpustné a plně funkční preparáty intasomu prototypu pěnového viru (PFV), získané pomocí rekombinantní integrázy PFV a dvouřetězcových oligonukleotidů.
Pozoruhodná stabilita komplexů integráza-DNA byla určena pozorováním reakcí přenosu vláken in vitro, které byly klasifikovány do tří způsobů deproteinační migrace: (1) jednotlivé sladěné události: linearizovaný cílový plazmid; (2) vícenásobné sladěné události: rozmazání; (3) události v polovině místa: otevřená kruhová DNA. Další charakterizace intasomu PFV rovněž prokázala strukturní podstatu, která naznačovala silné interakce protein-protein a protein-DNA navzdory dlouhodobé inkubaci v podmínkách vysoké iontové síly. Komplexní krystalizační testy vedly k vytvoření životaschopné krystalové konfigurace, která difraktovala rentgenové záření s rozlišením 2,9 Angstromu. Nakonec byla určena trojrozměrná struktura. Asymetrická jednotka obsahovala jeden dimer integrázy se stabilně vázanou molekulou virové DNA a dvojici dimerů integrázy spojených symetricky, které tvořily podlouhlý tetramer. Rozhraní dimerů je stabilizováno mezimolekulárními interakcemi amino terminálu a katalytického jádra domény (vnitřní podjednotka-venkovní podjednotka). Celkový tvar podlouhlého tetrameru je jedinečný, i když nese podobnosti s dříve popsanými komplexy HIV-1 integrázy.
Krystalizační technika
Komplexy protein-DNA byly vytvořeny za použití plné délky divokého typu PFV IN a syntetické dsDNA, která modelovala virový konec.
Intrasom byl krystalizován s využitím techniky visuté difúze s kapáním páry. Rezervoárový roztok se skládal z 1,35 M síranu amonného, 25 % (v/v) glycerolu, 4,8 % (v/v) 1,6-hexandiolu a 50 mM 2-(N-morfolin) kyseliny etansulfonové (MES) při pH 6,5. Roztok byl rozpuštěn v roztoku o koncentraci 1,35 M. Krystaly proteinu a DNA byly rovněž namočeny v přítomnosti MK0518, GS9137, Mg(II) a/nebo Mn(II). Krystalová struktura byla vyřešena pomocí molekulární náhrady.
Krystalografická a zpřesňující statistika
Hare et al (2010) publikovali údaje o sedmi krystalových strukturách. Tato data zahrnují komplex PFV IN (apo forma) a šest dalších struktur, včetně komplexu vázaného na Mg, Mn, Mg/MK0518, Mn/MK0518, Mg/GS9137 a Mn/GS9137. Všech sedm struktur patří do prostorové skupiny P41212. Byly zpřesněny na rozlišení mezi 2,85 a 3,25 Å.
Celková architektura & Komponenty
Struktura
Celková struktura sestaveného intasomu PFV je tetramerový model založený na dvou doménových strukturách s rozhraním dimer-dimer. Předchozí modely intasomu zobrazují podobnou, ale pružnější strukturu, zatímco intasom PFV se ukázal jako vysoce omezený. Pomocí homologického modelování Hare et al (2010) navrhují, že kratší interdoménové linkery mohou být faktorem flexibility, konkrétně u HIV-1 integrázy. Vnitřní podjednotky tetrameru se podílejí na celkové tetramerizaci a vazbě virové DNA. Katalytické domény jádra vnějších podjednotek mohou fungovat jako nosiče, ale vzhledem k tomu, že amino- a karboxy-terminální domény nejsou na mapách elektronové hustoty rozlišeny, jejich funkce zůstává neprůkazná. Doména katalytického jádra a linker karboxyterminální domény zaujímají po většinu své délky prodlouženou konformaci a jsou umístěny paralelně s aminoterminální doménou a linkerem domény katalytického jádra vnitřní podjednotky. Interdoménové linkery Interdoménové linkery (CCD-CTD linker a NTD-CCD linker) spojují obě poloviny intasomu dohromady a struktura je dále stabilizována dvojicí karboxyterminálních domén, které interagují s oběma vnitřními doménami katalytického jádra.
Interakce integrázy a DNA
Silné interakce protein-DNA se nacházejí v koncových šesti nukleotidech. Každá karboxyterminální doména interaguje s fosfodiesterovou páteří obou molekul virové DNA. Kromě toho amino-terminální doména-rozšíření a amino-terminální doména interagují s virovou DNA v aktivním místě protilehlé domény katalytického jádra.
Aktivní místo
Karboxyláty aktivního místa jsou postranní řetězce Asp 128, Asp 185, Glu 221.
V blízkosti aktivních míst se nachází po jednom atomu zinku.
- .
- .
Inhibitory integrázy
| Název | Značka | Společnost | Patent | Poznámky |
| Raltegravir | Isentress | Merck & Co. | – | známý také pod názvem MK-0518. Isopropyl a methyl-oxadiazol MK-0518 se účastní hydrofobních a stohovacích interakcí s postranními řetězci Pro 214 a Tyr 212, které stabilizují toto léčivo v aktivním místě intasomu PFV. Tento způsob vazebné interakce s léčivem způsobuje vytlačení reaktivního 3′ konce virové DNA z aktivního místa intasomu PFV. Po navázání přípravku MK-0518 do aktivního místa se reaktivní 3′ hydroxylová skupina vzdálí od aktivního místa intasomu PFV o více než 6 Angstromů. Raltegravir byl schválen FDA 12. října 2007 pro použití s dalšími anti-HIV látkami při léčbě HIV infekce u dospělých. Jedná se o první inhibitor integrázy schválený FDA. |
| Elvitegravir | – | Gilead Science | – | GS-9137 interaguje s Pro 214 intasomu PFV prostřednictvím své chinolonové báze a izopropylové skupiny. V experimentální fázi; sdílí základní strukturu chinolonových antibiotik. Byly dokončeny studie fáze II elvitegraviru u osob se zkušeností s léčbou. Studie fáze III u pacientů se zkušeností s léčbou probíhají. Probíhá studie fáze II elvitegraviru u osob, které nikdy neužívaly antiretrovirovou léčbu. V této studii bude rovněž hodnocena posilující látka namísto norviru, v současné době nazvaná GS9350. Elvitegravir je slibný pro HIV pozitivní pacienty, kteří v minulosti užívali jiné léky proti HIV. |
| MK-2048 | – | Merck & Co. | – | Inhibitor integrázy druhé generace, určený k použití proti infekci HIV. Je lepší než první dostupný inhibitor integrázy, raltegravir, protože inhibuje enzym HIV integrázu 4krát déle. Je zkoumán pro použití v rámci preexpoziční profylaxe (PrEP). |
Viz také Farmakokinetika inhibitoru retrovirové integrázy.
.