- Co dělá molekulu polární?
- Podívejte se na strukturní vzorec oxidu uhličitého:
- Proč je voda polární?
Voda je polární molekula, protože její kyslík je silně elektronegativní a jako takový přitahuje elektronový pár k sobě (od dvou atomů vodíku), čímž získává mírně záporný náboj.
Polarita molekuly závisí nejen na jejích jednotlivých atomech, ale také na tom, jak jsou uspořádány kolem centrálního atomu, tj. na prostorovém uspořádání těchto atomů. Abychom tomu lépe porozuměli, probereme toto téma podrobněji.
Co činí molekulu polární?
Polarita molekuly souvisí s posunem elektronů určitým směrem. To zase závisí na polaritě vazeb přítomných v molekule, protože tyto vazby také obsahují elektrony.
V molekule platí, že atom, který má větší schopnost přitahovat elektrony k sobě (tj, je elektronegativnější než druhý atom) na sebe získá mírně záporný náboj a vazba mezi oběma atomy se stane polární.
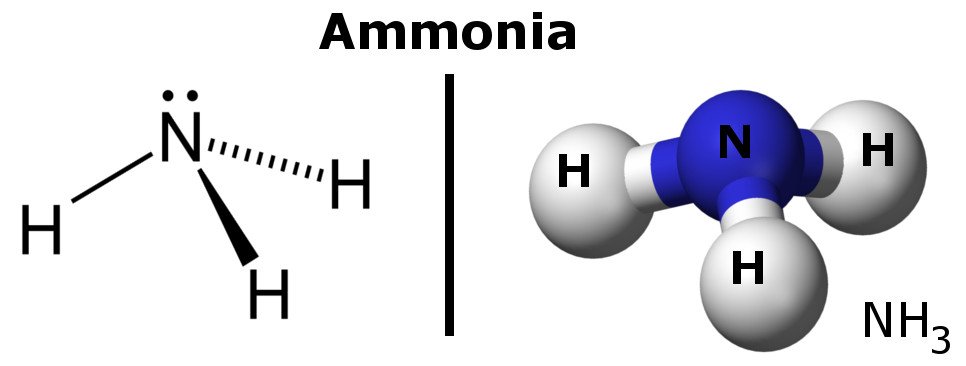
Amoniak je polární molekula, protože má oblasti mírně záporných a kladných nábojů.
Celkem by se dalo říci, že elektronová hustota polární vazby se hromadí směrem k jednomu konci vazby, což má za následek, že tento konec má mírně záporný náboj, zatímco druhý konec má mírně kladný náboj. Tím se molekula stává polární.
Podobně, pokud molekula nemá oblasti s kladným a záporným nábojem, je považována za nepolární.
Zajímavé však je, že čím větší je rozdíl elektronegativit, tím polárnější bude vazba v molekule. Karbonylové sloučeniny jsou polární, protože karbonylový uhlík je mírně kladný. Neměl by tedy oxid uhličitý, který obsahuje kladný uhlík a dva částečně záporné oxygeny, být polární?
No, oxid uhličitý se skládá ze dvou atomů kyslíku připojených k atomu uhlíku. Atomy kyslíku jsou mnohem elektronegativnější než atomy uhlíku, a proto by měly mít částečně záporný náboj, zatímco atom uhlíku by měl být mírně kladně nabitý. Je však zajímavé, že se tak neděje.
Podívejte se na strukturní vzorec oxidu uhličitého:
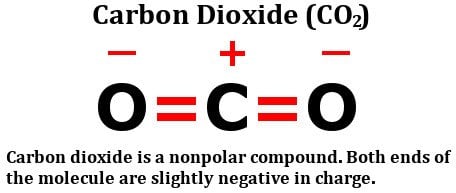
Skládá se ze dvou stejně elektronegativních atomů kyslíku, ano, ale podívejte se, jak jsou tyto atomy uspořádány kolem atomu uhlíku. Oba stojí v ideálním úhlu 180 stupňů od uhlíku. V důsledku toho odtahují elektronovou hustotu od uhlíku stejnou silou v opačných směrech. Výsledkem je, že elektronová hustota na atomu uhlíku zůstává neovlivněna, což činí molekulu oxidu uhličitého nepolární.
Dioxid uhličitý je skvělým příkladem toho, jak geometrie molekuly hraje zásadní roli při určování, zda je polární nebo nepolární. Nyní se podívejme na molekulu vody:
Proč je voda polární?
Chemický vzorec vody je H20, což znamená, že obsahuje dva atomy vodíku a jeden atom kyslíku. Atomy vodíku mají ve své slupce pouze jeden elektron, zatímco atom kyslíku má 6 valenčních elektronů.
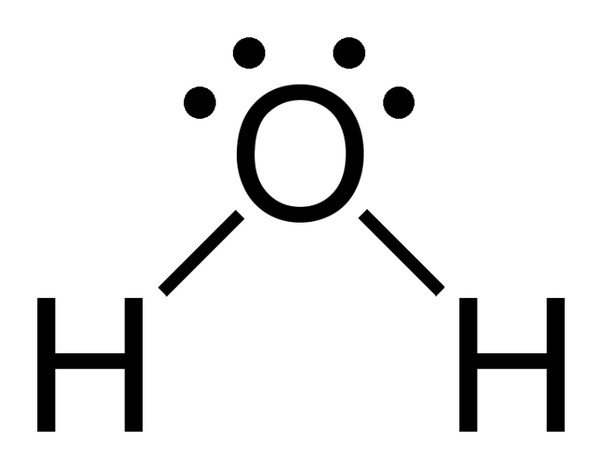
Všimněte si 2 osamělých párů elektronů na atomu kyslíku ve vodě.
Protože má kyslík ve své valenční slupce 6 elektronů, sdílí s každým atomem vodíku jeden elektron. Tímto způsobem mu zůstávají 4 nevázané elektrony v jeho 2 orbitalech. Tyto vazebné a nevazebné elektronové páry se kolem kyslíku uspořádají do tetraedrického tvaru, a proto se zdá, že obě vazby mají ohnutý tvar.
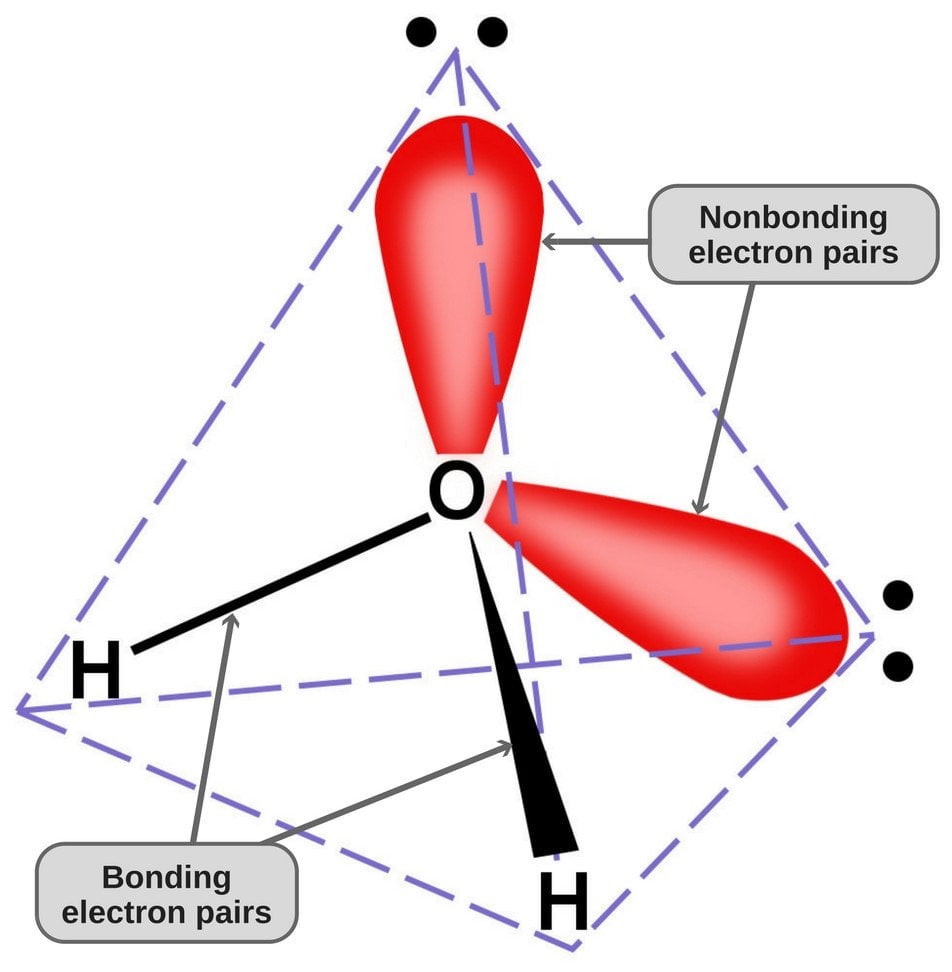
Tetraedrická geometrie molekuly vody.
Atomy kyslíku i vodíku mají různou elektronegativitu (hodnota elektronegativity vodíku je 2,1, zatímco elektronegativita kyslíku je 3,5), proto jsou obě vazby polární. Protože kyslík je elektronegativnější než vodík, přesouvá se elektronová hustota v obou těchto vazbách směrem ke kyslíku, čímž se oblast kolem kyslíku stává negativnější než oblasti kolem obou atomů vodíku.
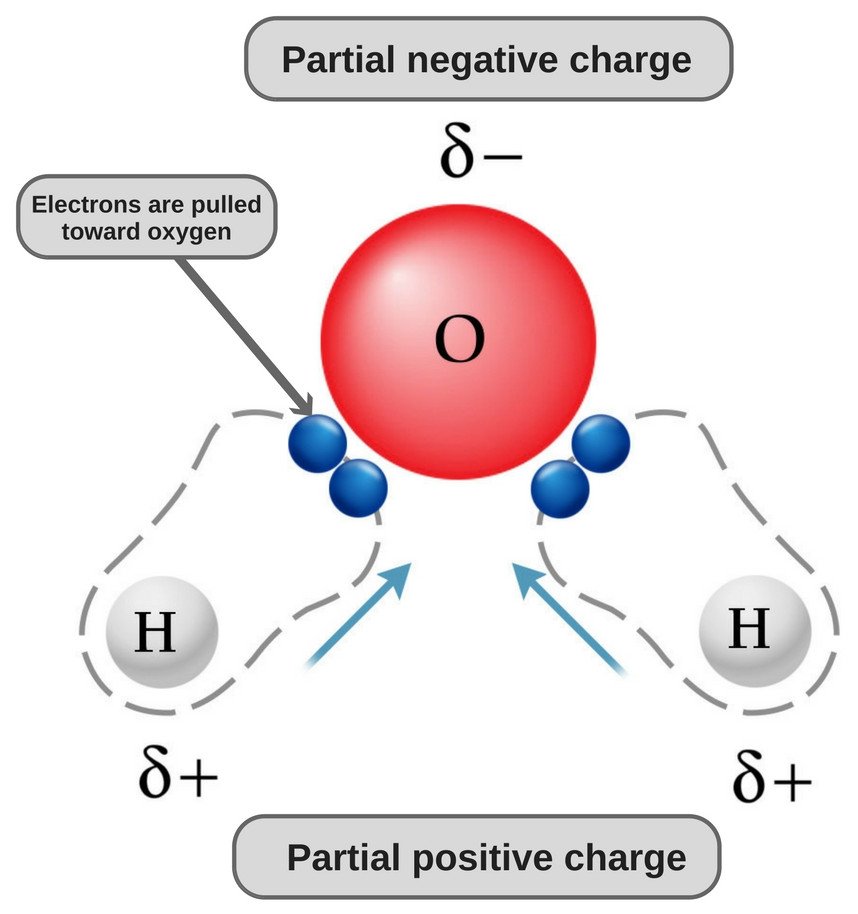
To je důvod, proč se molekula vody stává polární!