Správná odpověď je: C. 18F-FDG PET/CT
Po diskusi s kardiologickým týmem jsme se rozhodli pro nukleární zobrazovací vyšetření, abychom zjistili, zda se jedná o absces kořene aorty. Nouzové vyšetření pozitronovou emisní tomografií/počítačovou tomografií (PET/CT) s fluorodeoxyglukózou F 18 (18F-FDG) objasnilo ložisko intenzivního vychytávání 18F-FDG v sousedství kalcifikací kořene aorty s rozšířením zánětu na pravou přední stranu kořene aorty. Tyto nálezy odpovídaly fokální aortitidě. Zaznamenán byl také perikardiální výpotek se smíšenou hustotou opouzdřený lemem mírného vychytávání 18F-FDG, což představovalo bílkovinnou/hemoragickou složku výpotku a probíhající perikarditidu (obrázek 1).
Obrázek 1
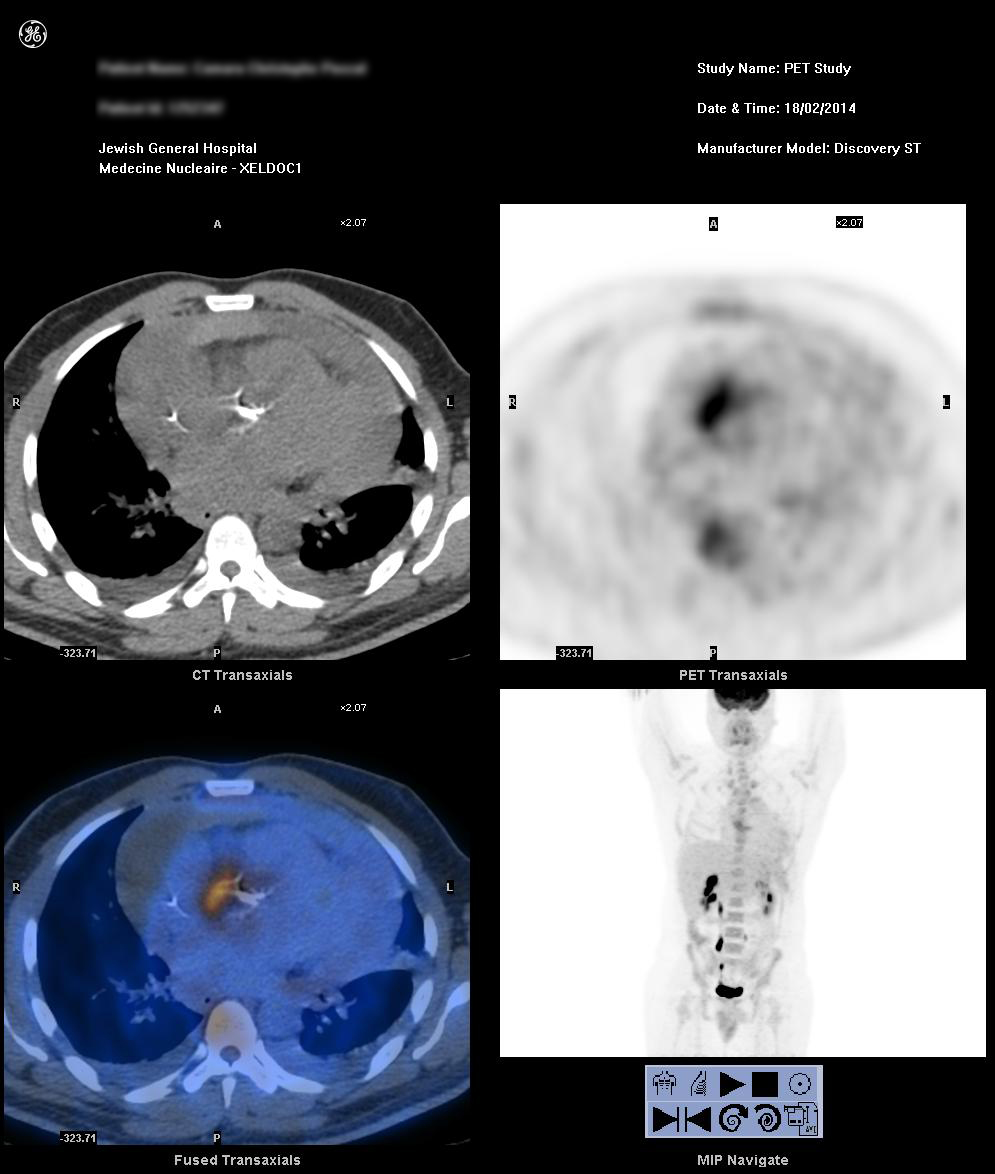
U našeho pacienta byla následně diagnostikována akutní endokarditida aortální chlopně na nativní aortální chlopni, která byla komplikována abscesem aortálního kořene i obsaženou rupturou aortálního kořene, což vedlo k hemoragické perikarditidě. Předně umístěný absces byl na TEE retrospektivně zastíněn silně kalcifikovanou aortální chlopní.
Pacient byl urgentně odeslán na operační sál, kde chirurgové zaznamenali napjatý perikard s přítomností krve, hemoperikard a množství krevních sraženin nad přední stranou pravé komory. Dále zjistili hemoragickou perikarditidu a infikovaný kořen aorty, zejména nad pravým koronárním sinem a nekoronárním sinem. Ačkoli na vnější straně aortálního kořene nebyl otevřený hnis, identifikovali oblast obsažené ruptury a zazděného abscesu. Nakonec bylo zjištěno, že aortální chlopeň je silně kalcifikovaná pravděpodobně revmatickým onemocněním, na kterém byly identifikovány vegetace.
Přítomnost perivalvulárního rozšíření IE je spojena se špatnou prognózou. Mezi tyto komplikace patří tvorba abscesů, pseudoaneuryzmat a píštělí.1 Vzhledem k tomu, že přítomnost abscesu kořene aorty je urgentní indikací k operaci, je její rychlá a přesná diagnóza povinná ve snaze snížit perioperační morbiditu a mortalitu.2
TEE díky lepší kvalitě obrazu a těsné blízkosti jednotlivých dotčených struktur spolu s vyšší frekvencí sond umožňuje detailnější prostorové a časové rozlišení k detekci chlopenní vegetace a všech souvisejících komplikací.3 Navíc je TEE se senzitivitou 90 % považována za lepší diagnostickou zobrazovací metodu ve srovnání s TTE (senzitivita přibližně 50 %) při diagnostice abscesů u komplikované endokarditidy aortální chlopně.4,5 Evropská kardiologická společnost (ESC) proto doporučuje TEE, pokud je TTE suboptimální kvality, pokud je přítomna protetická chlopeň nebo pokud existuje podezření na komplikace způsobené tímto infekčním procesem.
Abscesy předního kořene aorty byly klasicky obtížněji diagnostikovatelné. Jsou lépe viditelné v podélné rovině a k identifikaci jejich přítomnosti je zapotřebí zobrazení ve více rovinách.2 Přítomnost kalcifikací navíc brání přenosu ultrazvukových vln při TEE a je zřejmým omezením při posuzování kalcifikované aortální chlopně.6 V důsledku toho bylo v našem případě k upřesnění diagnózy podezření na infikovanou endokarditidu vyhledáno použití alternativního zobrazovacího vyšetření.
V předchozí iteraci pokynů ESC pro diagnostiku a léčbu endokarditidy bylo doporučeno opakovat TEE do 7-10 dnů od prezentace, pokud je počáteční zobrazovací vyšetření negativní, ale klinické podezření na IE zůstává vysoké.1,7-10 Nedávné studie však prokázaly dodatečnou diagnostickou hodnotu PET/CT u infekcí zahrnujících chlopenní protézy a zařízení, kdy je diagnóza často obtížná. Saby et al. zjistili, že u endokarditidy chlopenních protéz má PET/CT senzitivitu 73 % a specificitu 80 %. Při kombinaci výsledků PET/CT s tradičními Dukeovými kritérii se senzitivita a specificita pro diagnózu IE zvýšila ze 70 na 97 %, resp. z 52 na 91 %.1,10 Zařazení PET/CT do modifikovaných Dukeových kritérií navíc umožnilo stanovit diagnózu dříve, zejména pokud byla echokardiografie normální nebo pochybná, a co je důležitější, ještě předtím, než došlo k jakémukoli infekčnímu poškození nebo nežádoucí příhodě.10 Poslední iterace pokynů ESC pro diagnostiku a léčbu endokarditidy tak zahrnula 18F-FDG PET/CT v případě diagnostické nejistoty. My jako tým jsme z těchto údajů extrapolovali, že při silné kalcifikaci by PET/CT umožnilo potvrdit naše podezření v případě endokarditidy nativní chlopně.
Závěr
TEE, zejména v případě endokarditidy mitrální chlopně, je pro diagnostiku a hodnocení IE a s ní spojených komplikací jednoznačně lepší než TTE. Na druhé straně endokarditida aortální chlopně se někdy může ukázat jako diagnostický problém, zejména při hodnocení předního kořene aorty na přítomnost abscesu. Za těchto okolností hrají TTE a TEE doplňující roli při stanovení definitivní diagnózy. Tuto diagnostickou výzvu může zvýraznit, jak ukazuje tento případ, přítomnost protézy nebo silné kalcifikace. Za těchto okolností by mělo být získáno alternativní zobrazovací vyšetření. PET-CT může při podezření na periaortální abscesy umožnit časnější definitivní diagnózu a zabránit progresi závažných komplikací.
- Habib G, Lancellotti P, Antunes MJ, et al. 2015 ESC Guidelines for the management of infective endocarditis: Pracovní skupina pro léčbu infekční endokarditidy Evropské kardiologické společnosti (ESC). Schváleno: Kardiologický ústav AV ČR, v. v. i: Evropská asociace pro kardiochirurgii (EACTS), Evropská asociace nukleární medicíny (EANM). Eur Heart J 2015;36:3075-128.
- Leung DY, Cranney GB, Hopkins AP, Walsh WF. Úloha transoezofageální echokardiografie v diagnostice a léčbě abscesu kořene aorty. Br Heart J 1994;72:175-81.
- Karalis DG, Bansal RC, Hauck AJ, et al. Transesophageal echocardiographic recognition of subaortic complications in aortic valve endocarditis. Klinické a chirurgické důsledky. Circulation 1992;86:353-62.
- Habib G, Badano L, Tribouilloy C, et al. Recommendations for the practice of echocardiography in infective endocarditis. Eur J Echocardiogr 2010;11:202-19.
- Daniel WG, Mügge A, Martin RP, et al. Zlepšení diagnostiky abscesů spojených s endokarditidou pomocí transezofageální echokardiografie. N Engl J Med 1991;324:795-800.
- Iung B, Rouzet F, Brochet E, Duval X. Cardiac Imaging of Infective Endocarditis, Echo and Beyond. Curr Infect Dis Rep 2017;19:8.
- Habib G, Hoen B, Tornos P, et al. Guidelines on the prevention, diagnosis, and treatment of infective endocarditis (new version 2009): the Task Force on the Prevention, Diagnosis, and Treatment of Infective Endocarditis of the European Society of Cardiology (ESC). Schváleno Evropskou společností klinické mikrobiologie a infekčních nemocí (ESCMID) a Mezinárodní společností pro chemoterapii (ISC) pro infekce a rakovinu. Eur Heart J 2009;30:2369-413.
- Pérez-Vázquez A, Fariñas MC, García-Palomo JD, Bernal JM, Revuelta JM, González-Macías J. Evaluation of the Duke criteria in 93 episodes of prosthetic valve endocarditis: could sensitivity be improved? Arch Intern Med 2000;160:1185-91.
- Roque A, Pizzi MN, Cuéllar-Calàbria H, Aguadé-Bruix S. 18F-FDG-PET/CT Angiography for the Diagnosis of Infective Endocarditis. Curr Cardiol Rep 2017;19:15.
- Saby L, Laas O, Habib G, et al. Positron emission tomography/computed tomography for diagnosis of prosthetic valve endocarditis: increased valvular 18F-fluorodeoxyglucose uptake as a novel major criterion. J Am Coll Cardiol 2013;61:2374-82.
.