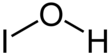
El ácido hipoiódico es el compuesto inorgánico de fórmula química HIO. Se forma cuando se trata una solución acuosa de yodo con sales de mercurio o plata. Se descompone rápidamente por desproporción:
|
|||
 |
|||
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC
Ácido hipoideo
|
|||
| Identificadores | |||
|
|||
|
Modelo 3D (JSmol)
|
|||
| ChEBI |
|
||
| ChemSpider |
|
||
|
PubChem CID
|
|||
| UNII |
|
||
|
CompTox Dashboard (EPA)
|
|||
|
|||
|
|||
| Propiedades | |||
| HIO | |||
| Masa molecular | 143.89 g/mol | ||
| Acidez (pKa) | 10.5 (en agua, estimación) | ||
| Base conjugada | Hipoiodita | ||
|
Salvo que se indique lo contrario, los datos se dan para materiales en su estado estándar (a 25 °C , 100 kPa).
|
|||
| |
|||
| Referencias Infobox | |||
5 HIO → HIO3 + 2 I2 + 2 H2O
Los hipoioditos de los metales alcalinos y alcalinotérreos pueden hacerse en soluciones diluidas frías si se añade yodo a sus respectivos hidróxidos.El ácido hipoiódico es un ácido débil con un pKa de aproximadamente 11. La base conjugada es el hipoiodito (IO-). Las sales de este anión pueden prepararse tratando el I2 con hidróxidos alcalinos. Se desproporcionan rápidamente para formar yoduros y yodatos.