Bedömning | Biopsykologi | Jämförande | Kognitiv | Utveckling | Språk | Individuella skillnader | Personlighet | Filosofi | Social |
Metoder | Statistik | Klinisk | Pedagogisk | Utbildningsvetenskap | Industriell | Professionell | Världspsykologi |
Biologisk:Beteendegenetik – Evolutionspsykologi – Neuroanatomi – Neurokemi – Neuroendokrinologi -Neurovetenskap – Psykoneuroimmunologi – Fysiologisk psykologi – Psykofarmakologi(Index, Översikt)
| Hjärnan: Hypotalamus | ||
|---|---|---|
 |
||
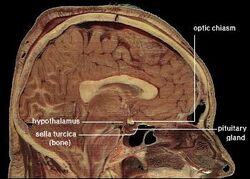
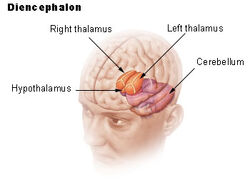
| Hypotalamus hos människan | ||
 |
||
| Dienchephalon | ||
| Latin | hypothalamus | |
| Grays | subjekt #189 812 | |
| del av | ||
| Komponenter | ||
| Arterie | ||
| Vein | ||
| HjärnaInfo/UW | hier-358 | |
| MeSH | A08.186.211.730.385.357 | |
Hypotalamus förbinder nervsystemet med det endokrina systemet via hypofysen (hypofysen). Hypothalamus, (från grekiska ὑποθαλαμος = under thalamus) ligger under thalamus, strax ovanför hjärnstammen. Denna körtel upptar större delen av den ventrala regionen av diencephalon. Den finns i alla däggdjurshjärnor. Hos människor är den ungefär lika stor som en mandel.
Hypotalamus reglerar vissa metaboliska processer och andra aktiviteter i det autonoma nervsystemet. Den syntetiserar och utsöndrar neurohormoner, ofta kallade hypotalamiskt frigörande hormoner, och dessa stimulerar eller hämmar i sin tur utsöndringen av hypofyshormoner.
Hypotalamus kontrollerar kroppstemperatur, hunger, törst, trötthet, ilska och cirkadiska cykler.
- Inflöden
- Olfaktoriska stimuli
- Blodburna stimuli
- Steroider
- Neurala ingångar
- Kärnor
- Utfall
- Neurala projektioner
- Endokrina hormoner
- Kontroll av födointag
- Könsdimorfism
- Reaktioner på ovarialsteroider
- Gonadala steroider i råttors neonatala liv
- Androgener hos primater
- Andra influenser på hypotalamusutvecklingen
- Effekter av åldrande på hypotalamus
- Se även
- Ytterligare bilder
- Referenser & Bibliografi
- Papper
- Ytterligare material
- Papper
Inflöden
Hypotalamus är en mycket komplex region i människans hjärna, och även små kärnor i hypotalamus är involverade i många olika funktioner. Den paraventrikulära kärnan innehåller till exempel oxytocin- och vasopressin (även kallat antidiuretiskt hormon) neuroner som projicerar till den bakre hypofysen, men innehåller också neuroner som reglerar ACTH- och TSH-sekretionen (som projicerar till den främre hypofysen), magreflexer, modersbeteende, blodtryck, födointag, immunreaktioner och temperatur.
Hypotalamus samordnar många hormonella och beteendemässiga cirkadiska rytmer, komplexa mönster av neuroendokrina utflöden, komplexa homeostatiska mekanismer och många viktiga beteenden. Hypotalamus måste därför reagera på många olika signaler, varav en del genereras externt och en del internt. Den är därför nära förbunden med många delar av CNS, inklusive hjärnstammens retikulära formation och autonoma zoner, den limbiska framhjärnan (särskilt amygdala, septum, Brocas diagonala band, luktbulberna och hjärnbarken) och hjärnbarken.
Hypotalamus reagerar på:
- Ljus: Dagslängd och fotoperiod för reglering av cirkadiska och säsongsmässiga rytmer
- Olfaktoriska stimuli, inklusive feromoner
- Steroider, inklusive gonadala steroider och kortikosteroider
- Neuralt överförd information som kommer särskilt från hjärtat, magen, och fortplantningssystemet
- Autonoma inflöden
- Blodburna stimuli, inklusive leptin, ghrelin, angiotensin, insulin, hypofyshormoner, cytokiner, plasmakoncentrationer av glukos och osmolaritet etc
- Stress
- Invadera mikroorganismer genom att öka kroppstemperaturen, ställa om kroppens termostat uppåt.
Olfaktoriska stimuli
Olfaktoriska stimuli är viktiga för reproduktion och neuroendokrin funktion hos många arter. Om till exempel en dräktig mus utsätts för urin från en ”främmande” hane under en kritisk period efter samlag misslyckas dräktigheten (Bruce-effekten). Under samlag bildar en mushona ett exakt ”olfaktoriskt minne” av sin partner som består i flera dagar. feromonala signaler underlättar synkroniseringen av brunsten hos många arter. Hos kvinnor kan synkroniserad menstruation också uppstå på grund av feromonala signaler, även om vissa ifrågasätter feromonernas roll hos människor.
Blodburna stimuli
Peptidhormoner har viktiga influenser på hypotalamus, och för att kunna göra det måste de ta sig förbi blod-hjärnbarriären. Hypotalamus avgränsas delvis av specialiserade hjärnregioner som saknar en effektiv blod-hjärnbarriär; det kapillära endotelet på dessa platser är fenestrerat för att tillåta fri passage av även stora proteiner och andra molekyler. Några av dessa områden är platser för neurosekretion – neurohypofysen och den mediala eminensen. Andra är platser där hjärnan tar prover på blodets sammansättning. Två av dessa platser, det subfornikala organet och OVLT (organum vasculosum of the lamina terminalis) är så kallade circumventrikulära organ, där neuronerna är i intim kontakt med både blod och CSF. Dessa strukturer är tätt vaskulariserade och innehåller osmoreceptiva och natriumreceptiva neuroner som kontrollerar drickande, vasopressinfrisättning, natriumutsöndring och natriumapptit. De innehåller också neuroner med receptorer för angiotensin, atriell natriuretisk faktor, endotelin och relaxin, som alla är viktiga för regleringen av vätske- och elektrolytbalansen. Neuroner i OVLT och SFO projicerar till den supraoptiska kärnan och den paraventrikulära kärnan och även till preoptiska hypotalamiska områden. De circumventrikulära organen kan också vara den plats där interleukiner verkar för att framkalla både feber och ACTH-sekretion, via effekter på paraventrikulära neuroner.
Det är inte klart hur alla peptider som påverkar den hypotalamiska aktiviteten får den nödvändiga tillgången. När det gäller prolaktin och leptin finns det bevis för ett aktivt upptag vid plexus choroidus från blod till CSF. Vissa hypofyshormoner har ett negativt återkopplingsinflytande på hypotalamisk sekretion; till exempel återkopplar tillväxthormon till hypotalamus, men hur det kommer in i hjärnan är oklart. Det finns också bevis för att prolaktin och TSH verkar centralt.
Steroider
Hypotalamus innehåller neuroner som är känsliga för gonadala steroider och glukokortikoider – (binjurens steroidhormoner som frisätts som svar på ACTH). Den innehåller också specialiserade glukoskänsliga neuroner (i arcuate nucleus och ventromedial hypothalamus) som är viktiga för aptiten. Det preoptiska området innehåller termokänsliga neuroner; dessa är viktiga för TRH-sekretionen.
Neurala ingångar
Hypothalamus får många ingångar från hjärnstammen; särskilt från kärnan i den solitära trakten, locus coeruleus och ventrolaterala medulla. Oxytocinutsöndring som svar på amning eller vagino-cervikal stimulering förmedlas av några av dessa vägar; vasopressinutsöndring som svar på kardiovaskulära stimuli som kommer från kemoreceptorer i sinus carotis och aortabågen, och från förmaksvolymreceptorer med lågt tryck, förmedlas av andra. Hos råttan orsakar stimulering av vagina också prolaktinsekretion, vilket leder till pseudo-graviditet efter en infertil parning. Hos kaninen framkallar samlag reflexmässig ägglossning. Hos får kan stimulering av livmoderhalsen i närvaro av höga nivåer av östrogen framkalla moderligt beteende hos en jungfrulig tacka. Alla dessa effekter förmedlas av hypotalamus, och informationen överförs huvudsakligen via ryggmärgsbanor som vidarebefordras till hjärnstammen. Stimulering av bröstvårtorna stimulerar frisättningen av oxytocin och prolaktin och undertrycker frisättningen av LH och FSH.
Kardiovaskulära stimuli överförs av vagusnerven, men vagus förmedlar också en mängd olika visceral information, inklusive till exempel signaler som härrör från gastrisk distension för att undertrycka matning. Även denna information når hypotalamus via reläer i hjärnstammen.
Kärnor
De hypotalamiska kärnorna omfattar följande:
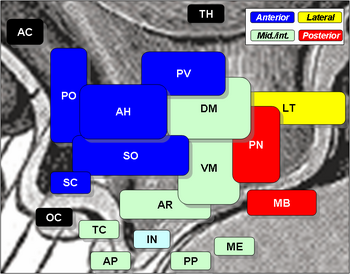
Hypotalamiska kärnor
| Region | Area | Nucleus | Funktion |
| Anterior | Medial | Medial preoptisk kärna |
|
| Supraoptisk kärna (SO) |
|
||
| Paraventrikulär kärna (PV) |
|
||
| Anterior hypotalamisk kärna (AH) |
|
||
| Suprachiasmatisk kärna (SC) |
|
||
| Laterala | Laterala preoptiska kärnan | ||
| Laterala kärnan (LT) |
|
||
| Del av supraoptisk kärna (SO) |
|
||
| Tuberal | Medial | Dorsomedial hypotalamisk kärna (DM) |
|
| Ventromedial kärna (VM) |
|
||
Arcuate nucleus (AR)
|
|||
| Lateral | Lateral kärna (LT) |
|
|
| Lateral tuberal nuclei | |||
| Posterior | Medial | Mammillärkärnor (del av mammillärkroppar) (MB) |
|
| Bakre kärnan (PN) |
|
||
| Lateral | Lateral nucleus (LT) |
Se även: Ventrolaterala preoptiska kärnan
Utfall
Hypotalamusens utfall kan delas in i två kategorier: neurala projektioner och endokrina hormoner.
Neurala projektioner
De flesta fibersystem i hypotalamus löper i två riktningar (dubbelriktade).
- Projektioner till områden kaudala till hypotalamus går genom det mediala främre hjärnbunten, den mammillotegmentala banan och den dorsala longitudinella fascikeln.
- Projektioner till områden rostralt om hypothalamus går via den mammillothalamiska trakten, fornix och terminal stria.
Endokrina hormoner
Hypothalamus påverkar det endokrina systemet och styr känslomässigt beteende, som till exempel, ilska och sexuell aktivitet. De flesta av de hypotalamiska hormoner som genereras distribueras till hypofysen via det hypofysiska portalsystemet. Hypotalamus upprätthåller homeostas detta inkluderar en reglering av blodtryck, hjärtfrekvens och temperatur.
De primära hypotalamiska hormonerna är:
| Namn | Andra namn | Abkortningar | Placering | Funktion |
|---|---|---|---|---|
| Corticotropinfrisättande hormon | Corticotropinfrisättande faktor, kortikolibrerin | CRH, CRF | parvocellulära neuroendokrina neuroner i den paraventrikulära kärnan | med vasopressin, stimulerar främre hypofysen att utsöndra ACTH |
| Dopamin | Prolaktinhämmande hormon | DA, PIH | neuroendokrina neuroner i den bågformiga kärnan | hämmar utsöndringen av prolaktin från den främre hypofysen |
| Gonadotropinfrisättande hormon | Luteiniserande hormonfrisättande hormon | GnRH, LHRH | neuroendokrina neuroner i de mediala preoptiska och arcuate kärnorna | stimulerar främre hypofysen att utsöndra LH och FSH |
| Växthormonfrisättande hormon | Växthormonfrisättande faktor, somatokrinin | GHRH, GHRF, GRF | Arcuate nucleus neuroendokrina neuroner | stimulerar främre hypofysen att utsöndra tillväxthormon |
| Melatonin | suprachiasmatisk kärna | |||
| Somatostatin | Växthormon-hämmande hormon, Somatotropinfrisättande hämmande faktor | SS, GHIH, SRIF | neuroendokrina neuroner i den periventrikulära kärnan | hämmar utsöndringen av tillväxthormon från den främre hypofysen |
| Thyrotropinfrisättande hormon | Thyrotropinfrisättande faktor, Thyroliberin, Protirelin | TRH, TRF | parvocellulära neuroendokrina neuroner i de paraventrikulära och främre hypotalamiska kärnorna | stimulerar främre hypofysen till att utsöndra TSH |
Se även: Hypokretin
Kontroll av födointag
Den yttersta laterala delen av den ventromediala kärnan i hypotalamus ansvarar för kontrollen av födointag. Stimulering av detta område orsakar ökat matintag. Bilateral lesion av detta område orsakar fullständigt upphörande av födointag. De mediala delarna av kärnan har en kontrollerande effekt på den laterala delen. Bilateral lesion av den mediala delen av den ventromediala kärnan orsakar hyperfagi och fetma hos djuret. Ytterligare lesion av den laterala delen av den ventromediala kärnan hos samma djur ger fullständigt upphörande av födointag.
Det finns olika hypoteser relaterade till denna reglering:
- Lipostatisk hypotes – denna hypotes menar att fettvävnaden producerar en humoral signal som står i proportion till fettmängden och som verkar på hypothalamus för att minska födointaget och öka energiuttaget. Det har visat sig att ett hormon leptin verkar på hypotalamus för att minska födointaget och öka energiuttaget.
- Gutpeptidhypotes – gastrointestinala hormoner som Grp, glukagoner, CCK och andra påstås hämma födointaget. Maten som kommer in i mag-tarmkanalen utlöser frisättning av dessa hormoner som verkar på hjärnan för att producera mättnadskänsla. Hjärnan innehåller både CCK-A- och CCK-B-receptorer.
- Glukostatisk hypotes – aktiviteten hos mättnadscentret i de ventromediala kärnorna styrs troligen av glukosanvändningen i neuronerna. Det har postulerats att när deras glukosutnyttjande är lågt och följaktligen när den arteriovenösa blodglukosdifferensen över dem är låg, minskar aktiviteten över neuronerna. Under dessa förhållanden är aktiviteten i matningscentret okontrollerad och individen känner sig hungrig. Matintaget ökar snabbt genom intraventrikulär administrering av 2-deoxyglukos och minskar därför glukosutnyttjandet i cellerna.
- Thermostatisk hypotes – enligt denna hypotes stimulerar en sänkning av kroppstemperaturen under ett visst börvärde aptiten, medan en ökning över börvärdet hämmar aptiten.
Könsdimorfism
Flera hypotalamiska kärnor är könsdimorfa, dvs. det finns tydliga skillnader i både struktur och funktion mellan män och kvinnor.
Vissa skillnader är uppenbara till och med i den grova neuroanatomin: mest anmärkningsvärd är den könsdimorfa kärnan inom det preoptiska området, som endast finns hos män. De flesta skillnaderna är dock subtila förändringar i konnektiviteten och den kemiska känsligheten hos särskilda uppsättningar av neuroner.
Den viktiga betydelsen av dessa förändringar kan kännas igen genom funktionella skillnader mellan män och kvinnor. Till exempel är mönstret för utsöndring av tillväxthormon könsdimorf, och detta är en av anledningarna till att vuxna hanar hos många arter är mycket större än honor.
Reaktioner på ovarialsteroider
Andra slående funktionella dimorfismer finns i de beteendemässiga reaktionerna på ovarialsteroider hos den vuxna individen. Män och kvinnor reagerar olika på ovarialsteroider, delvis på grund av att uttrycket av östrogenkänsliga neuroner i hypotalamus är könsdimorf, dvs. östrogenreceptorer uttrycks i olika uppsättningar av neuroner.
Östrogen och progesteron kan påverka genuttrycket i särskilda neuroner eller inducera förändringar i cellmembranpotentialen och kinasaktivering, vilket leder till olika icke-genomiska cellulära funktioner. Östrogen och progesteron binder till sina kärnhormonreceptorer, som translokaliseras till cellkärnan och interagerar med DNA-regioner som kallas Hormonresponselement (HRE) eller knyts till en annan transkriptionsfaktors bindningsställe. Östrogenreceptorn (ER) har visat sig transaktivera andra transkriptionsfaktorer på detta sätt, trots avsaknaden av ett östrogenresponselement (ERE) i genens proximala promotorregion. ER och progesteronreceptorer (PR) är generellt sett genaktiverare, med ökad mRNA- och efterföljande proteinsyntes efter hormonexponering.
Manliga och kvinnliga hjärnor skiljer sig åt när det gäller fördelningen av östrogenreceptorer, och denna skillnad är en irreversibel konsekvens av neonatal steroidexponering. Östrogenreceptorer (och progesteronreceptorer) finns huvudsakligen i neuroner i den främre och mediobasala hypothalamus, särskilt:
- det preoptiska området (där LHRH-neuronerna är lokaliserade)
- den periventrikulära kärnan (där somatostatinneuronerna är lokaliserade)
- den ventromediala hypotalamus (som är viktig för sexuellt beteende).
Gonadala steroider i råttors neonatala liv
I det neonatala livet påverkar gonadala steroider utvecklingen av den neuroendokrina hypotalamus. De bestämmer till exempel förmågan hos honor att uppvisa en normal reproduktionscykel och hos hanar och honor att uppvisa lämpliga reproduktionsbeteenden i det vuxna livet.
- Om en råtthona injiceras en gång med testosteron under de första dagarna av det postnatala livet (under den ”kritiska perioden” för påverkan av könssteroider), blir hypotalamus irreversibelt maskuliniserad; den vuxna råttan kommer att vara oförmögen att generera en LH-ökning som svar på östrogen (vilket är karakteristiskt för honor), men kommer att kunna uppvisa manliga sexuella beteenden (bestiga en sexuellt mottaglig hona).
- Däremot kommer en hanråtta som kastreras strax efter födseln att feminiseras, och den vuxna råttan kommer att uppvisa kvinnliga sexuella beteenden som svar på östrogen (sexuell mottaglighet, lordos).
Androgener hos primater
Inom primater är androgenernas utvecklingsmässiga inflytande mindre tydligt och konsekvenserna är mindre fullständiga. ’Tomboyism’ hos flickor kan återspegla androgenernas effekter på fosterhjärnan, men uppväxtkönet under de första 2-3 åren anses av många vara den viktigaste bestämmande faktorn för könsidentitet, eftersom antingen östrogen eller testosteron under denna fas kommer att ha permanenta effekter på antingen en kvinnlig eller en manlig hjärna, vilket påverkar både heterosexualitet och homosexualitet.
Paradoxen är att testosteronets maskuliniserande effekter förmedlas av östrogen. I hjärnan aromatiseras testosteron till (östradiol), vilket är det huvudsakliga aktiva hormonet för utvecklingsinflytande. Den mänskliga testikeln utsöndrar höga nivåer av testosteron från ungefär vecka 8 i fosterlivet till 5-6 månader efter födseln (en liknande perinatal ökning av testosteron observeras hos många arter), en process som tycks ligga till grund för den manliga fenotypen. Östrogen från moderns cirkulation är relativt ineffektivt, delvis på grund av de höga cirkulerande nivåerna av steroidbindande proteiner under graviditeten.
Andra influenser på hypotalamusutvecklingen
Könsstroiderna är inte de enda viktiga influenserna på hypotalamusutvecklingen; särskilt stress före puberteten i det tidiga livet bestämmer den vuxna hypotalamusens förmåga att reagera på en akut stressor. Till skillnad från gonadala steroidreceptorer är glukokortikoidreceptorer mycket utbredda i hela hjärnan. I den paraventrikulära kärnan förmedlar de negativ återkopplingskontroll av CRF-syntesen och -utsöndringen, men på andra ställen är deras roll inte väl förstådd.
Effekter av åldrande på hypotalamus
Studier på honmöss har visat att både den supraoptiska kärnan (SON) och den paraventrikulära kärnan (PVN) förlorar ungefär en tredjedel av de celler som är immunoreaktiva för IGF-1R vid normalt åldrande. Gamla kaloribegränsade (CR) möss förlorade också ett större antal IGF-1R icke-immunoreaktiva celler samtidigt som de bibehöll liknande antal IGF-1R-immunoreaktiva celler i jämförelse med gamla al-möss. Följaktligen uppvisar gamla CR-möss en högre andel IGF-1R-immunoreaktiva celler, vilket återspeglar en ökad hypotalamisk känslighet för IGF-1 i jämförelse med normalt åldrande möss.
Se även
- HPA-axel
- Hypothalamo hypofysesystem
- Hypothalamo hypofys- och binjuresystem
- Hypothalamuslesioner
- Medial forebrain bundle
- Neuroendokrinologi
- Preoptiskt område
.
Ytterligare bilder
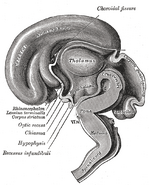
Lägg ett foto till detta galleri
- http://www.cancer.gov/Templates/db_alpha.aspx?CdrID=46359
- http://www.sci.uidaho.edu/med532/hypothal.htm
- Diagram över atomkärnor (psycheducation.org)
- Diagram of Nuclei (universe-review.ca)
- Diagram of Nuclei (utdallas.edu)
- Om inget annat anges i tabellen är ref: Guyton Eight Edition
- Walter F., PhD. Boron. Medicinsk fysiologi: A Cellular And Molecular Approaoch, Elsevier/Saunders. Sid 840
- http://thalamus.wustl.edu/course/hypoANS.html
- http://www.vivo.colostate.edu/hbooks/pathphys/endocrine/hypopit/overview.html
- Theologides A (1976). Anorexia-producerande intermediära metaboliter. Am J Clin Nutr 29 (5): 552-8.
- John Money, ”The concept of gender identity disorder in childhood and adolescence after 39 years”, Journal of Sex and Marital Therapy 20 (1994): 163-77.
- Romeo, Russell D, Rudy Bellani, Ilia N. Karatsoreos, Nara Chhua, Mary Vernov, Cheryl D. Conrad och Bruce S. McEwen (2005). Stresshistoria och pubertetsutveckling samverkar för att forma hypotalamus-hypofys- och binjureaxelns plasticitet. Endocrinology 147 (4): 1664-1674.
- Saeed O,Yaghmaie F,Garan SA,Gouw AM,Voelker MA,Sternberg H, Timiras PS. (2007). Immunoreaktiva celler med insulinliknande tillväxtfaktor-1-receptor bibehålls selektivt i den paraventrikulära hypothalamus hos kaloriskt begränsade möss. Int J Dev Neurosci 25 (1): 23-8.
- Yaghmaie F, Saeed O, Garan SA, Voelker MA, Gouw AM, Freitag W, Sternberg H, Timiras PS (2006). Åldersberoende förlust av immunoreaktiva celler med insulinliknande tillväxtfaktor-1-receptor i den supraoptiska hypotalamus minskar hos kaloriskt begränsade möss. Int J Dev Neurosci 24 (7): 431-6.
- F. Yaghmaie, O. Saeed, S.A. Garan, A.M. Gouw, P. Jafar, J. Kaur, S. Nijjar, P.S. Timiras, H. Sternberg, M.A. Voelker (2007). Spårning av förändringar i hypotalamisk IGF-1-känslighet med åldrande och kalorirestriktion. Experimental Gerontology 42 (1-2): 148-149.
Referenser & Bibliografi
Papper
- Arees, E.A. and Mayer, B, (1967) Anatomical connections between medial and lateral regions of the hypothalamus concerned with food intake, Science 157: 1574-5
- Grossman, S.P. (1960) Eating or drinking elicited by direct adrenergic or cholinergic stimulation of the hypothalamus, Science 132: 301-2.
- Hetherington, A.W. and Ranson, S.W. (1942) The relation of various hypothalamic lesions to adiposity in the rat, 76: 475-99.
Ytterligare material
Papper
- Google Scholar
.
- BrainMaps at UCDavis Hypothalamus
- Endokrina systemet och hypothalamus
- Hög-Resolution Cytoarchitectural Primate Brain Atlases
- The Hypothalamus and Pituitary at endotexts.org
- Diagram of Nuclei (psycheducation.org)
- Diagram of Nuclei (universe-review.ca)
- Diagram of Nuclei (utdallas.edu)
|
v-d-e
Mänsklig hjärna: diencephalon (TA A14.1.08, GA 9.807) |
||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Epithalamus |
|
Överyta
|
||||||||||||||
| Thalamus |
|
Överyta
|
Grå substans/
kärnor |
|||||||||||||
| Hypothalamus |
|
|||||||||||||||
| Subthalamus |
Subthalamisk kärna – Zona incerta |
|||||||||||||||
| Ventrikelsystemet: Tredje kammaren |
fördjupningar: (Optisk fördjupning, Infundibulär fördjupning, Suprapineal fördjupning, Pineal fördjupning) Hypothalamisk sulcus – Tela chorioidea i tredje ventrikeln Subfornikalt organ Öppningar: Interventrikulär/Monro Posterior commissure |
|||||||||||||||
|
v-d-e
Mänsklig anatomi, endokrina systemet: endokrina körtlar |
||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Hypotalamiska/ hypofysiska axlar |
|
|
|
|
||||||||||||
| Kotpelaren |
Kotpelaren – Korpora arenacea |
|||||||||||||||
| Islets of pankreas |
Alphacell – Betacell – Deltacell – PP-cell – Epsiloncell |
|||||||||||||||
Humana hjärnan: Limbiskt system
Amygdala – Cingulate gyrus – Fornicate gyrus – Hippocampus – Hypothalamus – Mammillary body – Nucleus accumbens – Orbitofrontal cortex – Parahippocampal gyrus