Detta kapitel är mest relevant för avsnitt F8(ii) i 2017 års kursplan för CICM Primary Syllabus, där man förväntar sig att examinanderna ska kunna ”beskriva koldioxidhanteringen i blodet, inklusive Haldaneeffekten och kloridskiftet”. Även om ingen någonsin har ställt en CICM SAQ med formuleringen ”Vad är Haldane-effekten?” är det helt klart en rimlig fråga och man bör förvänta sig att kunna detta för detta prov. Som de flesta vettiga människor hänvisade Haldane inte till denna sak som ”min effekt”, även om han uppenbarligen kunde ha gjort det med minimal falsk blygsamhet eftersom det i själva verket var Haldanes eget defibrinerade blod som användes för experimentet.
Sammanfattningsvis:
- Haldaneeffekten är ett fysikalisk-kemiskt fenomen som beskriver blodets ökade förmåga att transportera koldioxid under förhållanden med minskad syremättnad av hemoglobin
- Både Haldane- och Bohr-effekten är samma egenskaper hos samma fenomen
- Haldaneeffekten är vad som händer med pH-värdet och koldioxidbindningen på grund av syre, och Bohr-effekten är vad som händer med syrebindningen på grund av koldioxid och lägre pH.
- Mer koldioxid binds till hemoglobin vid lägre syremättnad
- Denna effekt underlättar avlägsnandet av koldioxid från vävnaderna
Bundet. CO2 frigörs från hemoglobin när det blir syresatt
- Denna ”omvända Haldane-effekt” underlättar elimineringen av CO2
- Det finns två mekanismer:
- Det syrefria hemoglobinet har en högre affinitet för CO2
- Detta beror på den allosteriska moduleringen av CO2-bindningsställen av det syrefria hemoglobinet
- Den buffrande kapaciteten hos det syrefria hemoglobinet ökar;
- Reducerat (syrefritt) hemoglobin blir mer basiskt
- Detta ökar pH-värdet i RBC-cytosolen
- Med ett ökat pH-värde kan mer kolsyra dissociera till bikarbonat
- Därmed, ökar den totala mängden CO2 som transporteras som bikarbonat
- Jämfört med transporten av CO2 av deoxyhemoglobin spelar denna del av Haldaneeffekten en mindre roll
Tebboul & Scheeren (2017) erbjuder en utan krusiduller avfettad förklaring, och deras artikel är tillgänglig gratis. Om man vill ha fett och krusiduller kan man gå till denna utmärkta genomgång av Itiro Tyuma (1984). Även om det inte är nödvändigt kan man också vilja läsa J.S Haldanes ursprungliga artikel, där han var den tredje författaren (Christiansen et al, 1914).
Definition av Haldane-effekten
Det finns ingen formell definition här, men lyckligtvis har praktiskt taget alla författare som någonsin skrivit om ämnet känt sig tvungna att inleda sin artikel med några inledande ord, där de oundvikligen gör ett försök att definiera detta fenomen, eller åtminstone att så kärnfullt sammanfatta det att det täcks av en enda mening. En representativ definition skulle därför kunna vara:
”Haldaneeffekten är ett fysikalisk-kemiskt fenomen som beskriver blodets ökade förmåga att transportera koldioxid under förhållanden med minskad hemoglobinmättnad”
Och något liknande. I verkligheten är Haldane-effekten och Bohr-effekten olika uttryck för samma molekylära mekanism som är något orelaterad till koldioxid (som bara råkar vara den ligand som är av intresse inom andningsfysiologin). I verkligheten finns det många andra molekylära aktörer (protoner, oorganiska joner som klorid, organiska fosfater som 2,3-DPG) som binder till syrefritt hemoglobin med högre affinitet. Samtidigt tenderar bindningen av dessa olika molekyler att stabilisera hemoglobinmolekylens syrefria T-tillstånd, vilket minskar dess affinitet för syre (vilket i princip är Bohr-effekten). Om man var trogen fakta skulle man alltså tvingas medge att båda effekterna egentligen borde ha samma definition:
”Bohr-Haldane-effekten är ett fysikalisk-kemiskt fenomen som beskriver de förändringar i affiniteten för bindning av icke-syreligander till hemoglobin som är ett resultat av de konforma förändringar som induceras i hemoglobintetrameren genom att syre binds till hem.”
Det är dock inte riktigt så enkelt att det går att säga. Ingen bland CICM-examinatorerna skulle heller bli särskilt upprörd om man föredrar den tidigare nämnda karboxycentrerade definitionen. Haldane- och Bohr-effekter skiljs i allmänhet åt i högskolelitteraturen. Historiskt sett tenderar också examinationsinriktade studiehandledningar som Brandis’ The Physiology Viva att diskutera dem som separata fenomen, förmodligen för att deras kliniska relevans är något annorlunda. I vilket fall som helst skulle man förmodligen klara sig bra om man bara citerade Nunns:
” skillnaden i den mängd koldioxid som transporteras, vid konstant PCO2, i syresatt och syrefritt blod”
Haldaneeffekt på grund av att koldioxid transporteras av syrefritt hemoglobin
Det faktum att koldioxid kan binda till aminosyror för att bilda karbaminsyror och konjugerade karbamatbaser har redan diskuterats på annat håll. Frågan är vad som gör röda cellers hemoglobin så speciellt, och hur förändras detta när hemoglobin syresätts?
För att sammanfatta:
- CO2 binder till oladdade N-terminala α-aminogrupper på både α- och β-subenheter av hemoglobin
- Oxygenering av hemjärnatomen i en hemoglobinmolekyl är en heterotrop allosterisk modulerare av dessa CO2-bindningsställen eftersom den introducerar en konformationsförändring i hemoglobintetramern (positiv kooperativitet)
- Som ett resultat av denna allosteriska modulering, CO2 har en högre affinitet för det syrefria T-tillståndet än för R-tillståndet
- Denna mekanism bidrar med 70 % av den totala CO2-transporten på grund av Haldane-effekten (Roughton, 1964), och därmed med cirka 10-15 % av den totala transporten av CO2 i blodet.
Det räcker antagligen för myndighetsarbete, men om man verkligen vill dyka ner i det purgande träsket av fysiologiska detaljer, kommer Austen Riggs artikel från 1988 att fungera som en utmärkt utgångspunkt. Som nämnts ovan är ”effekten” inte begränsad till koldioxid, utan är snarare ett fenomen som också innebär att hemoglobin binder promiskuöst med olika andra jonarter. Det syrefria hemoglobinet är t.ex. en massiv hora för protoner. Att fullständigt syrefria en blodvolym (ned till en SaO2 på 0 %) suger upp tillräckligt många protoner för att öka volymens pH-värde med 0,03, enligt Nunns (s. 155 i den åttonde upplagan). Detta är ett bra sätt att övergå till nästa avsnitt:
Haldaneeffekt på grund av ökad buffring av hemoglobin
Ännu en sammanfattning:
- Varje hemoglobintetramermolekyl har 38 laddade histidinrester, av vilka fyra är knutna till hemgruppen.
- Dissociationskonstanten för var och en av dessa histidinrester påverkas av syresättningen av hem
- Som ett resultat av detta blir hemoglobintetrameren som helhet mer basisk när hem förlorar syre.
- Detta tar bort vätejoner från lösningen (dvs. buffrar lösningen)
- Den effekt detta har på jämvikten mellan bikarbonat och kolsyra gynnar omvandlingen av kolsyra till bikarbonat
- Därmed ökar förlusten av syre från hemoglobintetramern, genom buffring, mängden koldioxid som transporteras i form av bikarbonat
Detta bidrar troligen endast till cirka 30 % av Haldaneeffekten. Den bidrar också till pH-ändringen i venöst blod. Veneriskt blod skulle normalt vara ganska surt på grund av närvaron av extra koldioxid (6 mm Hg mer än arteriellt blod), men den buffrande effekten av syrefritt hemoglobin återställer pH-värdet närmare det normala, så mycket att vissa hävdar att venösa prover säkert kan ersätta arteriella prover för mätning av pH hos ED-patienter.
Konsekvenser av Haldane-effekten för total koldioxidtransport
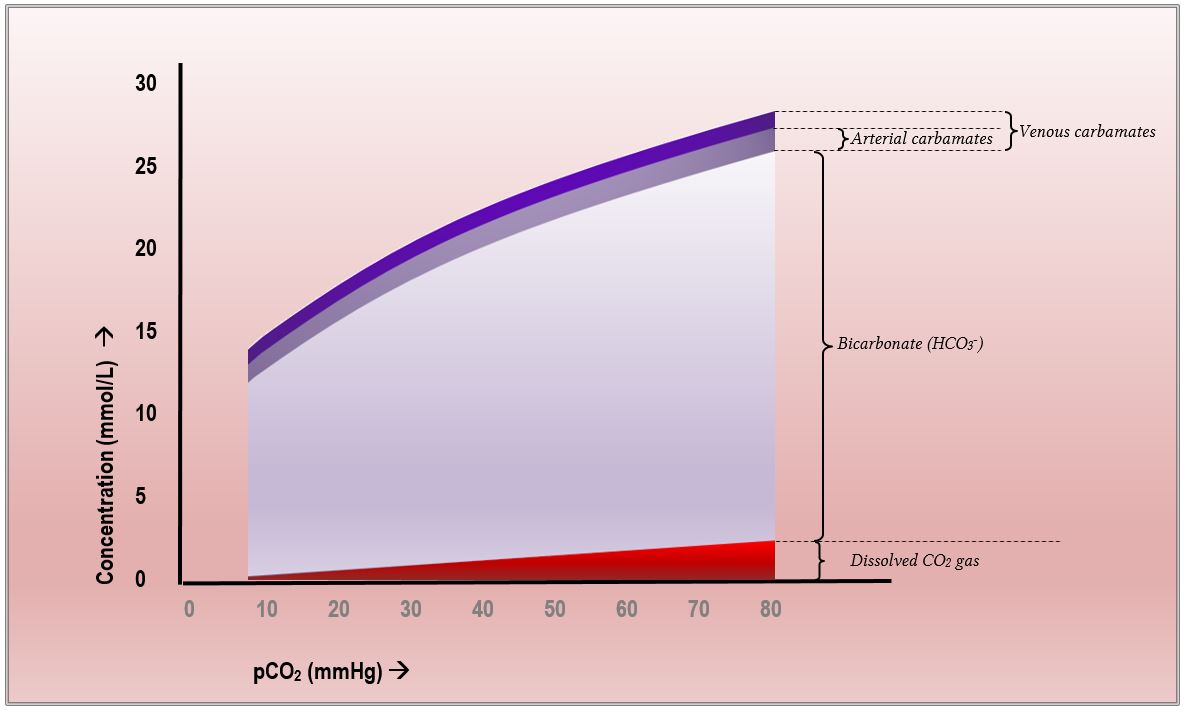
Även här tvingas man titta på detta diagram över koldioxidens dissociationskurva.
Observera att det finns en skillnad mellan den arteriella och venösa karbamathalten. Skillnaden förblir dock ganska stabil längs kontinuumet från 10 mmHg till 80 mmHg CO2. Det är som om det faktiska PaCO2 inte spelar någon roll. Så är faktiskt fallet: skillnaden mellan arteriell och venös karbamattransport av CO2 beror enbart på skillnaden i syresättningsgrad av hemoglobin. Ibland förväntas man identifiera den ”arteriella punkten” och den ”venösa punkten” på dessa kurvor, som illustrerar hur Haldane-effekten bidrar till den (lilla) skillnaden i total CO2-halt mellan arteriellt och blandat venöst blod. Kort sagt, även om den totala skillnaden är liten är Haldane-effekten ansvarig för mer än en tredjedel av den.

För att titta lite närmare på dessa:

Detta diagram, som är vanligt förekommande i läroböcker, illustrerar att om blodets syrgasmättnad ökas, så kommer också koldioxidens partialtryck att öka, eftersom mer koldioxid frigörs från sina bundna platser. Om blandat venöst blod (SpO2 = 75 %) skulle bli fullständigt syresatt skulle PaCO2 öka från 40 till 46 mmHg. Samtidigt skulle den totala CO2-halten förbli densamma. Om man förlänger linjen ytterligare till höger kan man konstatera att om blandat venöst blod på något sätt skulle bli fullständigt syresatt utan att dess CO2-innehåll förändras, skulle PaCO2 öka från 46 mmHg till cirka 55 mmHg.
Om man var uppmärksam skulle man kunna notera att detta fenomen, om det skulle bidra på ett användbart sätt till andningen, borde utspela sig över mycket små tidsperioder, som i stort sett motsvarar den tid som de röda blodkropparna spenderar i kapillärerna. Om det tog längre tid än så skulle man bara få en koldioxidberikad arteriell cirkulation av allt detta. Lyckligtvis, som den lätt färgade grafen från Klocke (1973) visar, sker hela processen på tiondels sekunder:
.jpg)