Begreppet godartad prostatahyperplasi (BPH) har nyligen införts i vår omgivning, vilket innebär att andra termer, som t.ex. den allmänt använda termen prostataadenom, har lämnats åt sidan. Detta är inte bara en ändring av nomenklaturen, utan snarare ett koncept som integrerar de tre aspekter ur vilka den vanligaste prostatasjukdomen (40 % av männen över 50 år) kan betraktas. Författaren tar upp diagnos och behandling av BPH, eftersom det är de två aspekter som kan vara av störst intresse för farmaceuten.
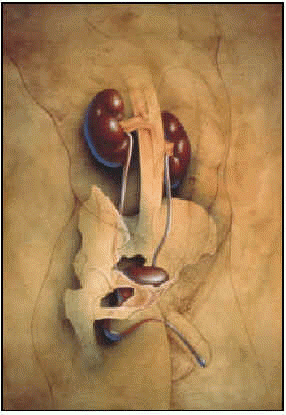
Prostatan är ett udda, extraperitonealt organ som är beläget i bäckenrummet. Namnet kommer från grekiskan och betyder ”den som är placerad nedanför”, eftersom den ligger precis under blåsans hals och omsluter urinröret. Den fick detta namn av Herophilus 300 f.Kr. Den utvecklas med åldern och når sin mognad i puberteten. Dess funktion är i huvudsak sexuell och deltar i bildandet av sädesvätska och sammandragning vid utlösning.
Den normala prostatan är ett muskuloglandulärt organ: 30 % är muskelmassa, belägen i den främre delen, och resten är körtel, belägen i den bakre och laterala delen.
PH är ett resultat av en icke-cancerartad tillväxt av vävnaden som bildar prostatan. Orsakerna är inte kända, men det verkar vara relaterat till hormonella förändringar som sker i samband med åldrandet. Vid 60 års ålder har hälften av den manliga befolkningen redan mikroskopiska tecken på BPH och vid 70 års ålder har mer än 40 % av männen en förstorad prostata som kan upptäckas genom undersökning. Den normala storleken på prostatan är ungefär lika stor som en kastanj. Vid 40 års ålder kan den vara lika stor som en aprikos och vid 60 års ålder kan den vara lika stor som en citron.
Prostataförstoringen är kopplad till det histologiska begreppet av sjukdomen, men det finns mycket förstorade prostata som uppträder utan obstruktion och utan symtom (och vice versa). Symptomen på denna sjukdom är ospecifika och kan förekomma i samband med många andra urologiska tillstånd. Det innebär att det kan finnas patienter med symtom och prostataförstoring eller med prostataförstoring utan symtom, eller båda, och i båda fallen kan det finnas hinder för urinflödet eller inte (fig. 1).

Fig. Hald-modellen: a) utvidgning och symtom utan hinder, b) symtom och hinder utan utvidgning, c) utvidgning och hinder utan symtom, d) utvidgning, symtom och hinder.
BPH är en av de vanligaste sjukdomarna hos äldre män. Det påverkar vanligtvis inte den sexuella funktionen, men den förstorade körteln orsakar tryck på urinblåsan och urinröret, vilket försvårar urinflödet. Urinering börjar med svårighet, i form av små droppar. Det finns också ofta ett behov av att kissa oftare och det kan finnas ett akut behov av att kissa. Många män måste gå upp flera gånger under natten för att kissa, andra har en obekväm känsla eftersom blåsan aldrig töms helt. Att tvinga blåsan att tömma sig kan förvärra situationen: blåsan drar ihop sig, blåsans väggar blir tjockare och förlorar sin elasticitet och blåsans muskler blir mindre effektiva. Urinansamling i urinblåsan kan ge upphov till urinvägsinfektioner, och försök att tvinga urinströmmen kommer bara att ge uppåtriktat tryck, vilket till slut kan skada njurarna.
En fullständig blockering av urinröret är en medicinsk nödsituation som kräver omedelbar kateterisering. Andra möjliga komplikationer till BPH är blåssten och blödning.
Diagnos
Trots bristen på kunskap om BPH:s naturliga historia och patogenes är det uppenbart att ett ökande antal läkarkonsultationer görs på grund av problem som uppstår på grund av tumörtillväxt i prostatan.
Under de senaste åren har nya terapeutiska metoder dykt upp, vilket har resulterat i en förändring av standardbehandlingen av symtomgivande BPH, och kirurgi har förpassats till en sekundär roll. Därför är det mycket viktigt att diagnostisera denna patologi och fastställa de parametrar som gör det möjligt att göra en korrekt bedömning av patienten för att sedan fastställa de terapeutiska indikationerna för BPH.
Traditionellt har symtomen på BPH delats in i två klasser, obstruktiva symtom och irriterande symtom (tabell 1). De förstnämnda beror på förekomsten av infravesikal obstruktion och de sistnämnda orsakas oftast av detrusorinstabilitet. Nästan tre fjärdedelar av männen med BPH har blandade symtom.

Förekomsten av symtom i allmänna befolkningsundersökningar hänger samman med ålder och åldern för symtomen vid det första besöket, vilket varierar mellan olika studier. Däremot verkar den kliniska betydelsen inte vara relaterad till den faktiska prostatastorleken. Patienter med allvarliga symtom på blåsobstruktion kan ha en liten prostata och andra personer utan kliniska symtom kan ha en stor prostata. Eftersom det är svårt att kvantifiera miktionssymtomen vid prostatism är det därför nödvändigt att använda ett antal poängsystem för att bedöma symtomens svårighetsgrad. Det finns olika frågeformulär, men det mest accepterade är den sju frågor långa symptomskattningsskalan, som av konsensuskommittén för BPH och med stöd av WHO (Paris, 1991) benämns International Prostatic Symptom Score (IPSS). En fråga om livskvalitet har lagts till i frågeformuläret (tabell 2).

Som vid alla andra sjukdomstillstånd är anamnesen viktig för att fastställa en misstänkt diagnos. På grundval av uppgifterna från anamnesen kan andra patologier med symtom som liknar BPH uteslutas (tabell 3). Därefter görs en allmän och lokal fysisk undersökning för att utvärdera prostatan och eventuella komplikationer. Det är viktigt att utföra bukpalpation för att upptäcka betydande resturinvolymer och naturligtvis en rektalundersökning. Rektalundersökning används för att bedöma prostatans morfologi och konsistens och samtidigt utvärdera tonen i analsfinktern för att upptäcka neurologiska förändringar, och av samma anledning är det nödvändigt att observera bulbocavernosusreflexen. Enbart genom beröring kan man dock inte göra en exakt bedömning av prostatans storlek, vikt eller grad av obstruktion. Därför kommer studien att fortsätta med en serie kompletterande undersökningar som inkluderar urinanalys (med pipstick eller odling) för att utesluta en eventuell urininfektion, bestämning av PSA-värde, bedömning av njurfunktionen och ultraljudsundersökning (transrektal och abdominell). Renovesikalt ultraljud hjälper till att utesluta eventuella komplikationer (urinlithiasis, divertiklar i urinblåsan, dilatation av urinvägarna, tumörer i njurarna eller blåsan) och att kvantifiera restmängden efter urinen. Suprapubiskt ultraljud är en enkel metod som inte har några kontraindikationer eller risker och som gör det möjligt att uppskatta prostatavolymen och morfologin ganska exakt. Transrektalt ultraljud är dock mycket noggrannare och rekommenderas därför för detta ändamål.


PSA är ett glykoprotein med en molekylvikt på mellan 33 000 och 34 000 Da som produceras i epitelet av prostataceller. Det finns i höga koncentrationer i spermaplasma, där det är inblandat i upplösningen av spermaklumpen som bildas efter utlösning. Den normala serumkoncentrationen av PSA hos unga friska män är mycket låg och ökar med åldern. Traditionellt accepteras PSA-värden mellan 0 och 4 ng/ml som normala. Förekomst av högre värden än normalt i serum tyder på förekomst av prostatapatologi. PSA är dock långt ifrån den ”perfekta” tumörmarkören, eftersom det också har upptäckts (om än i låga koncentrationer) i andra vävnader än prostatavävnad. Dessutom kan den inte heller betraktas som en specifik markör för cancer, eftersom den också är förhöjd vid BPH. Hos dessa patienter har man funnit att värdena är högre med större prostatavolym eller vid förekomst av komplikationer till följd av BPH. Ett tröskelvärde på 10 ng/ml har föreslagits för att skilja BPH från prostatacancer, men 10 % av personerna med BPH har högre PSA-värden. Därför har flera studier genomförts för att upptäcka former av PSA som skulle öka testets specificitet.
För närvarande rekommenderar American Cancer Society och American Urological Association årlig PSA-testning och digital rektalundersökning för män över 50 år som screeningmetoder för prostatacancer. Vissa författare anser att screening under 50 års ålder endast är tillrådligt för personer med hög risk för prostatacancer på grund av en familjehistoria av cancer. I det här fallet börjar studien vid 40 års ålder. De anser inte heller att screening är motiverat för män över 70 år, utom för dem som har en förväntad livslängd på mer än 10 år.
Med alla uppgifter som erhålls genom de olika testerna (tabell 4) kan vi fastställa en korrekt diagnos och bestämma den lämpligaste behandlingen för varje enskilt fall.

Terapier
Det huvudsakliga terapeutiska målet är, som i alla behandlingar, att uppnå ett gynnsamt förhållande mellan nytta och biverkningar. Därför delas patienter med BPH in i tre grupper: milda, måttliga och svåra.
Den milda gruppen omfattar patienter med symtom kvantifierade genom IPSS-frågeformuläret på mindre än 8, med liten påverkan på livskvaliteten och utan obstruktiva tecken; den måttliga BPH-undergruppen motsvarar patienter med IPSS 8-10, med eller utan en viss grad av obstruktion, och kan ha en påverkan på livskvaliteten. Gruppen med svår BPH är de som har ett IPSS över 19 och/eller tecken på obstruktion, med stor påverkan på livskvaliteten.
Behandlingsstrategin kommer därför att bero på symtomens svårighetsgrad och graden av obstruktion. Patienter med svåra symtom (IPSS > 20) och/eller komplikationer till följd av obstruktionen (njursvikt, urinretention, blåslitiasis, återkommande urinvägsinfektioner, hematuri, residus efter urinen större än 300 ml eller divertiklar i urinblåsan) kommer att kräva kirurgisk behandling. Patienter med milda symtom och små besvär kan hanteras väntande, medan patienter med måttliga symtom eller dåligt tolererade milda symtom bör hanteras medicinskt.
En schematisk bild av behandlingsstrategin för BPH visas i figur 2.

Figur 2. Behandlingsstrategi för BPH (källa: Bobé F, et al. Treatment of benign prostatic hyperplasia).
Farmakologisk behandling
Tre grupper av läkemedel finns för närvarande tillgängliga för behandling av BPH: alfablockerare (doxazosin, terazosin, alfuzosin, tamsulosin), 5-alpha-reduktashämmare (finasterid) och fytoterapi (tabell 5).

Alfablockerare
Virker genom att blockera alfa-1-receptorer i muskelfibrerna i blåshalsen och prostatavävnaden med åtföljande avslappning, vilket leder till minskat motstånd mot urinflödet utan att det påverkar detrusorkontraktiliteten negativt. Deras roll bygger alltså på att minska den dynamiska komponenten av prostataobstruktion. Alfablockerare minskar den sympatiska tonen i blåshals- och prostatamuskulaturen, förbättrar symtomen och det högsta urinflödet utan att ändra prostatastorleken.
Selektiva alfablockerare kan öka urinflödet och förbättra symtomen på 2-3 veckor, vilket gör dem till ett förstahandsval i behandlingen. Dessa inkluderar selektiva alfa-1-receptorblockerare, med färre oönskade effekter eftersom de inte blockerar glattmuskelreceptorer på andra ställen. Till denna grupp hör prazosin, alfuzosin, terazosin och doxazosin. En nyare alfablockerare är tamsulosin som har färre biverkningar.
De viktigaste alfablockerarna som används för behandling av BPH är:
Prazosin. Det användes ursprungligen för behandling av högt blodtryck, men används för närvarande inte för behandling av BPH eftersom det har större biverkningar än de andra läkemedlen i denna grupp.
Terazosin. En av de mest studerade blockerarna. Den rekommenderade dosen är 5 mg/dag och måste administreras i progressiva doser med början vid 1 mg/dag i 4 veckor för att minimera risken för ortostatisk hypotension. När det gäller blodtrycket ger det kliniskt obetydliga förändringar hos normotensiva patienter och hypotensiva effekter hos hypertensiva patienter, vilket gör det till ett bra terapeutiskt alternativ för patienter med båda sjukdomarna.
Doxazosin. Används även till patienter med högt blodtryck. Ursprungligen skulle det påbörjas successivt, men det finns nu en ny 4 mg formulering med långvarig frisättning där den aktiva substansen finns i en absorberbar tablett som inte kan tas upp i magen. Detta möjliggör en daglig dosering på 4 mg från den första dosen. Studier med doser på 8 mg/dag har visat signifikant ytterligare symtomförbättring.
173; Tamsulosin. Det är en selektiv alfa-1-blockerare och är därför det första ”uroselektiva” preparatet i sin grupp. Den lägre affiniteten för alfa-1B-receptorerna i blodkärlen ger en högre kardiovaskulär säkerhet. Dosen är fast, 0,4 mg/dag utan behov av progressiva ökningar, och det verkar som om symtomförbättring kan uppnås tidigare.
Och även om det terapeutiska svaret på alfablockerare som grupp är snabbt och dosberoende, finns det inga studier som visar att de förhindrar sjukdomsprogression, utveckling av komplikationer eller att de minskar behovet av slutgiltig kirurgisk behandling.
Biverkningarna av denna farmakologiska grupp är huvudvärk, asteni, somnolens, illamående, nästäppa, svindelkänsla och ortostatisk hypotoni, som tolereras sämst, även om den oönskade uppfattningen kan minskas genom att börja med posologin i ökande doser på kvällen.
5-alfa-reduktashämmare
Detta är fallet med finasterid, som inducerar en regression av prostataförstoring och ökar det maximala urinflödet, vilket förbättrar patientens symtom. Som biverkningar har finasterid långvariga återverkningar (minst 6 månader) och orsakar störningar i den sexuella funktionen (minskad libido, ejakulatorisk dysfunktion och impotens och andra såsom gynekomasti, ökad bröstkänslighet och hudutslag) och sänker PSA-värdena i serum (50 %) utan att förändra andelen fritt PSA.
Resultaten av kliniska prövningar visar efter två år en klinisk förbättring med signifikanta skillnader jämfört med placebo och en lägre förekomst av urinretention och prostatakirurgi i den grupp som behandlades med finasterid. Resultaten från en annan studie visar att svaret bibehålls över tid. Efter fyra år har det alltså inte bara skett en minskning av symptomatiska index och prostatavolym och en ökning av toppflödet (med statistiskt signifikanta skillnader i alla fall), utan också en lägre andel prostatakirurgi (10 vs. 5 %) och urinretention (7 vs. 3 %), vilket innebär en minskning av risken för kirurgi med finasterid med 55 respektive 57 % (PLESS-studien). Totalt sett kommer 13 % av placebopatienterna och 7 % av de finasteridbehandlade patienterna att behöva opereras eller kateteriseras för akut urinretention, med en faktisk fördel hos 6 % av patienterna.
Större prostata reagerar mer gynnsamt på behandling som syftar till att minska storleken på den, vilket bekräftas av resultaten av en metaanalys av 6 kliniska studier. Prostatavolymen i utgångsläget är därför en prediktiv faktor för behandlingssvaret, och finasterid är särskilt effektivt för stora prostatavolymer (mer än 40 ml). Omvänt måste patienter med liten prostata betraktas som dåliga första kandidater för behandling med detta läkemedel. Variationen i svar på finasteridbehandling kan inte förklaras enbart av prostatastorleken utan kan återspegla sjukdomens heterogena karaktär. Å andra sidan, och oberoende av varandra, rekommenderar klinikern finasteridbehandling som den bästa behandlingen för patienter med återkommande grov hematuri sekundärt till BPH.
Fytoterapi
Fytoterapeutisk behandling består av applicering av växtextrakt (Pygeum africanum, Serenoa repens). Deras verkningsmekanism är inte känd, men i vissa studier antas de ha en bättre effekt än placebo och till och med ge urodynamiska förbättringar. S. repens verkar verka på prostaglandinmetabolismen i prostatacellkulturer och modulerar även mänskligt 5-alfa-reduktas, varför det har utvärderats i en randomiserad studie mot finasterid i 1.098 patienter, som visade liknande effektivitet och brist på korrelation mellan symtomintensitet och prostatastorlek.
De har få biverkningar och representerar en låg ekonomisk kostnad.
Kirurgisk behandling
Transuretral resektion av prostatan är den vanligaste kirurgiska behandlingen av BPH. Det är en effektiv, men inte perfekt behandling. Ungefär 20 % av de patienter som genomgår en operation är missnöjda med det långsiktiga resultatet av ingreppet. Komplikationer inkluderar 70 % retrograda ejakulanter, impotens hos 5 %, postoperativa urinvägsinfektioner hos 5 % och en varierande grad av inkontinens hos 3 % av patienterna, samt kvarstående symtom hos en varierande procentandel av patienterna beroende på urvalskriterierna.
Därmed bör kirurgisk indikation fastställas hos de patienter vars symtom faktiskt kommer att förbättras. För tidiga ingrepp bör inte göras, men å andra sidan bör de inte fördröjas hos patienter med allvarlig obstruktion där försämringen av detrusorerna kommer att leda till att de irriterande symtomen kvarstår trots att prostataobstruktionen har lösts.
Det finns ett antal absoluta kirurgiska indikationer såsom återkommande urinretention, återkommande urinvägsinfektioner, utveckling av obstruktiv uropati i de övre urinvägarna och allvarlig hematuri.
Minimalt invasiva terapier (tabell 6) kan förbättra urinflödet till obstruerade värden, även om de alltid är lägre än de värden som erhålls genom transuretral resektion eller öppen adenotomi. De är dock ett giltigt behandlingsalternativ för patienter med allvarligt försämrat allmäntillstånd som erbjuds ett alternativ till permanent kateterisering och där konventionell kirurgi skulle innebära en betydande kirurgisk risk.

Allmänt innehåll i bibliografin
Baile A, Asua J, Albisu A. Benign prostatahyperplasi. Variationer i praxis och evidensbaserade riktlinjer. Atención Primaria 1999;23(3):142-50.
Berkow R, Fletcher AJ, et al. The Merck manual. Barcelona: Doyma, 1989;1808-9.
Bobé F, et al. Behandling av godartad prostatahyperplasi. FMC 2002;9(4): 290-9.
Giménez Serrano S. Pathologies of the prostate. Farmacia Profesional 2003;17(1):39-43.
Orejas V. Current aspects in the diagnosis of benign prostatic hyperplasia. Jano 2001;60(1375):78-82.
Ribal MJ, Alcaraz A. Daglig konsultation. Vad skulle du göra med benign prostatahyperplasi? Medicina Integral 2000;35(07):302-7.
Sebastián L. Prostataadenom. Nuvarande status. Jano 1999;56(1305):57-63.
Vela R. Benign prostatahyperplasi, en medicinsk-kirurgisk patologi? Jano 2001;61(1395):38-41.