Triacylglycerid/fosfolipid Stereokemi
Glycerol är en achiral molekyl, eftersom C2 har två identiska substituenter, -CH2OH. Glycerol i kroppen kan kemiskt omvandlas till triacylglycerider och fosfolipider (PL) som är chirala och som finns i en enantiomerisk form. Hur kan detta vara möjligt om de två CH2OH-grupperna på glycerol är identiska? Det visar sig att även om dessa grupper är stereokemiskt likvärdiga kan vi skilja dem åt på följande sätt. Orientera glycerol så att OH-gruppen på C2 pekar åt vänster. Ersätt sedan OH på C1 med OD, där D är deuterium. Nu är de två alkoholsubstituenterna på C1 och C3 inte identiska och den resulterande molekylen är kiral. Genom att rotera molekylen så att H på C2 pekar bakåt och genom att prioritera de andra substituenterna på C2 på följande sätt: OH =1, DOCH2 =2 och CH2OH = 3, kan man se att den resulterande molekylen är i S-konfiguration. Därför säger vi att C1 är proS-kol. På samma sätt, om vi ersätter OH på C3 med OD, kommer vi att bilda R-enantiomeren. C3 är alltså proR-kol. Detta visar att vi i verkligheten kan skilja mellan de två identiska CH2OH-substituenterna. Vi säger att glycerol inte är chiral, utan prochiral. (Tänk dig detta som att glycerol har potential att bli kiral genom att ändra en av två identiska substituenter.)
Figur: Glycerol – en prochiral molekyl
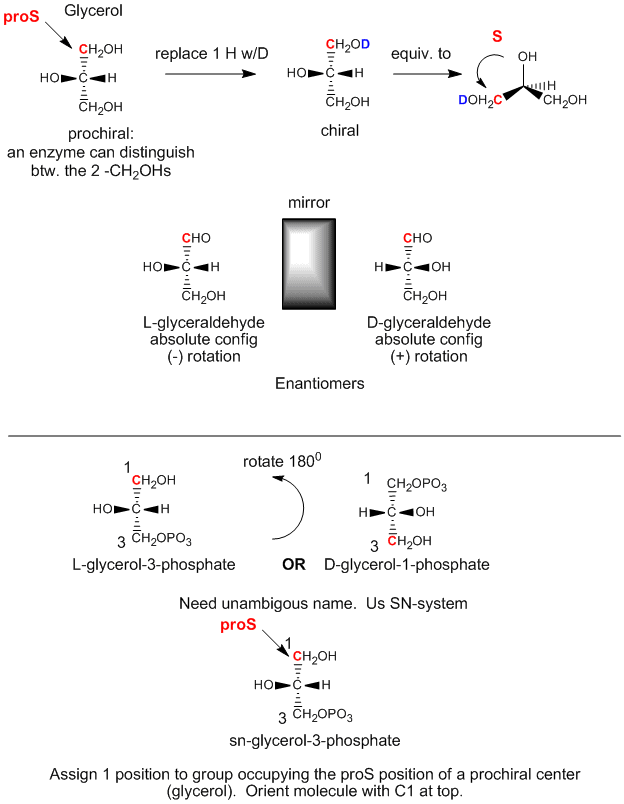
Vi kan relatera konfigurationen av glycerol ovan (när OH på C2 pekar åt vänster) till den absoluta konfigurationen av L-glyceraldehyd, ett enkelt socker (en polyhydroxyaldehyd eller keton), ett annat 3C-glycerolderivat. Denna molekyl är kiral med OH på C2 (det enda kirala kolet) pekande åt vänster. Det är lätt att komma ihåg att alla L-socker har OH på det sista chirala kolet som pekar åt vänster. Enantiomeren (spegelbildsisomeren) av L-glyceraldehyd är D-glyeraldehyd, där OH på C2 pekar åt höger. Biokemister använder L och D för stereokemi av lipider, socker och aminosyror, i stället för den R,S-nomenklatur som du använde i organisk kemi. Den stereokemiska beteckningen för alla sockerarter, aminosyror och glycerolipider kan bestämmas utifrån den absoluta konfigurationen av L- och D-glyceraldehyd.
Det första steget i in vivo-syntesen (i kroppen) av kirala derivat från den achirala glycerolen innebär fosforylering av OH på C3 med hjälp av ATP (en fosfoanhydrid som till sin struktur liknar ättiksyraanhydrid, ett utmärkt acetyleringsmedel) för att producera den kirala molekylen glycerolfosfat. Om man utgår från den absoluta konfigurationen av L-glyceraldehyd och använder den för att rita glycerol (med OH på C2 pekande åt vänster) kan man se att den fosforylerade molekylen kan benämnas L-glycerol-3-fosfat. Genom att rotera denna molekyl 180 grader, utan att ändra molekylens stereokemi, ändrar vi dock inte molekylen alls, utan med hjälp av D/L-nomenklaturen ovan skulle vi benämna den roterade molekylen som D-glycerol-1-fosfat. Vi kan inte ge samma molekyl två olika namn. Därför har biokemister utvecklat det stereospecifika numreringssystemet (sn), som tilldelar 1-positionen i en prochiral molekyl till den grupp som upptar proS-positionen. Med hjälp av denna nomenklatur kan vi se att den chirala molekyl som beskrivs ovan, glycerolfosfat, otvetydigt kan benämnas sn-glycerol-3-fosfat. Hydroxylsubstituenten på proR-karbonet fosforylerades.
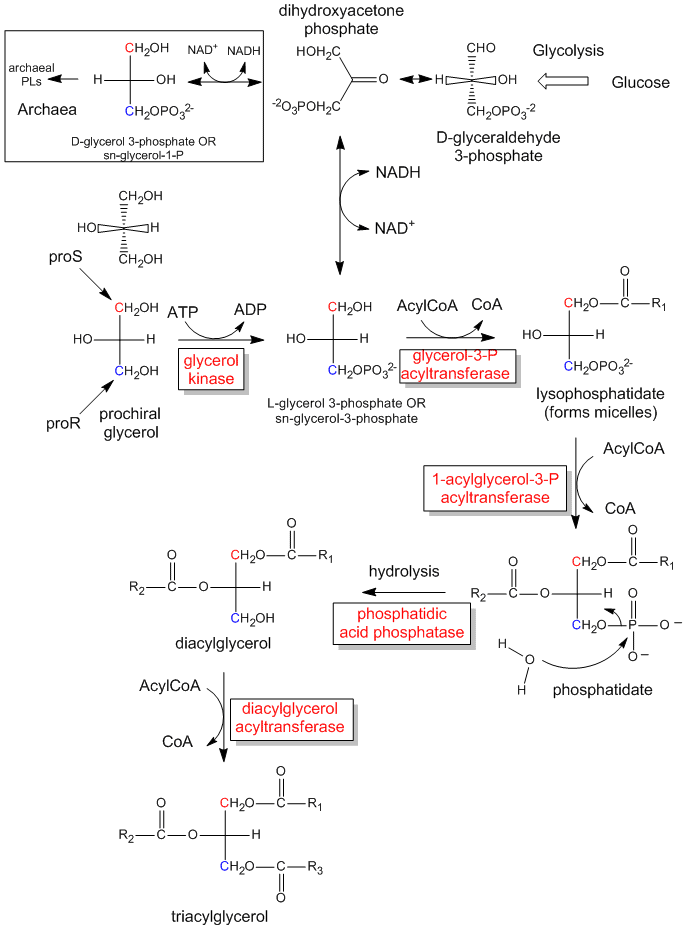
Figur: Den biologiska syntesen av triacylglycerider och fosfatidsyra från prochiral glycerol
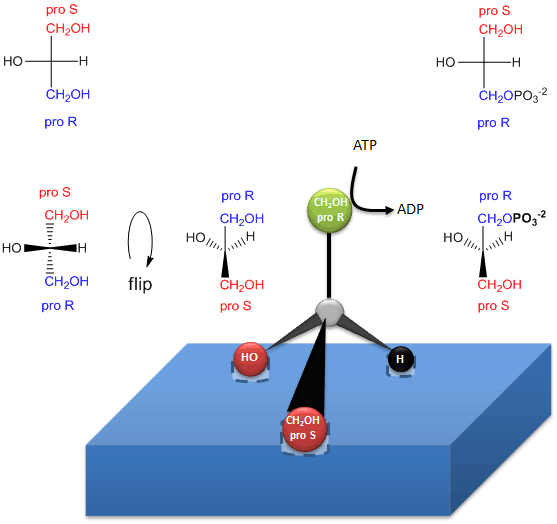
Den enzymatiska fosforyleringen av prochiral glycerol på OH på proR-kolet för att bilda sn-glycerol-3-fosfat illustreras i länken nedan. Eftersom vi kunde särskilja de två identiska CH2OH-substituenterna som innehållande antingen proS- eller proR-kolonnerna, kan enzymet också göra det. Enzymet kan skilja identiska substituenter på en prochiral molekyl om den prochirala molekylen interagerar med enzymet på tre punkter. Ett annat exempel på ett system med prochirala reaktanter/enzym är oxideringen av den prochirala molekylen etanol med enzymet alkoholdehydrogenas, där endast proR H av de två H:na på C2 avlägsnas. (Vi kommer att diskutera detta senare.)
Figur: Hur ett enzym (glycerolkinas) överför en PO4 från ATP till proR CH2OH av glycerol vid bildning av chirala triacylglyceroler och fosfatidsyra.