Denumire generică: clorhidrat de loperamidă
Forma de dozare: capsule
Revizuit medical de Drugs.com. Ultima actualizare la 22 ianuarie 2021.
- Vizualizare
- Efecte secundare
- Dosare
- Profesional
- Interacțiuni
- Mai multe
- Descriere Imodium
- Imodium – Farmacologie clinică
- Indicații și mod de utilizare pentru Imodium
- Contraindicații
- Atenționări
- Atenționări
- Generale
- Informații pentru pacienți
- Interacțiuni medicamentoase
- Carcinogeneză, mutageneză, afectarea fertilității
- Fertilitate
- Categoria de fertilitate C
- Mame care alăptează
- Utilizare pediatrică
- Reacții adverse
- Date din studiile clinice
- Experiență după punerea pe piață
- Abuzul și dependența de medicamente
- Abuzul
- Dependență
- Supradozaj
- Dosare și mod de administrare a iodului
- Diarree acută
- Diarree cronică
- Copii sub 2 ani
- Vârstnici
- Insuficiență renală
- Insuficiență hepatică
- Cum se administrează Imodium
- Întrebări frecvente
- Mai multe despre Imodium (loperamidă)
- Resurse pentru consumatori
- Resurse pentru profesioniști
- Alte formulări
- Ghiduri de tratament conexe
Descriere Imodium
Imodium® (clorhidrat de loperamidă), 4-(p-clorofenil)-4-hidroxi-N,N-dimetil-a,a-difenil-1-piperidinbutiramidă monoclorhidrat, este un antidiareic sintetic pentru uz oral.
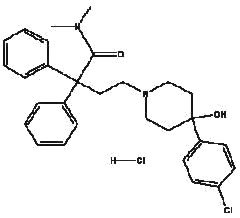
Imodium® este disponibil sub formă de capsule de 2 mg.
Ingredientele inactive sunt: Lactoză, amidon de porumb, talc și stearat de magneziu. Capsulele Imodium® conțin FD&C Yellow No. 6.
Imodium – Farmacologie clinică
Studiile in vitro și pe animale arată că Imodium® (clorhidrat de loperamidă) acționează prin încetinirea motilității intestinale și prin afectarea mișcării apei și a electroliților prin intestin. Loperamida se leagă de receptorul opiaceu din peretele intestinal. În consecință, aceasta inhibă eliberarea de acetilcolină și prostaglandine, reducând astfel peristaltismul și crescând timpul de tranzit intestinal. Loperamida crește tonusul sfincterului anal, reducând astfel incontinența și urgența.
La om, Imodium® prelungește timpul de tranzit al conținutului intestinal. Reduce volumul fecal zilnic, crește vâscozitatea și densitatea aparentă și diminuează pierderea de lichide și electroliți. Nu a fost observată toleranță la efectul antidiareic. Studiile clinice au indicat că timpul de înjumătățire aparent de eliminare a loperamidei la om este de 10,8 ore, cu un interval de 9,1 – 14,4 ore. Nivelurile plasmatice ale medicamentului neschimbat rămân sub 2 nanograme pe ml după administrarea unei capsule de 2 mg de Imodium®. Nivelurile plasmatice sunt cele mai ridicate la aproximativ cinci ore după administrarea capsulei și la 2,5 ore după administrarea lichidului. Nivelurile plasmatice maxime de loperamidă au fost similare pentru ambele formulări. Eliminarea loperamidei are loc în principal prin N-demetilare oxidativă. Se consideră că izozimele citocromului P450 (CYP450), CYP2C8 și CYP3A4, joacă un rol important în procesul de N-demetilare a loperamidei, deoarece quercetina (inhibitor al CYP2C8) și ketoconazolul (inhibitor al CYP3A4) au inhibat semnificativ procesul de N-demetilare in vitro cu 40% și, respectiv, 90%. În plus, CYP2B6 și CYP2D6 par să joace un rol minor în N-demetilarea loperamidei. Excreția loperamidei neschimbate și a metaboliților săi are loc în principal prin fecale. La acei pacienți la care au fost monitorizați parametrii biochimici și hematologici în timpul studiilor clinice, nu au fost observate tendințe spre anomalii în timpul tratamentului cu Imodium®. În mod similar, analizele de urină, EKG și examinările clinice oftalmologice nu au evidențiat tendințe spre anormalitate.
Indicații și mod de utilizare pentru Imodium
Imodium® (clorhidrat de loperamidă) este indicat pentru controlul și ameliorarea simptomatică a diareei acute nespecifice și a diareei cronice asociate cu boala inflamatorie intestinală. Imodium® este indicat, de asemenea, pentru reducerea volumului de secreție din ileostomii.
Contraindicații
Imodium este contraindicat la pacienții cu hipersensibilitate cunoscută la clorhidrat de loperamidă sau la oricare dintre excipienți.
Imodium este contraindicat la pacienții cu dureri abdominale în absența diareei.
Imodium nu este recomandat la sugarii cu vârsta sub 24 de luni.
Imodium nu trebuie utilizat ca terapie primară:
– la pacienții cu dizenterie acută, care se caracterizează prin sânge în scaune și febră mare, – la pacienții cu colită ulcerativă acută, – la pacienții cu enterocolită bacteriană cauzată de organisme invazive, inclusiv Salmonella, Shigella și Campylobacter, – la pacienții cu colită pseudomembranoasă asociată cu utilizarea de antibiotice cu spectru larg.
Atenționări
La pacienții care au diaree apare adesea o depleție de lichide și electroliți. În astfel de cazuri, administrarea de lichide și electroliți corespunzători este foarte importantă. Utilizarea Imodium® nu exclude necesitatea unei terapii adecvate cu lichide și electroliți.
În general, Imodium nu trebuie utilizat atunci când trebuie evitată inhibarea peristaltismului din cauza riscului posibil de sechele semnificative, inclusiv ileus, megacolon și megacolon toxic. Imodium trebuie întrerupt prompt atunci când apar constipație, distensie abdominală sau ileus.
Tratamentul diareei cu Imodium este doar simptomatic. Ori de câte ori se poate determina o etiologie subiacentă, trebuie administrat un tratament specific atunci când este adecvat (sau când este indicat).
Pacienților cu SIDA tratați cu Imodium pentru diaree trebuie să li se întrerupă tratamentul la primele semne de distensie abdominală. Au fost raportate cazuri izolate de megacolon toxic la pacienții cu SIDA cu colită infecțioasă atât de la agenți patogeni virali cât și bacterieni tratați cu clorhidrat de loperamidă.
Imodium® trebuie utilizat cu precauție specială la copiii mici din cauza variabilității mai mari a răspunsului la această grupă de vârstă. Deshidratarea, în special la copiii mai mici, poate influența și mai mult variabilitatea răspunsului la Imodium®.
Atenționări
Generale
Au fost raportate reacții alergice extrem de rare, inclusiv anafilaxie și șoc anafilactic. În diareea acută, dacă nu se observă o ameliorare clinică în 48 de ore, administrarea de Imodium® (clorhidrat de loperamidă) trebuie întreruptă și pacienții trebuie sfătuiți să se adreseze medicului lor. Deși nu sunt disponibile date farmacocinetice la pacienții cu insuficiență hepatică, Imodium trebuie utilizat cu prudență la acești pacienți din cauza metabolismului de prim pasaj redus. Pacienții cu disfuncție hepatică trebuie monitorizați îndeaproape pentru semne de toxicitate la nivelul SNC. Nu sunt disponibile date farmacocinetice la pacienții cu insuficiență renală. Deoarece s-a raportat că cea mai mare parte a medicamentului este metabolizată și metaboliții sau medicamentul neschimbat este excretat în principal în fecale, nu sunt necesare ajustări ale dozei la pacienții cu insuficiență renală. Nu au fost efectuate studii oficiale pentru a evalua farmacocinetica loperamidei la subiecții vârstnici. Cu toate acestea, în două studii care au inclus pacienți vârstnici, nu au existat diferențe majore în ceea ce privește dispoziția medicamentului la pacienții vârstnici cu diaree în raport cu pacienții tineri.
Informații pentru pacienți
Pacienții trebuie sfătuiți să se adreseze medicului dacă diareea nu se ameliorează în 48 de ore sau dacă observă sânge în scaune, dacă fac febră sau dacă prezintă distensie abdominală. În cadrul sindroamelor diareice tratate cu Imodium pot apărea stări de oboseală, amețeli sau somnolență. Prin urmare, se recomandă prudență atunci când conduceți o mașină sau folosiți utilaje. (vezi Reacții adverse).
Interacțiuni medicamentoase
Datele nonclinice au arătat că loperamida este un substrat al glicoproteinei P. Administrarea concomitentă de loperamidă (16 mg doză unică) cu o doză unică de 600 mg fie de chinidină, fie de ritonavir, ambele fiind inhibitori ai P-glicoproteinei, a dus la o creștere de 2 până la 3 ori a concentrațiilor plasmatice de loperamidă. Datorită potențialului de intensificare a efectelor centrale atunci când loperamida este coadministrată cu chinidină și cu ritonavir, trebuie să se manifeste prudență atunci când loperamida este administrată la dozele recomandate (2 mg, până la 16 mg doza zilnică maximă) cu inhibitori ai P-glicoproteinei.
Când o singură doză de 16 mg de loperamidă este coadministrată cu o doză unică de saquinavir de 600 mg, loperamida a scăzut expunerea la saquinavir cu 54%, ceea ce poate avea relevanță clinică datorită reducerii eficacității terapeutice a saquinavirului. Efectul saquinavirului asupra loperamidei are o semnificație clinică mai mică. Prin urmare, atunci când loperamida este administrată împreună cu saquinavirul, eficacitatea terapeutică a saquinavirului trebuie monitorizată îndeaproape.
Carcinogeneză, mutageneză, afectarea fertilității
Într-un studiu de 18 luni la șobolani cu doze orale de până la 40 mg/kg/zi (de 21 de ori doza maximă la om de 16 mg/zi, pe baza unei comparații a suprafeței corporale), nu au existat dovezi de carcinogeneză.
Loperamida nu a fost genotoxică în testul Ames, testul cromotestul SOS în E. coli, testul letal dominant la femelele de șoarece sau testul de transformare a celulelor embrionare de șoarece.
Fertilitatea și performanțele de reproducere au fost evaluate la șobolani folosind doze orale de 2,5, 10 și 40 mg/kg/zi (numai la femele) într-un al doilea studiu. Administrarea orală de 20 mg/kg/zi (aproximativ de 11 ori doza umană pe baza unei comparații a suprafeței corporale) și mai mare a produs o afectare puternică a fertilității femelelor. Tratarea șobolanilor femele cu până la 10 mg/kg/zi pe cale orală (aproximativ de 5 ori doza umană bazată pe o comparație a suprafeței corporale) nu a avut niciun efect asupra fertilității. Tratamentul șobolanilor masculi cu 40 mg/kg/zi pe cale orală (de aproximativ 21 de ori doza umană bazată pe o comparație a suprafeței corporale) a produs afectarea fertilității masculine, în timp ce administrarea unei doze de până la 10 mg/kg/zi (de aproximativ 5 ori doza umană bazată pe o comparație a suprafeței corporale) nu a avut niciun efect.
Fertilitate
Efecte teratogene
Categoria de fertilitate C
Studii teratologice au fost efectuate la șobolani folosind doze orale de 2,5, 10 și 40 mg/kg/zi și la iepuri folosind doze orale de 5, 20 și 40 mg/kg/zi. Aceste studii nu au evidențiat nicio dovadă de afectare a fertilității sau de vătămare a fătului la doze de până la 10 mg/kg/zi la șobolani (de 5 ori doza umană bazată pe compararea suprafeței corporale) și de 40 mg/kg/zi la iepuri (de 43 de ori doza umană bazată pe compararea suprafeței corporale). Tratamentul șobolanilor cu 40 mg/kg/zi pe cale orală (de 21 de ori doza umană bazată pe o comparație a suprafeței corporale) a produs o afectare marcată a fertilității. Studiile nu au produs nicio dovadă de activitate teratogenă. Nu există studii adecvate și bine controlate la femeile gravide. Loperamida trebuie utilizată în timpul sarcinii numai dacă beneficiul potențial justifică riscul potențial pentru făt.
Efecte nonteratogene
Într-un studiu de reproducere peri- și postnatală la șobolani, administrarea orală a 40 mg/kg/zi a produs afectarea creșterii și supraviețuirii descendenților.
Mame care alăptează
Cantități mici de loperamidă pot apărea în laptele matern uman. Prin urmare, Imodium nu este recomandat în timpul alăptării.
Utilizare pediatrică
Vezi secțiunea „Atenționări” pentru informații privind variabilitatea mai mare a răspunsului la această grupă de vârstă. În caz de supradozaj accidental de Imodium® de către copii, vezi secțiunea „Supradozaj” pentru tratamentul sugerat.
Reacții adverse
Date din studiile clinice
Efectele adverse raportate în timpul investigațiilor clinice cu Imodium® (clorhidrat de loperamidă) sunt dificil de distins de simptomele asociate cu sindromul diareic. Efectele adverse înregistrate în timpul studiilor clinice cu Imodium® au fost, în general, de natură minoră și autolimitată. Acestea au fost observate mai frecvent în timpul tratamentului diareei cronice.
Evenimentele adverse raportate sunt rezumate indiferent de evaluarea cauzalității de către investigatori.
1) Evenimente adverse din 4 studii controlate cu placebo la pacienții cu diaree acută
Evenimentele adverse cu o incidență de 1.0% sau mai mare, care au fost raportate cel puțin la fel de des la pacienții cu clorhidrat de loperamidă ca și la cei cu placebo, sunt prezentate în tabelul de mai jos.
| Diarree acută | ||
|---|---|---|
| Clorhidrat de loperamidă | Placebo | |
| Nr. de pacienți tratați | 231 | 236 |
| EA gastrointestinale% | ||
| Constipație | 2,6% | 0.8% |
Evenimentele adverse cu o incidență de 1,0% sau mai mare, care au fost raportate mai frecvent la pacienții care au primit placebo decât la cei care au primit clorhidrat de loperamidă, au fost: gură uscată, flatulență, crampe abdominale și colici.
2) Reacții adverse din 20 de studii controlate cu placebo la pacienții cu diaree cronică
Reacțiile adverse cu o incidență de 1,0% sau mai mare, care au fost raportate cel puțin la fel de des la pacienții care au primit clorhidrat de loperamidă ca și la cei care au primit placebo, sunt prezentate mai jos în tabelul de mai jos.
| Diarree cronică | |||
|---|---|---|---|
| Clorhidrat de loperamidă | Placebo | ||
| Nr. de pacienți tratați | 285 | 277 | |
| EA gastrointestinale% | |||
| Constipație | 5.3% | 0,0% | |
| Sistemul nervos central și periferic AE% | |||
| Vârtej | 1,4% | 0,7% | |
Evenimentele adverse cu o incidență de 1.0% sau mai mare, care au fost raportate mai frecvent la pacienții care au primit placebo decât la cei care au primit clorhidrat de loperamidă au fost: greață, vărsături, cefalee, meteorism, dureri abdominale, crampe abdominale și colici.
3) Reacții adverse din șaptezeci și șase de studii controlate și necontrolate la pacienții cu diaree acută sau cronică
Reacțiile adverse cu o incidență de 1.0% sau mai mare la pacienții din toate studiile sunt prezentate în tabelul de mai jos.
| Diarree acută | Diarree cronică | Toate studiile * | ||
|---|---|---|---|---|
| * Toți pacienții din toate studiile, inclusiv cele în care nu s-a specificat dacă evenimentele adverse au apărut la pacienții cu diaree acută sau cronică. | ||||
| Nr. de pacienți tratați | 1913 | 1371 | 3740 | |
| EAC gastro-intestinale% | ||||
| Nauzea | 0,7% | 3,2% | 1.8% | |
| Constipație | 1,6% | 1,9% | 1,7% | |
| Crampe abdominale | 0.5% | 3,0% | 1,4% | |
Experiență după punerea pe piață
Au fost raportate următoarele reacții adverse:
Dezordini ale pielii și ale țesutului subcutanat
Erupții cutanate, prurit, urticarie, angioedem și cazuri extrem de rare de erupții buloase, inclusiv eritem multiform, sindrom Stevens-Johnson și necroliză epidermică toxică au fost raportate la utilizarea Imodium
Dezordini ale sistemului imunitar
Au fost raportate apariții izolate de reacții alergice și, în unele cazuri, reacții severe de hipersensibilitate, inclusiv șoc anafilactic și reacții anafilactoide, la utilizarea Imodium.
Tulburări gastrointestinale
Gură uscată, dureri abdominale, distensie sau disconfort, greață, vărsături, flatulență, dispepsie, constipație, ileus paralitic, megacolon, inclusiv megacolon toxic (vezi contraindicații și atenționări).
Tulburări renale și urinare
Reținere urinară
Tulburări ale sistemului nervos
Somnolență, amețeală
Tulburări generale și afecțiuni ale locului de administrare
Cădere
O serie de reacții adverse raportate în timpul investigațiilor clinice și a experienței postcomercializare cu loperamidă sunt simptome frecvente ale sindromului diareic subiacent (durere/disconfort abdominal, greață, vărsături, uscăciune a gurii, oboseală, somnolență, amețeală, constipație și flatulență). Aceste simptome sunt adesea dificil de distins de efectele nedorite ale medicamentului.
Abuzul și dependența de medicamente
Abuzul
Un studiu clinic specific conceput pentru a evalua potențialul de abuz al loperamidei la doze mari a dus la constatarea unui potențial de abuz extrem de scăzut.
Dependență
Studii efectuate pe maimuțe dependente de morfină au demonstrat că clorhidratul de loperamidă în doze mai mari decât cele recomandate pentru om a prevenit semnele de sevraj la morfină. Cu toate acestea, la om, testul de provocare a pupilei cu naloxonă, care, atunci când este pozitiv, indică efecte asemănătoare opiaceelor, efectuat după o singură doză mare, sau după mai mult de doi ani de utilizare terapeutică a Imodium® (clorhidrat de loperamidă), a fost negativ. Imodium® (loperamidă formulată cu stearat de magneziu) administrat pe cale orală este atât foarte insolubil, cât și slab penetrat în SNC.
Supradozaj
În caz de supradozaj, (inclusiv supradozaj relativ datorat disfuncției hepatice), pot apărea retenție urinară, ileus paralitic și depresie a SNC. Copiii pot fi mai sensibili la efectele asupra SNC decât adulții. Studiile clinice au demonstrat că o suspensie de cărbune activat administrată imediat după ingestia de clorhidrat de loperamidă poate reduce de până la nouă ori cantitatea de medicament care este absorbită în circulația sistemică. Dacă vărsăturile apar spontan la ingestie, trebuie administrată pe cale orală o suspensie de 100 g de cărbune activat, de îndată ce lichidele pot fi reținute.
Dacă nu au apărut vărsături, trebuie efectuată o spălătură gastrică urmată de administrarea a 100 g de suspensie de cărbune activat prin sonda gastrică. În caz de supradozaj, pacienții trebuie monitorizați pentru semne de depresie a SNC timp de cel puțin 24 de ore.
Dacă apar simptome de supradozaj, se poate administra naloxonă ca antidot. În cazul în care răspunde la naloxonă, semnele vitale trebuie monitorizate cu atenție pentru depistarea reapariției simptomelor de supradozaj medicamentos timp de cel puțin 24 de ore după ultima doză de naloxonă.
Din cauza acțiunii prelungite a loperamidei și a duratei scurte (una până la trei ore) a naloxonei, pacientul trebuie monitorizat îndeaproape și tratat în mod repetat cu naloxonă, după cum este indicat. Deoarece relativ puțin medicament este excretat în urină, nu se așteaptă ca diureza forțată să fie eficientă în cazul supradozajului cu Imodium® (clorhidrat de loperamidă).
În studiile clinice, un adult care a luat trei doze de 20 mg într-o perioadă de 24 de ore a avut grețuri după a doua doză și a vomitat după a treia doză. În studiile concepute pentru a examina potențialul de reacții adverse, ingestia intenționată de până la 60 mg de clorhidrat de loperamidă într-o singură doză la subiecți sănătoși nu a avut ca rezultat efecte adverse semnificative.
Dosare și mod de administrare a iodului
(1 capsulă = 2 mg)
Pacienții trebuie să primească înlocuirea corespunzătoare a lichidelor și electroliților, după cum este necesar.
Diarree acută
Adulți: Doza inițială recomandată este de 4 mg (două capsule) urmată de 2 mg (o capsulă) după fiecare scaun neformat. Doza zilnică nu trebuie să depășească 16mg (opt capsule). Îmbunătățirea clinică se observă de obicei în 48 de ore.
Copii: La copiii cu vârsta cuprinsă între 2 și 5 ani (20 kg sau mai puțin), trebuie utilizată formula lichidă fără prescripție medicală (Imodium® A-D 1 mg/7,5 ml); pentru vârstele cuprinse între 6 și 12 ani, se poate utiliza fie Imodium® Capsule, fie Imodium® A-D Lichid. Pentru copiii cu vârste cuprinse între 2 și 12 ani, următorul program pentru capsule sau lichid va satisface de obicei cerințele inițiale de dozare:
Schema de dozare recomandată pentru prima zi
De la 2 la 5 ani: 1 mg t.i.d. (3 mg doză zilnică) (13-20 kg)
De la șase la opt ani: 2 mg b.i.d. (4 mg doză zilnică) (20-30 kg)
De la opt la doisprezece ani: 2 mg t.i.d. (3 mg doză zilnică). (6mg doză zilnică) (peste 30 kg)
Dosare zilnică ulterioară recomandată
După prima zi de tratament, se recomandă ca dozele ulterioare de Imodium® (1 mg/10 kg greutate corporală) să fie administrate numai după un scaun liber. Doza zilnică totală nu trebuie să depășească dozele recomandate pentru prima zi.
Diarree cronică
Copii: Deși Imodium® a fost studiat la un număr limitat de copii cu diaree cronică; doza terapeutică pentru tratamentul diareei cronice la o populație pediatrică nu a fost stabilită.
Adulți: Doza inițială recomandată este de 4 mg (două capsule) urmată de 2 mg (o capsulă) după fiecare scaun neformat până când diareea este controlată, după care doza de Imodium® trebuie redusă pentru a satisface cerințele individuale. Atunci când a fost stabilită doza zilnică optimă, această cantitate poate fi administrată ca doză unică sau în doze divizate.
Dosarea zilnică medie de întreținere în studiile clinice a fost de 4 până la 8 mg (două până la patru capsule). O doză de 16 mg (opt capsule) a fost rareori depășită. Dacă nu se observă o ameliorare clinică după tratamentul cu 16 mg pe zi timp de cel puțin 10 zile, este puțin probabil ca simptomele să fie controlate prin administrarea ulterioară. Administrarea Imodium® poate fi continuată dacă diareea nu poate fi controlată în mod adecvat prin dietă sau tratament specific.
Copii sub 2 ani
Nu se recomandă utilizarea Imodium la copii sub 2 ani. Au existat raportări rare de ileus paralitic asociat cu distensia abdominală. Cele mai multe dintre aceste raportări au apărut în contextul dizenteriei acute, supradozajului și la copii foarte mici, cu vârsta mai mică de 2 ani.
Vârstnici
Nu au fost efectuate studii farmacocinetice oficiale la subiecții vârstnici. Cu toate acestea, nu au fost raportate diferențe majore în ceea ce privește dispoziția medicamentului la pacienții vârstnici cu diaree în raport cu pacienții tineri. Nu este necesară ajustarea dozei la vârstnici.
Insuficiență renală
Nu sunt disponibile date farmacocinetice la pacienții cu insuficiență renală. Deoarece metaboliții și medicamentul neschimbat sunt excretați în principal în fecale, nu este necesară ajustarea dozei la pacienții cu insuficiență renală (vezi secțiunea PRECAUȚII).
Insuficiență hepatică
Deși nu sunt disponibile date farmacocinetice la pacienții cu insuficiență hepatică, Imodium trebuie utilizat cu prudență la acești pacienți din cauza metabolismului de prim pasaj redus. (vezi pct. Precauții).
Cum se administrează Imodium
Capsule – fiecare capsulă conține 2 mg de clorhidrat de loperamidă. Capsulele au un corp de culoare verde deschis și un capac de culoare verde închis cu inscripția „JANSSEN” pe un segment și „Imodium” pe celălalt segment. Capsulele Imodium® sunt furnizate în flacoane a câte 100.
NDC 50458-400-10
(100 CAPSULE)
Să se păstreze la 15°-25°C (59°-77°F).
Revizuit în septembrie 1996, iulie 1998, aprilie 2004
Aprobat în octombrie 2005
©Janssen Pharmaceutica Inc. 1998
Doar pentru prescripție medicală
Imprimat în SUA
U.S.A. Brevet 3, 714,159
| Imodium clorhidrat de loperamidă capsulă |
|||||||||||||||||||||||
|
|||||||||||||||||||||||
|
|||||||||||||||||||||||
|
|||||||||||||||||||||||
|
|||||||||||||||||||||||
|
|||||||||||||||||||||||
Etichetă – McNeil Consumer Healthcare
Întrebări frecvente
- Cum se oprește diareea – sugestii de medicamente sau remedii?
Mai multe despre Imodium (loperamidă)
- Efecte secundare
- În timpul sarcinii sau alăptării
- Dosare Informații
- Imagini ale medicamentelor
- Interacțiuni medicamentoase
- Comparați alternativele
- Grupul de suport
- 24 Recenzii
- Clasa de medicament: antidiareice
- Alerte FDA (2)
Resurse pentru consumatori
- Lectură avansată
Resurse pentru profesioniști
- Informații de prescriere
- Loperamidă soluție orală (FDA)
Alte mărci antidiareice, Up and Up Anti-Diarrheal Solution
Alte formulări
- Imodium A-D
Ghiduri de tratament conexe
- Diarreea, Acută
- Diarreea, cronică
- Diarreea călătorului
- Diarreea
Denunțare medicală
.