- Ce face ca o moleculă să fie polară?
- Vezi formula structurală a dioxidului de carbon:
- De ce este apa polară?
Apa este o moleculă polară deoarece oxigenul său este puternic electronegativ și, ca atare, atrage perechea de electroni spre sine (departe de cei doi atomi de hidrogen), dobândind astfel o sarcină ușor negativă.
Polaritatea unei molecule depinde nu numai de atomii care o compun, ci și de modul în care aceștia sunt dispuși în jurul atomului central, adică de dispunerea spațială a acestor atomi. Pentru a înțelege mai bine acest lucru, să discutăm subiectul mai în detaliu.
Ce face o moleculă polară?
Polaritatea unei molecule este legată de deplasarea electronilor într-o anumită direcție. Aceasta, la rândul ei, depinde de polaritatea legăturilor prezente în moleculă, deoarece aceste legături conțin, de asemenea, electroni.
În cadrul unei molecule, atomul cu cea mai mare putere de a atrage electronii spre el (de ex, este mai electronegativ decât celălalt atom) va căpăta o ușoară sarcină negativă pe el însuși, iar legătura dintre cei doi atomi va deveni polară.
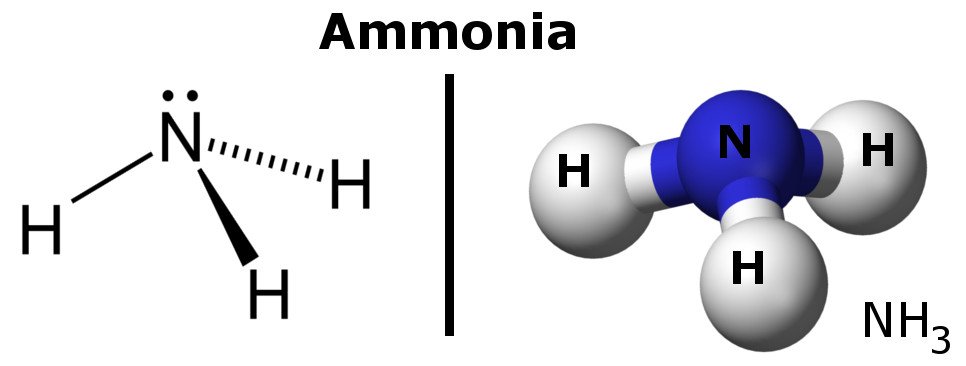
Amonia este o moleculă polară deoarece are regiuni cu ușoare sarcini negative și pozitive.
În concluzie, se poate spune că densitatea de electroni a unei legături polare se acumulează spre un capăt al legăturii, ceea ce face ca acel capăt să posede o ușoară sarcină negativă, în timp ce celălalt capăt are o ușoară sarcină pozitivă. Acest lucru face ca o moleculă să fie polară.
În mod similar, dacă o moleculă nu are regiuni de sarcină pozitivă și negativă, este considerată nepolară.
Cu toate acestea, un lucru interesant de remarcat este că, cu cât diferența de electronegativitate este mai mare, cu atât mai polară va fi legătura în cadrul unei molecule. Compușii carbonilici sunt polari deoarece carbonul carbonilic este ușor pozitiv. Astfel, dioxidul de carbon, care conține un carbon pozitiv și doi oxigeni parțial negativi, nu ar trebui să fie polar?
Ei bine, dioxidul de carbon este format din doi atomi de oxigen legați de un atom de carbon. Atomii de oxigen sunt mult mai electronegativi decât atomii de carbon și, ca atare, ar trebui să dețină o sarcină parțial negativă, în timp ce atomul de carbon ar trebui să fie ușor încărcat pozitiv. Cu toate acestea, destul de interesant, acest lucru nu se întâmplă.
Aruncați o privire la formula structurală a dioxidului de carbon:
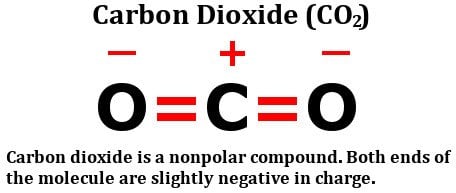
Este format din doi atomi de oxigen la fel de electronegativi, da, dar priviți cum sunt aranjați acești atomi în jurul atomului de carbon. Amândoi se află la unghiuri perfecte de 180 de grade față de carbon. În consecință, ei trag densitatea de electroni din carbon cu o forță egală în direcții opuse. Rezultatul net este că densitatea de electroni de pe atomul de carbon rămâne neafectată, ceea ce face ca molecula de dioxid de carbon să fie nepolară.
Dioxidul de carbon este un exemplu excelent al modului în care geometria unei molecule joacă un rol crucial în a determina dacă aceasta este polară sau nepolară. Acum, să ne uităm la o moleculă de apă:
De ce este apa polară?
Formula chimică a apei este H20, ceea ce înseamnă că ea conține doi atomi de hidrogen și un atom de oxigen. Atomii de hidrogen au doar un singur electron în învelișul lor, în timp ce atomul de oxigen are 6 electroni de valență.
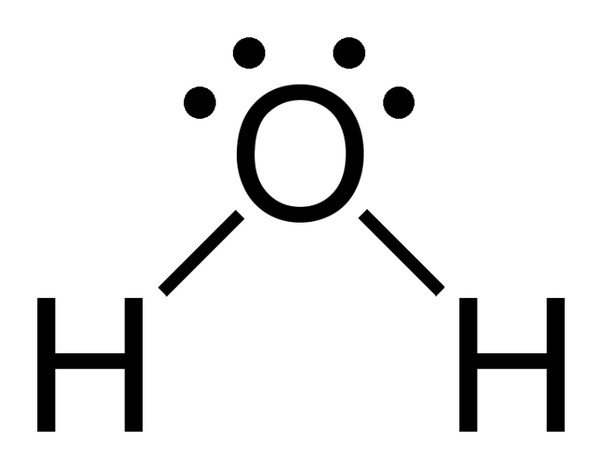
Rețineți cele 2 perechi de electroni solitari de pe atomul de oxigen din apă.
Din moment ce oxigenul are 6 electroni în învelișul său de valență, el împarte un electron cu fiecare atom de hidrogen. În acest fel, el rămâne cu 4 electroni nelegate în cei 2 orbitali ai săi. Aceste perechi de electroni legați și nelegate se aranjează într-o formă tetraedrică în jurul oxigenului, motiv pentru care cele două legături par a avea o formă curbată.
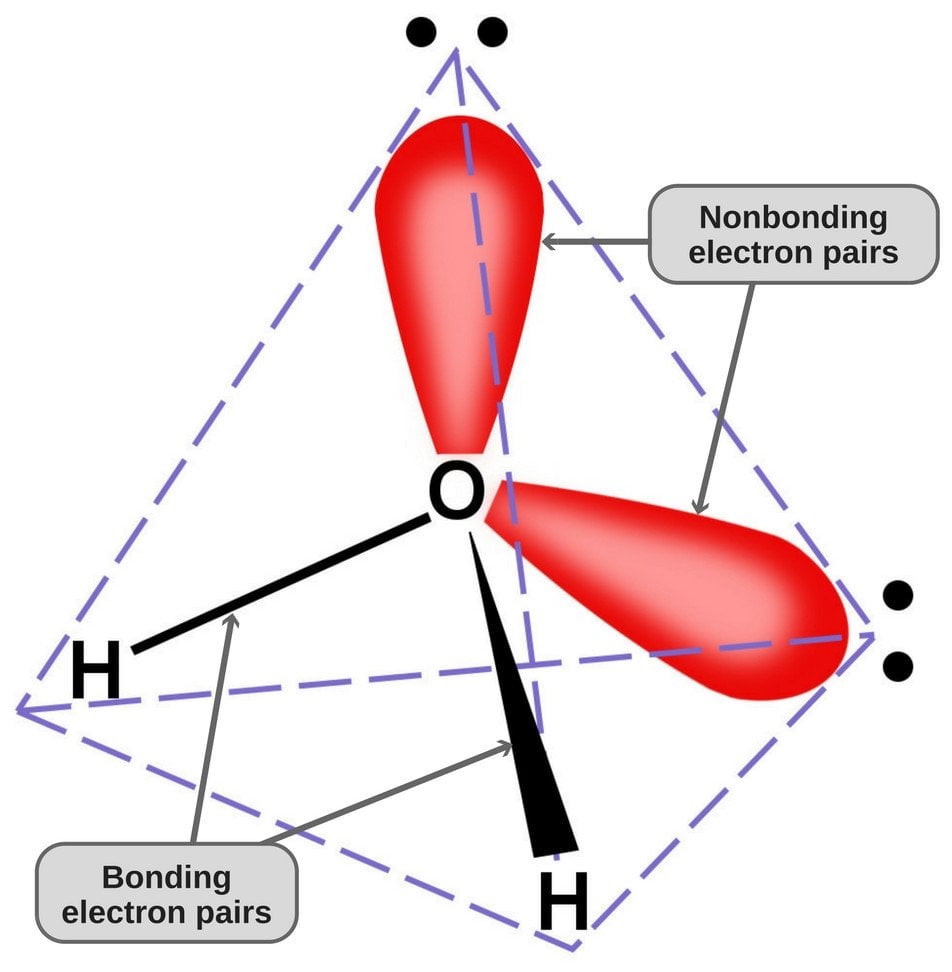
Geometria tetraedrică a moleculei de apă.
Acum, atât atomii de oxigen cât și cei de hidrogen au electronegativități diferite (valoarea electronegativității hidrogenului este de 2,1, în timp ce electronegativitatea oxigenului este de 3,5); prin urmare, ambele legături sunt polare. Deoarece oxigenul este mai electronegativ decât hidrogenul, densitatea de electroni se deplasează spre oxigen în ambele legături, făcând astfel ca regiunea din jurul oxigenului să fie mai negativă decât zonele din jurul celor doi atomi de hidrogen.
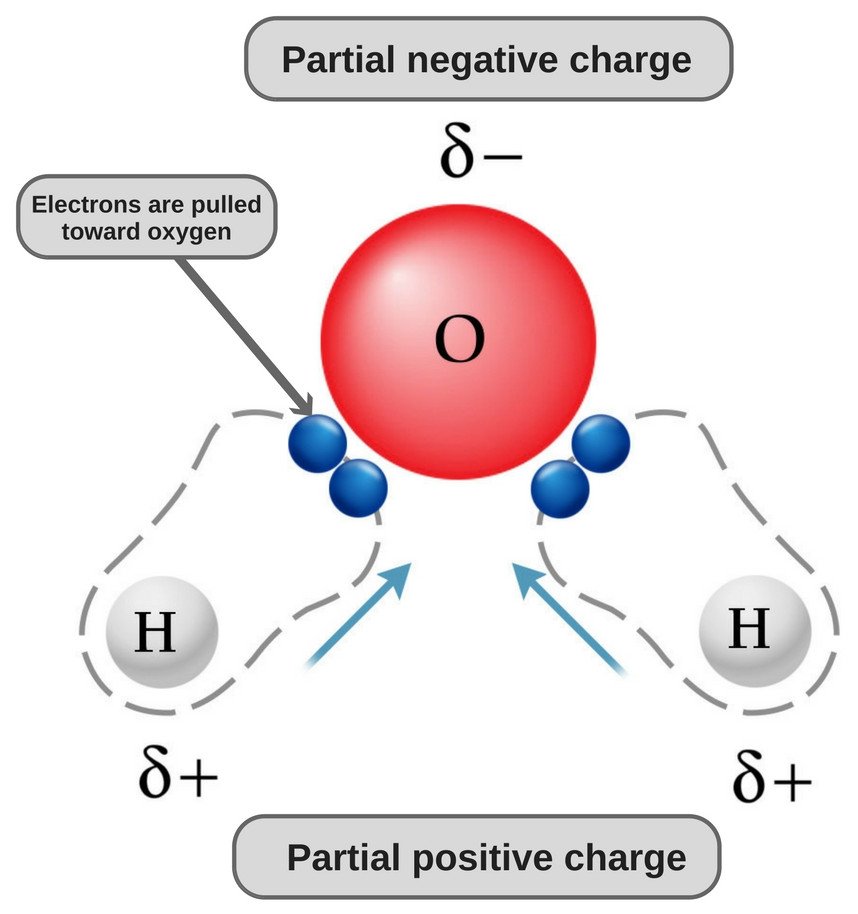
Acesta este motivul pentru care molecula de apă devine polară!
.