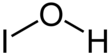
Ácido hipoídico é o composto inorgânico com a fórmula química HIO. Forma-se quando uma solução aquosa de iodo é tratada com sais mercúricos ou de prata. Decompõe-se rapidamente por desproporção:
|
|||
 |
|||
| Nomes | |||
|---|---|---|---|
| Nome IUPAC
Ácido hipoodioso
|
|||
| Identificadores | |||
|
|||
|
3D modelo (JSmol)
|
|||
| ChEBI |
|
||
| ChemSpider |
|
||
|
CID PubChem
|
|||
| UNII |
|
||
|
CompTox Dashboard (EPA)
|
|||
|
|||
|
|||
| Propriedades | |||
| HIO | |||
| Massa solar | 143.89 g/mol | ||
| Acidez (pKa) | 10.5 (em água, estimativa) | ||
| Base conjugada | Hypoiodite | ||
|
Exceto onde de outra forma observado, os dados são dados para materiais no seu estado padrão (a 25 °C , 100 kPa).
|
|||
| |
|||
| ReferênciasInfobox | |||
5 HIO → HIO3 + 2 I2 + 2 H2O
Hypoiodites de metais alcalinos e alcalino-terrosos podem ser feitos em soluções diluídas a frio se o iodo for adicionado aos seus respectivos hidróxidos.O ácido hipoodioso é um ácido fraco com uma pKa de cerca de 11. A base do conjugado é hipoiodito (IO-). Os sais deste ânion podem ser preparados tratando o I2 com hidróxidos alcalinos. Eles são rapidamente desproporcionais para formar iodetos e iodatos.