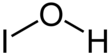
Kwas hipojodowy jest związkiem nieorganicznym o wzorze chemicznym HIO. Powstaje on w wyniku działania wodnego roztworu jodu na sole rtęci lub srebra. Rozkłada się szybko przez dysproporcjonowanie:
|
|||
 |
|||
| Nazwy | |||
|---|---|---|---|
| Nazwa IUPAC
Kwas hipojodowy
|
|||
| Identyfikatory | |||
|
|||
|
model 3D (JSmol)
|
|||
| ChEBI |
|
||
| ChemSpider |
|
||
|
PubChem CID
|
|||
| UNII |
|
||
|
. CompTox Dashboard (EPA)
|
|||
|
|||
|
|||
| Właściwości | |||
| HIO | |||
| Masa molowa | 143.89 g/mol | ||
| Kwasowość (pKa) | 10.5 (w wodzie, szacunkowo) | ||
| Zasada sprzężona | Hipoiodyt | ||
|
Jeśli nie zaznaczono inaczej, dane podano dla materiałów w stanie standardowym (w temperaturze 25 °C , 100 kPa).
|
|||
| |
|||
| Infobox referencje | |||
5 HIO → HIO3 + 2 I2 + 2 H2O
Hipoiodyty metali alkalicznych i metali ziem alkalicznych można otrzymać w zimnych rozcieńczonych roztworach, jeśli do ich odpowiednich wodorotlenków doda się jod.Kwas hipojodowy jest słabym kwasem o pKa około 11. Sprzężoną zasadą jest hipojod (IO-). Sole tego anionu można otrzymać przez traktowanie I2 wodorotlenkami alkalicznymi. Szybko ulegają one dysproporcjonowaniu tworząc jodki i jodany.