Abstract
Hemityroidektomia, czyli jednostronna lobektomia tarczycy, polega na usunięciu połowy gruczołu tarczowego. Zabieg ten wykonuje się zwykle w przypadku podejrzenia guzków tarczycy lub małych zróżnicowanych raków tarczycy na podstawie biopsji metodą aspiracji cienkoigłowej (FNA) oraz sporadycznie w przypadku objawowych łagodnych guzków tarczycy. W większości ośrodków operacja może być bezpiecznie przeprowadzona w trybie ambulatoryjnym, a pacjent może zostać wypisany ze szpitala tego samego dnia. Zazwyczaj zabieg wykonywany jest przez przezszyjkowe nacięcie kołnierza, ale opisywano również zabiegi endoskopowe i przezustne. Zabieg obejmuje mobilizację płata tarczycy, podwiązanie naczyń tarczycy, zachowanie przytarczyc, ochronę nerwu krtaniowego wstecznego i odseparowanie od tchawicy. U opisywanej pacjentki wykryto guzek tarczycy, który w biopsji metodą FNA okazał się nieokreślony. Wykonano hemithyroidektomię w celach diagnostycznych.
Przegląd przypadku
Tło
Guzki tarczycy są częstym objawem klinicznym; prawie 20-70% osób poddanych badaniu USG szyjki macicy może mieć guzki tarczycy.1,2 Chociaż większość tych guzków jest łagodna, u 7-15% pacjentów może występować rak tarczycy3,4 z czego ponad 90% to raki zróżnicowane (brodawkowate lub pęcherzykowe).5 Na podstawie cech ultrasonograficznych guzki tarczycy można sklasyfikować jako łagodne, o niskim podejrzeniu, pośrednim podejrzeniu lub wysokim podejrzeniu złośliwości.6 Na podstawie ultrasonograficznych cech guzka oraz wyników badań laboratoryjnych czynności tarczycy lekarze decydują o konieczności wykonania biopsji guzka metodą aspiracji cienkoigłowej (fine needle aspiration – FNA). Po wykonaniu biopsji radiologicznie podejrzanego guzka cytopatolog dokonuje kategoryzacji komórek w oparciu o system klasyfikacji Bethesda, co pozwala endokrynologom i chirurgom endokrynologicznym oszacować ryzyko złośliwości.7,8. Informacje te można następnie wykorzystać do określenia, którzy pacjenci wymagają hemithyroidektomii lub mogą odnieść korzyść z profilowania molekularnego.9
Skoncentrowana historia pacjenta
Pacjent jest 51-letnim mężczyzną, u którego przypadkowo wykryto guzek tarczycy po stronie prawej w tomografii komputerowej klatki piersiowej wykonanej po wypadku samochodowym. Nie miał żadnych objawów ani oznak nadczynności ani niedoczynności tarczycy. Następnie zgłosił się do lekarza podstawowej opieki zdrowotnej, który przeprowadził badanie przedmiotowe, zlecił badania czynności tarczycy, badania obrazowe i ostatecznie biopsję FNA. Wyniki badań laboratoryjnych były prawidłowe. Badanie ultrasonograficzne ujawniło guzek prawego płata tarczycy o średnicy 2,3 cm z wysoce podejrzanymi cechami. Biopsja została uznana za zgodną z „atypią o nieokreślonym znaczeniu” lub AUS. Pacjent miał również obciążający wywiad rodzinny w kierunku raka tarczycy; zarówno jego siostra, jak i dziadek ze strony ojca byli leczeni z powodu raka brodawkowatego tarczycy. Biorąc pod uwagę wywiad rodzinny, wyniki badania ultrasonograficznego i biopsji, zalecono wykonanie hemithyroidektomii diagnostycznej.
Badanie fizykalne
Ocena guzków tarczycy rozpoczyna się od badania fizykalnego skupiającego się na gruczole tarczowym oraz przyległych szyjnych węzłach chłonnych.6 Tarczyca powinna być oceniana pod kątem obecności dodatkowych guzków. Dodatkowe guzki mogą ostatecznie wpłynąć na wybór operacji. Należy ocenić konsystencję guzka i jego ruchomość. Stałe, twarde guzki mogą wskazywać na bardziej agresywną patologię. Należy zwrócić uwagę na limfadenopatię lub blizny po poprzednich operacjach na szyi. Limfadenopatia może oznaczać przerzutowe rozprzestrzenianie się nowotworu. Nieprawidłowości w głosie pacjenta zauważone przez pacjenta, członków rodziny lub lekarza powinny być oceniane dalej i mogą wymagać laryngoskopii, aby wykluczyć zajęcie nerwu krtaniowego wstecznego. Budowa ciała pacjenta, szerokość szyi, długość szyi, naturalne załamania skóry i wielkość tarczycy/guzka pomagają chirurgowi w podjęciu decyzji o miejscu nacięcia.
U tego konkretnego pacjenta przypadkowo odkryto guzek o wielkości 2,3 cm w prawym płacie tarczycy. Pacjent był szczupłym mężczyzną i dlatego guzek był wyczuwalny w badaniu fizykalnym. Był on ruchomy i gumowaty. Nie stwierdzono dodatkowych wyczuwalnych palpacyjnie guzków w tarczycy. Nie stwierdzono powiększenia węzłów chłonnych szyjnych, nie stwierdzono zmian głosu ani wcześniejszych blizn pooperacyjnych. BMI pacjenta wynosiło 23, a jego szerokość i długość szyi była odpowiednia do wzrostu. Wszystkie typowe punkty orientacyjne, w tym granice mięśni mostkowo-obojczykowo-sutkowych, chrząstki tarczowate i tarczowate oraz wcięcie nadmostkowe były dobrze widoczne i wyczuwalne palpacyjnie.
Obrazowanie
Usonografia tarczycy jest badaniem obrazowym z wyboru u pacjentów z podejrzeniem guzka tarczycy lub radiologicznym podejrzeniem guzka tarczycy w innych badaniach obrazowych (tomografia komputerowa itp.).6 Badanie ultrasonograficzne może pomóc w określeniu wielkości guzka, jak również w uzyskaniu ważnych danych dotyczących cech guzka. Cechy te obejmują skład, echogeniczność, brzegi, obecność zwapnień i kształt. Informacje te mogą być wykorzystane do stratyfikacji ryzyka związanego z guzkiem i określenia, czy wskazane jest wykonanie FNA. Ogólnie rzecz biorąc, hipoechogeniczność, nieregularność, guzki wyższe niż szersze i obecność mikrozwapnień w obrębie guzka zwiększają ryzyko ewentualnej złośliwości.6 Inne metody obrazowania, takie jak tomografia komputerowa lub rezonans magnetyczny szyi, są zwykle zarezerwowane dla pacjentów z bardziej zaawansowaną chorobą, takich jak agresywne nowotwory z miejscowym lub rozległym powiększeniem węzłów.6
W przypadku tego pacjenta badanie ultrasonograficzne ujawniło heterogenny guzek o największym wymiarze 2,3 cm z mikrozwapnieniami, jak pokazano na rycinach 1 i 2.
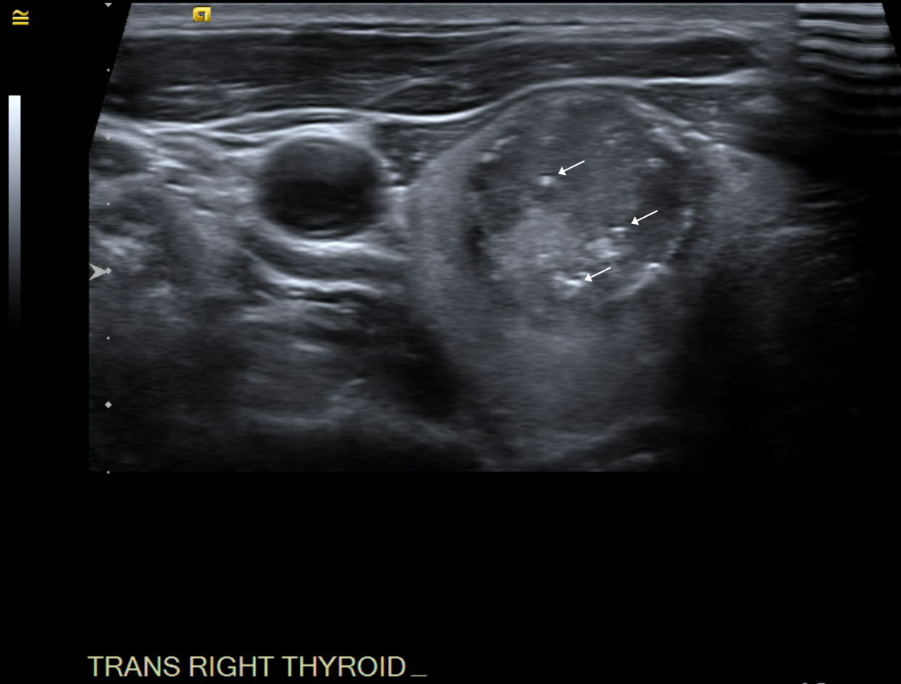 Rycina 1. Widok poprzeczny guzka w obrębie prawego płata tarczycy; białe strzałki oznaczają mikrozwapnienia.
Rycina 1. Widok poprzeczny guzka w obrębie prawego płata tarczycy; białe strzałki oznaczają mikrozwapnienia. 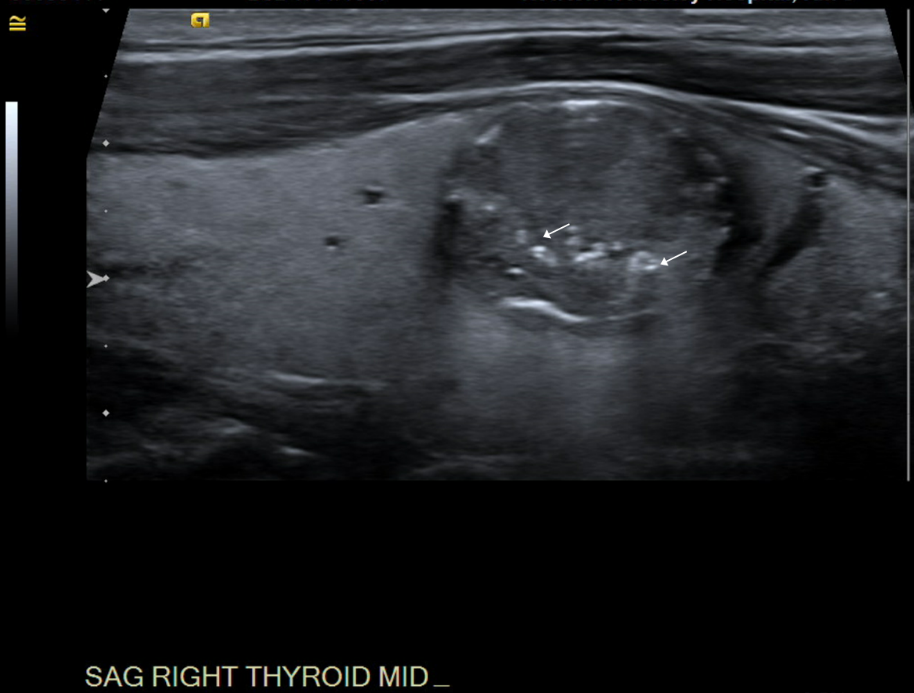 Rycina 2. Widok guzka w płaszczyźnie strzałkowej.
Rycina 2. Widok guzka w płaszczyźnie strzałkowej. Historia naturalna
Historia naturalna łagodnych cytologicznie guzków nie jest w pełni poznana; dostępne dane sugerują jednak, że większość guzków rzeczywiście zwiększa swoje rozmiary w ciągu kolejnych 3-5 lat od pierwszego wykrycia.10,11 Ostatecznie może to wymagać operacji z powodu objawów lub powtórnej biopsji. Nie wydaje się jednak, aby wzrost guzka korelował ze zwiększonym ryzykiem złośliwości.10-12
Historia naturalna nieleczonego, potwierdzonego biopsją zróżnicowanego raka tarczycy jest trudniejsza do zrozumienia, biorąc pod uwagę fakt, że większość tych chorych poddawana jest operacji. Jednak ostatnio wzrosło zainteresowanie obserwacją małych raków brodawkowatych tarczycy o wielkości poniżej 1 cm, o ile nie występują czynniki ryzyka bardziej zaawansowanej lub agresywnej choroby. Z ograniczonych danych wynika, że te małe raki brodawkowate nie ulegają dramatycznej progresji w czasie i że wiele z nich można obserwować bez leczenia.13
Opcje leczenia
Możliwości leczenia guzków tarczycy zależą od wyników badań radiograficznych, wyników biopsji, badań czynności tarczycy i objawów miejscowych. Jeśli guzek wydaje się łagodny w badaniu ultrasonograficznym, nie powoduje objawów i nie jest przyczyną nadczynności tarczycy, można go obserwować. Guzki o łagodnym wyglądzie, które są zgodne z gruczolakiem toksycznym lub wolem wieloguzkowym toksycznym mogą być leczone chirurgicznie, radiojodem lub tionamidem. Sonograficznie podejrzane guzki powinny być poddane biopsji. Jeśli wynik biopsji jest łagodny, można kontynuować obserwację. Powtórna biopsja może być wskazana, jeśli wstępne FNA jest niediagnostyczne. U pacjentów z nieokreślonym lub podejrzanym wynikiem biopsji można uzyskać dalszą stratyfikację ryzyka za pomocą badań profilowania molekularnego lub rozważyć poddanie się diagnostycznej hemithyroidektomii.6 Obserwacja jest również opcją zależną od czynników ryzyka pacjenta. W przypadku osób z nieokreślonym/podejrzanym wynikiem biopsji i kilkoma guzkami w obu płatach tarczycy lub z niedoczynnością tarczycy można rozważyć całkowitą tyreoidektomię jako leczenie wstępne.
Przesłanki do leczenia
Ta pacjentka ma kilka powodów, dla których należy przeprowadzić operację, a w szczególności diagnostyczną hemithyroidektomię. Po pierwsze, guzek miał podejrzane cechy na podstawie badania ultrasonograficznego. Po drugie, wynik biopsji był nieokreślony. Po trzecie, w jego rodzinie występowały przypadki raka tarczycy, co zwiększa ogólne ryzyko. Gdyby naprawdę chciał uniknąć operacji, mógłby rozważyć profilowanie molekularne guzka w celu dalszej stratyfikacji ryzyka zmiany. Biorąc jednak pod uwagę, że poza tym jest sprawny i zdrowy, zabieg o niskim ryzyku, taki jak hemithyroidektomia, jest bardzo rozsądną i ostateczną metodą w porównaniu z profilowaniem molekularnym.
Dyskusja
Historia operacji tarczycy sięga 1800 roku, kiedy Theodor Billroth rozpoczął jej wykonywanie w Szwajcarii. W tym czasie wyniki były słabe i dlatego kilku jego asystentów chirurgicznych i stażystów próbowało je poprawić. Największy sukces odniósł Theodor Kocher, który jako pierwszy opisał jednostronną lobektomię, próbując zminimalizować pooperacyjną niedoczynność tarczycy.14
Od tamtego czasu tyreoidektomia stała się bardzo bezpieczną operacją z bardzo niskim odsetkiem powikłań. W wielu ośrodkach hemithyroidektomia jest wykonywana w trybie ambulatoryjnym. Pacjenci są zwykle wypisywani do domu w ciągu kilku godzin po operacji.
Historycznie rak tarczycy był leczony agresywnie, a większość pacjentów poddawano całkowitej tyreoidektomii. Aktualne piśmiennictwo sugeruje, że nie ma różnicy w przeżywalności wybranych chorych z małymi nowotworami o niskim ryzyku, u których wykonuje się hemithyroidektomię w porównaniu z całkowitą tyreoidektomią.6,15 Dlatego też coraz więcej chorych otrzymuje opcję hemithyroidektomii, zwłaszcza w przypadku nieokreślonego lub podejrzanego guzka na podstawie biopsji. Ponadto prowadzi się wiele badań nad genetycznymi i molekularnymi podstawami raka tarczycy, co może doprowadzić do stworzenia genetycznych celów leczenia. Wyniki tych badań mogą w przyszłości doprowadzić do konieczności mniej agresywnych operacji tarczycy. Ostatecznie decyzja o operacji i jej zakresie jest przedmiotem dyskusji między chirurgiem, endokrynologami i pacjentem.
W przypadku tego pacjenta ostateczna patologia ujawniła raka brodawkowatego tarczycy o maksymalnych wymiarach 2,1 cm. Nie było innych cech sugerujących agresywny przebieg choroby, jednak pacjent starannie rozważył ryzyko i korzyści wynikające z obserwacji płata kontralateralnego lub całkowitej tyreoidektomii. Biorąc pod uwagę wywiad rodzinny, ostatecznie zdecydował się na doszczętną tyreoidektomię, która została wykonana bez powikłań. Obecnie radzi sobie dobrze dzięki stałej obserwacji.
Sprzęt
Lokalizator nerwów Nerveana, Neurovision Medical Products
Ujawnienia
Autorzy nie mają żadnych ujawnionych informacji do zgłoszenia.
Oświadczenie o zgodzie
Pacjent, o którym mowa w tym artykule wideo, wyraził świadomą zgodę na filmowanie i jest świadomy, że informacje i obrazy zostaną opublikowane online.
Cytaty
- Tan GH, Gharib H. Thyroid incidentalomas: management approaches to nonpalpable nodules discovered incidentally on thyroid imaging. Ann Intern Med. 1997;126(3):226-231. doi:10.7326/0003-4819-126-3-199702010-00009.
- Guth S, Theune U, Aberle J, Galach A, Bamberger CM. Very high prevalence of thyroid nodules detected by high frequency (13 MHz) ultrasound examination. Eur J Clin Invest. 2009;39(8):699-706. doi:10.1111/j.1365-2362.2009.02162.x.
- Hegedüs L. The thyroid nodule. N Engl J Med. 2004;351(17):1764-1771. doi:10.1056/NEJMcp031436.
- Mandel SJ. A 64-year-old woman with a thyroid nodule. JAMA. 2004;292(21):2632-2642. doi:10.1001/jama.292.21.2632.
- Sherman SI. Thyroid carcinoma. Lancet. 2003;361(9356):501-511. doi:10.1016/S0140-6736(03)12488-9.
- Haugen BR, Alexander EK, Bible KC, et al. 2015 American Thyroid Association Management Guidelines for Adult Patients with Thyroid Nodules and Differentiated Thyroid Cancer: The American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. Thyroid. 2016;26(1):1-133. doi:10.1089/thy.2015.0020.
- Cibas ES, Ali SZ. The Bethesda System for Reporting Thyroid Cytopathology. Am J Clin Pathol. 2009;132(5):658-665. doi:10.1309/AJCPPHLWMI3JV4LA.
- Bongiovanni M, Spitale A, Faquin WC, Mazzucchelli L, Baloch ZW. The Bethesda System for Reporting Thyroid Cytopathology: a meta-analysis. Acta Cytol. 2012;56(4):333-339. doi:10.1159/000339959.
- Ferris RL, Baloch Z, Bernet V, et al; American Thyroid Association Surgical Affairs Committee. American Thyroid Association Statement on Surgical Application of Molecular Profiling for Thyroid Nodules: Current Impact on Perioperative Decision Making. Thyroid. 2015;25(7):760-768. doi:10.1089/thy.2014.0502.
- Alexander EK, Hurwitz S, Heering JP, et al. Natural history of benign solid and cystic thyroid nodules. Ann Intern Med. 2003;138(4):315-318. doi:10.7326/0003-4819-138-4-200302180-00010.
- Ajmal S, Rapoport S, Ramirez Batlle H, Mazzaglia PJ. The natural history of the benign thyroid nodule: what is the appropriate follow-up strategy? J Am Coll Surg. 2015;220(6):987-992. doi:10.1016/j.jamcollsurg.2014.12.010.
- Durante C, Costante G, Lucisano G, et al. The natural history of benign thyroid nodules. JAMA. 2015;313(9):926-935. doi:10.1001/jama.2015.0956.
- Miyauchi A. Clinical Trials of Active Surveillance of Papillary Microcarcinoma of the Thyroid. World J Surg. 2016;40(3):516-522. doi:10.1007/s00268-015-3392-y.
- Hannan SA. The magnificent seven: a history of modern thyroid surgery. Int J Surg. 2006;4(3):187-191. doi:10.1016/j.ijsu.2006.03.002.
- Welch HG, Doherty GM. Saving thyroids – overtreatment of small papillary cancers. N Engl J Med. 2018;379(4):310-312. doi:10.1056/NEJMp1804426.