Mechanizmy wyjaśniają regioselektywność
X2/H2O lub X2/ROH: Regioselektywność tworzenia halohydryn w reakcji alkenu z halogenem w rozpuszczalniku nukleofilowym jest analogiczna do ścieżki oksymerkurcja-demerkurcja. Cząsteczka halogenu przyjmuje rolę elektrofilu przyjmując nukleofilowe elektrony pi z alkenu i jednocześnie tworzy wiązanie z drugim węglem winylowym tworząc jon bromonowy (lub chlorocyjanowy). Tworzenie jonu bromonowego (lub chloronowego) stabilizuje ładunek dodatni i zapobiega rearanżacji karbokationów. Rozpuszczalnik przyjmuje rolę nukleofila, ponieważ jest obecny w znacznie większym stopniu niż grupa opuszczająca i reaguje z najbardziej podstawionym węglem cyklicznego jonu bromonowego (lub chloronowego) tworząc regiochemię. Stereochemia tej reakcji jest antyaddycyjna, ponieważ rozpuszczalnik zbliża się do jonu bromonowego z orientacją wsteczną, aby wytworzyć produkt addycji. Jednakże, ponieważ oddziaływanie halogenu z alkenem może zachodzić od góry lub od dołu, nie ma kontroli stereochemicznej w tej reakcji i w stosownych przypadkach powstanie mieszanina enancjomerów. Ostatnim etapem tego mechanizmu jest przeniesienie protonu do cząsteczki wody w rozpuszczalniku w celu neutralizacji produktu addycji.
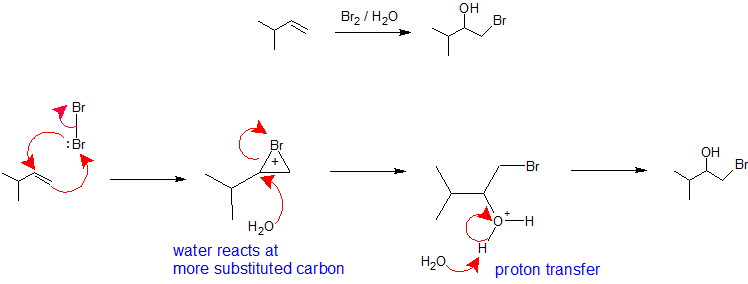
HOX lub RSCl: Regioselektywność reakcji kwasów hipohydrynowych i chlorku sulfenylu można wyjaśnić tym samym mechanizmem, którego użyliśmy do zracjonalizowania reguły Markownikowa. Wiązanie elektrofilowego gatunku do podwójnego wiązania alkenu tworzy preferencyjnie bardziej stabilną (silniej podstawioną) karbokację. Pośrednik ten powinien następnie szybko łączyć się z nukleofilową formą w celu wytworzenia produktu addycji.
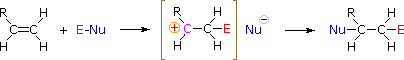
Aby zastosować ten mechanizm musimy określić elektrofilową cząsteczkę w każdym z reagentów. Wykorzystując różnice elektronegatywności możemy podzielić powszechnie występujące odczynniki addycyjne na część elektrofilową i nukleofilową, jak pokazano po prawej stronie. W przypadku kwasów podchlorawego i hipobromowego (HOX), te słabe kwasy Brønsteda (pKa ok. 8) nie reagują jako donory protonów; a ponieważ tlen jest bardziej elektroujemny niż chlor lub brom, elektrofil będzie kationem halogenkowym. Formą nukleofilową, która wiąże się z pośrednią karbokationem jest jon wodorotlenkowy lub, co bardziej prawdopodobne, woda (zwykły rozpuszczalnik dla tych odczynników), a produkty nazywane są halohydrynami. Chlorki sulfenylu dodają się w odwrotny sposób, ponieważ elektrofil jest kationem siarki, RS(+), podczas gdy nukleofilową cząsteczką jest anion chlorkowy (chlor jest bardziej elektroujemny niż siarka).
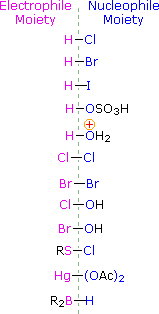
Poniżej znajduje się kilka przykładów ilustrujących dodawanie różnych elektrofilowych odczynników halogenowych do grup alkenowych. Zwróć uwagę na specyficzną regiochemię produktów, jak wyjaśniono powyżej.
Ćwiczenie
1. Przewidać produkt następującej reakcji:

2. Gdy buten jest traktowany NBS w obecności wody, produkt pokazuje, że brom znajduje się na najmniej podstawionym węglu, czy jest to reakcja Markownikowa czy anty-Markownikowa?
Odpowiedź

2. Ponieważ brom jest pierwszym dodatkiem do alkenu, ten dodatek byłby dodatkiem antymarkownikowskim.
Wydawcy
-
Prof. Steven Farmer (Sonoma State University)
-
William Reusch, Professor Emeritus (Michigan State U.), Virtual Textbook of Organic Chemistry
.