De XeF4 of Xenon Tetrafluoride is een chemische verbinding gemaakt van Xenon en Fluoride atomen. Het is ’s werelds eerste ontdekte binaire verbinding. Het is een soort edelgas met de chemische vergelijking van
Xe +2 F2 -> XeF4
De XeF4 heeft een vast wit uiterlijk en heeft een dichtheid van 4,040 g cm-3 in vaste vorm. In gewone omstandigheden verschijnt het als een kleurloze kristallijn. Het heeft een sublieme temperatuur van 115,7-graden Celsius of 240,26-graden Fahrenheit. Net als de andere xenonfluoriden wordt xenon-tetrafluoride exergonisch gevormd. Bij normale temperatuur en druk blijft het in stabiele toestand. Het reageert onmiddellijk met water en daarbij komen moleculaire zuurstof, waterstoffluoride en zuiver xenongas vrij.
| Naam van het molecuul | Xenontetrafluoride (XeF4) |
| Nr. van valentie elektronen in het molecuul | 36 |
| Hybridisatie van XeF4 | sp3d2 hybridisatie |
| Bondshoeken | 90 graden en 180 graden |
| Moleculaire Geometrie van XeF4 | Vierkante Planaire |
Om meer te weten over zijn fysische eigenschappen en chemische eigenschappen, moet men de Lewis-structuur en de moleculaire geometrie kennen. Laten we de Lewis-structuur van xenon tetrafluoride uitzoeken.
Voor het maken van de Lewis-structuur moeten we de valentie-elektronen van XeF4 kennen om de structuur te maken en de plaats van de atomen in het molecuul te kennen.
Inhoud
XeF4 Valentie-elektronen
In dit molecuul hebben we één atoom van Xenon en vier atomen van Fluor. We zullen de valentie-elektronen van deze twee atomen berekenen om het totale aantal valentie-elektronen van XeF4 te bepalen.
Valence-elektronen van Xenon = 8
Valence-elektronen van Fluor = 7*4 (omdat er vier Fluor-atomen zijn, vermenigvuldigen we dat met 4)
Totaal aantal valentie-elektronen van Xef4: 8 + 7*4
: 8 + 28
: 36
Hiermee zijn er in totaal 36 valentie-elektronen in XeF4.
XeF4 Lewisstructuur
Nu we de valentie-elektronen van xenon-tetrafluoride kennen, zal het voor jou gemakkelijker zijn om de Lewisstructuur te tekenen. Deze Lewis-puntstructuur is een picturale voorstelling van valentie-elektronen rond individuele atomen in een molecuul, samen met de binding die ze vormen.
De bindingen in de structuur worden weergegeven met lijnen, terwijl de elektronen die niet deelnemen aan de bindingvorming worden weergegeven als stippen. Elektronen die geen binding vormen, worden niet-bindende elektronen of lone elektronenparen genoemd.
Hierom is xenon het minst elektronegatieve atoom, dus plaatsen we het in het midden en alle andere fluoratomen eromheen:

Nu we alle atomen hebben geplaatst, laten we de bindingen tussen elk fluor- en xenonatoom zien. Elke binding in het molecuul neemt twee elektronen in beslag, en aangezien er vier enkelvoudige bindingen in dit molecuul zijn, worden 8 van de 36 elektronen opgebruikt.
Start met het plaatsen van de rest van de valentie-elektronen rond de atomen. Elk fluoratoom zal zes valentie-elektronen om zich heen hebben, omdat één elektron werd gebruikt om de binding te maken.
Het is u misschien opgevallen dat we al 24 van de 28 elektronen rond de fluoratomen hebben geplaatst. De resterende niet-bindende elektronen of elektronenparen zullen op Xenon worden geplaatst, omdat dit een uitzondering op de octetregel is.
Plaats deze twee paren niet-bondelende elektronen op Xenon, en nu heb je een Lewisstructuur waar er twee eenzame elektronenparen op Xenon zijn en zes niet-bondelende elektronen op elk Fluoratoom.
Hybridisatie van XeF4
De centrale omloopbanen van het xenonatoom zijn gehybridiseerd, waardoor er nieuwe gehybridiseerde omloopbanen ontstaan. Xenon heeft zes elektronen in zijn 5p-banen en twee elektronen in 5s-banen. Er zijn geen elektronen in d- en f-banen in de grondtoestand van xenon. Maar als dit atoom in een aangeslagen toestand is, verhuizen twee elektronen in de p-banen naar d-banen; daardoor zijn er in totaal vier ongepaarde elektronen. Twee daarvan bevinden zich in p-banen, en de andere twee in d-banen. Deze gehybridiseerde orbitalen leiden tot sp3d2 hybridisatie in XeF4.
XeF4 Moleculaire Geometrie
Het is gemakkelijker om de moleculaire geometrie van een bepaald molecuul te begrijpen als we zijn Lewisstructuur kennen. Omdat Xenon twee elektronenparen heeft, zal het een structuur aannemen die deze elektronenparen helpt de afstotingskrachten te vermijden. Om deze afstotingen tot een minimum te beperken, zullen de lone paren zich in een loodrecht vlak bevinden. En aangezien er vier fluoratomen zijn, zal het molecuul een zodanige opstelling hebben dat de moleculaire geometrie vierkant vlak is. XeF4 heeft een elektronische geometrie van octahedraal, waardoor de moleculaire geometrie van xenon-tetrafluoride vierkant vlak is.

XeF4 Bindingshoeken
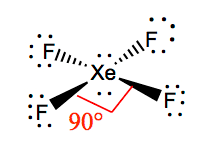
De bindingshoeken van F-Xe-F zijn 90 graden, en de lone pairs hebben hoeken van 180 graden. De fluoratomen staan in een hoek van 90 graden ten opzichte van elkaar, wat resulteert in een symmetrische verdeling van de elektronen in het vlak van het molecuul. Deze bindingshoeken dragen bij tot de vorming van een vierkante vlakke moleculaire geometrie.
XeF4 polariteit – Is XeF4 polair of niet-polair?
Hoewel de bindingen tussen Xenon en Fluor atomen polair zijn, is XeF4 een niet polair molecuul. Vraag je je af hoe? Alle Xe-F bindingen staan onderling in oppositie met elkaar, waardoor de som van het dipoolmoment nul is. Omdat er vier elektronen op het xenonatoom zitten, die gelokaliseerd zijn als niet-bindende elektronenparen. Aangezien de algemene rangschikking van de atomen en de elektronen in het molecuul zodanig is dat de vectorsom van de dipolen nul is, is XeF4 een niet-polair molecuul.
Conclusies
Xenon-tetrafluoride is een van die moleculen die betrekkelijk gemakkelijk te begrijpen zijn. Zijn Lewis-structuur is een van de minst gecompliceerde structuren, omdat alle fluoratomen in het symmetrische patroon zijn gerangschikt. De lone pairs in het molecuul bevinden zich in een loodrecht vlak in een octahedrale vorm om hun afstotende krachten tot een minimum te beperken.
Om deze blogpost samen te vatten, kunnen we zeggen dat XeF4 36 valentie-elektronen heeft. Het heeft twee eenzame paren van niet-bindende elektronen op het centrale atoom van Xenon. Het molecuul heeft een octahedrale elektronengeometrie en een vierkante planaire moleculaire geometrie. XeF4 is een apolair molecuul en heeft sp3d2 hybridisatie.