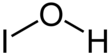
Hypojoodzuur is de anorganische verbinding met de chemische formule HIO. Het wordt gevormd wanneer een waterige oplossing van jodium wordt behandeld met kwik- of zilverzouten. Het ontleedt snel door disproportionering:
|
|||
 |
|||
| Namen | |||
|---|---|---|---|
| IUPAC-naam
Hypojoodzuur
|
|||
| Identifiers | |||
|
|||
|
3D-model (JSmol)
|
|||
| ChEBI |
|
||
| ChemSpider |
|
||
|
PubChem CID
|
|||
| UNII |
|
||
|
CompTox Dashboard (EPA)
|
|||
|
|||
|
|||
| Eigenschappen | |||
| HIO | |||
| Molaire massa | 143.89 g/mol | ||
| Zuurgraad (pKa) | 10.5 (in water, schatting) | ||
| Conjugaatbasis | Hypoiodiet | ||
|
Behoudens andersluidende vermelding gelden de gegevens voor materialen in hun standaardtoestand (bij 25 °C , 100 kPa).
|
|||
| |
|||
| Infoboxreferenties | |||
5 HIO → HIO3 + 2 I2 + 2 H2O
Hypojodieten van alkali- en aardalkalimetalen kunnen in koude verdunde oplossingen worden gemaakt als jood wordt toegevoegd aan hun respectieve hydroxiden.Hypojoodzuur is een zwak zuur met een pKa van ongeveer 11. De geconjugeerde base is hypojodiet (IO-). Zouten van dit anion kunnen worden bereid door I2 met alkalihydroxiden te behandelen. Zij disproportioneren snel tot jodiden en jodaten.