Chloride is het meest voorkomende anion in het extracellulaire vloeistofcompartiment (ECF). Hyperchloremie wordt gedefinieerd als een toename van de chlorideconcentratie in het plasmawater. Hyperchloremie en een relatief teveel aan chloride in het lichaam zijn in verband gebracht met de ontwikkeling van een verminderde doorbloeding van de nieren,1,2 een verhoogd interstitieel oedeem, ook in de nieren en het maagdarmstelsel,3 een verhoogde morbiditeit en mortaliteit bij ernstig zieke patiënten,4,5 en een verminderde overleving en herstel bij patiënten met acute nierschade.6 Net als natrium en andere chemicaliën in het ECF-compartiment, wordt de chlorideconcentratie gereguleerd. Het orgaan dat verantwoordelijk is voor het handhaven van de chloride balans in het lichaam is de nier. Dit artikel behandelt de chlorideverwerking door de nier en klinische situaties waarin hyperchloremie kan optreden.
Nierverwerking van chloride
Het chloridegehalte in het plasma wordt gereguleerd door de nier. De nier filtert chloride vrij over de keldermembranen van de glomeruli. De hoeveelheid chloride die in de urine wordt uitgescheiden, wordt bepaald door het chloride dat door de glomeruli wordt gefilterd en door een reeks transportprocessen die langs het nefron plaatsvinden. Onder normale omstandigheden wordt meer dan 60% van het gefilterde chloride geabsorbeerd langs de proximale tubulus. In de vroege proximale tubulus wordt natrium geabsorbeerd met een evenredige hoeveelheid water, zodat de natriumconcentratie niet verandert. Bicarbonaat en andere niet-chloride anionen worden daarentegen snel met natrium geabsorbeerd en uit het filtraat verwijderd7 (Fig. 1A). Terwijl natrium en andere anionen worden geabsorbeerd in de eerste proximale tubuli (S1 en S2), neemt de chlorideconcentratie in het lumen van de proximale tubuli toe. Tegen de tijd dat de tubulaire vloeistof het laatste segment van de proximale tubulus bereikt (S3), is de chlorideconcentratie hoog ten opzichte van de plasmaconcentratie, waardoor chloride passief kan worden geabsorbeerd langs de concentratiegradiënt (Fig. 1B). De transepitheliale permeabiliteit voor chloride is hoger dan de permeabiliteit voor bicarbonaat, zodat ondanks de gradiënt voor bicarbonaat van peritubulair naar lumen, het transport van chloride dat het lumen verlaat groter is dan het bicarbonaat dat de tubulaire vloeistof binnenkomt.

(A) In de vroege proximale tubulus vindt isotone natriumabsorptie plaats met organische oplosmiddelen, bicarbonaat, fosfaat samen met water, wat resulteert in een stijgende chlorideconcentratie. (B) De hoge chlorideconcentratie in het lumen bevordert ook het transcellulaire en paracellulaire transport. Intercellulaire juncties in de latere proximale tubulus worden meer permeabel voor chloride waardoor paracellulair transport wordt bevorderd. Zelfs wanneer de bicarbonaatconcentratie in het lumen daalt, blijft Na+-H+-uitwisseling een rol spelen bij de NaCl-reabsorptie. Transcellulaire natriumchloride-absorptie kan plaatsvinden via de koppeling van Na+-H+ uitwisseling met chloride-organische anionenuitwisseling (formiaat, oxalaat). Het organische zuur (mierenzuur of oxaalzuur) wordt gerecycleerd in de cellen.
In het eerste deel van de proximale tubulus vindt chloride-absorptie ook plaats via apicale chloride-anion (formaat, oxalaat, base) wisselaars en verlaat het de cel via basolaterale membraantransporteurs8 (Fig. 1B). Bij hyperchloremische metabole acidose als gevolg van HCl- of ammoniumchloride-belasting is de chloride reabsorptie in de proximale tubulus verminderd, deels vanwege de vermindering van de organische anion transporters die natrium-chloride transport faciliteren9 en de vermindering van de lumen-peritubulaire gradiënt voor chloride.
De dikke opgaande ledemaat van de lus van Henle (TALH) is een belangrijke plaats voor chloride reabsorptie.10 Op deze plaats worden natrium, kalium en chloride gelijktijdig getransporteerd via een natrium-kalium-2-chloride co-transporter (NKCC2) (Fig. 2). Chloride komt de TALH-cel binnen en verlaat zijn basolaterale aspect via een electrogenic chloride channel of via de electroneutrale kalium-chloride co-transporter. De beweging van chloride door het basolaterale chloridekanaal (CLC-NKB) draagt bij tot het ontstaan van een transepitheliale positieve (lumen) tot negatieve (basolaterale) potentiaalgradiënt. De intracellulaire positieve potentiaal die zou worden gegenereerd door de beweging van chloride uit de cel wordt gecompenseerd door de basolaterale electrogene Na+-K+ ATPase die natrium uit de cel transporteert in ruil voor kalium in de cel in een 3-2 verhouding. ROMK-kaliumkanalen op het apicale TALH-celmembraan dragen bij tot de positieve lumenpotentiaal (intracellulair negatief) door de geleidende beweging van kaliumionen van cel naar lumen. Het algemene effect is dat chloride, natrium en kalium de cel binnenkomen via NKCC2, en voor het grootste deel verlaat chloride de cel via het basolaterale ClC-NKB chloridekanaal, natrium verlaat de cel via de Na+-K+ ATPase en kalium recycleert terug naar het lumen via het ROMK kanaal of verlaat basolateraal de cel via de KCl co-transporter. De nauwe koppeling tussen natrium- en chloridetransport in de TALH wordt onderstreept door een van de varianten van het Bartter-syndroom, waarbij defecten in basolaterale chloridekanalen de natrium-chloridereabsorptie verstoren en het nierdefect nabootsen dat wordt waargenomen bij abnormale NKCC2-eiwitten. Hoewel andere transporters aan de peritubulaire zijde van de TAL-cel, zoals de KCl co-transporter, chloride transporteren op een natrium-onafhankelijke manier, is het grootste deel van de chloride die wordt opgenomen door de TALH gekoppeld aan natrium reabsorptie. Daarom zullen factoren die de natriumreabsorptie in dit segment verhogen, ook de chlorideherabsorptie verhogen.
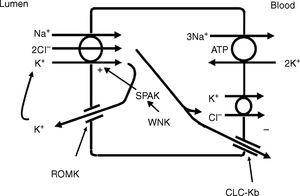
De dikke opgaande ledemaat van de lus van Henle absorbeert chloride via de apicale Na+-K+-2Cl- cotransporter (NKCC2) en chloride verlaat de cel via een basolateraal chloridekanaal en door K+-Cl- cotransport. K+ recycling in het lumen en basolaterale geleidende Cl- uittreding via CLC-Kb dragen bij aan de positieve-negatieve lumen naar basolaterale transepitheliale gradiënt. Intracellulair chloride kan NKCC2 transport reguleren via een chloride-sensing WNK kinase (WNK) dat het STE20/SPS1-gerelateerd proline/alanine-rijk kinase (SPAK) en NKCC2 kan activeren wanneer intracellulair Cl- laag is. Anderzijds, wanneer chloride zich ophoopt in de cel als gevolg van defecten in de basolaterale chloride kanaal exit pathway, wordt NKCC2 transport geblokkeerd. Wanneer NKCC2 wordt gestimuleerd, bijvoorbeeld door antidiuretisch hormoon, wordt de chloride-intrede verhoogd, maar wordt ook de basolaterale Cl-geleiding versterkt.
In de distale convoluale tubulus worden natrium en chloride vanuit het lumen naar de cel getransporteerd door een natrium-chloride co-transporter (NCC)11 (Fig. 3). De drijvende kracht voor het transport van chloride van het lumen naar de cellen komt van de natriumgradiënt tussen het lumen en de cel, die wordt opgewekt door de basolaterale Na+-K+ ATPase, die natrium uit de cel pompt, waardoor de intracellulaire natriumconcentraties laag blijven. Verdere regulatie van NCC en NKCC kan plaatsvinden via WNK kinases, die kunnen dienen als chloorsensoren12 en deze transporters kunnen reguleren door hun trafficking of hun fosforylatietoestand te wijzigen.13 In latere delen van de distale convoluted tubule kan een negatieve lumenpotentiaal, opgewekt door beweging van natrium door het apicale epitheliale natriumkanaal (ENaC), ook dienen als drijvende kracht voor passieve chloride reabsorptie. Aldus vertonen de segmenten van de distale convoluted tubule een directe koppeling van natrium- en chloridetransport via de NCC en een indirecte koppeling van transport via passieve beweging langs een elektrochemische gradiënt.
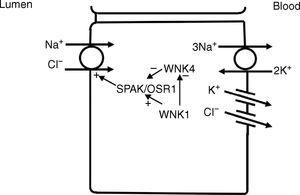
In de distale convoluale tubulus worden natrium en chloride in het lumen in de cel opgenomen via een Na+-Cl- cotransporter (NCC). Transport via NCC wordt aangedreven door een laag intracellulair natrium dat meestal wordt gegenereerd door het basolaterale Na+-K+ ATPase. Het WNK1 kinase kan dienen als chloride sensor om remming van NCC door het WNK4 kinase te blokkeren.
De verzamelbuis speelt een belangrijke rol bij het bepalen van het chloridegehalte van de uiteindelijke urine. Chloridenreabsorptie in dit deel van het nefron helpt om chloride te behouden als reactie op een lage chloride-inname en kan bijdragen tot de hypertensieve effecten van een natriumchloridedieet. Het grootste deel van het natrium dat in de verzamelbuis wordt geabsorbeerd, gebeurt in de hoofdcellen via aldosteron-gereguleerde apicale epitheliale natriumkanalen. Chloride reabsorptie in de verzamelleiding kan plaatsvinden via paracellulaire chloride absorptie die wordt aangedreven door de lumen negatieve transepitheliale potentiaal gegenereerd door lumen-naar-cel natrium stroom via ENaC (Fig. 4A). Bovendien kan in intercalaire cellen van het type B en niet van het type A chloride worden getransporteerd via pendrine, een chloride-bicarbonaat wisselaar, waarbij chloride van lumen naar cel wordt getransporteerd terwijl bicarbonaat in het lumen wordt afgescheiden (Fig. 4B). De relatie tussen verschillende natrium en chloride transportprocessen in dit deel van het nefron werd geïllustreerd in een recent artikel van Vallet en collega’s.14 De auteurs voerden een aantal fysiologische manoeuvres uit om hun effecten op ENaC en pendrine eiwitniveaus in de nier te bepalen. Langdurige NaCl belasting verminderde de pendrine eiwit niveaus significant, terwijl er een afname was in de “actieve” ENaC-γ submit en een verhoogde β-subeenheid. Een dissociatie tussen natrium- en chloridetransport werd waargenomen, echter, met remming van de natrium-chloride co-transporter met hydrochloorthiazide, daalden pendrine niveaus maar ENaC niveaus stegen. NaCl-restrictie verhoogde de expressie van pendrine.15 Een verhoogde luminale bicarbonaatconcentratie die zou ontstaan door pendrine-gemedieerde bicarbonaatsecretie beïnvloedt de natriumreabsorptie door de activiteit van de ENaC stroomafwaarts te verhogen.16 Natriumchloridetransport door intercalerende cellen kan ook worden bevorderd door de aanwezigheid van een thiazide-gevoelige apicale natriumafhankelijke chloride-bicarbonaat wisselaar (NDCBE, Slc4A8) die 1 natrium- en 2 bicarbonaationen vanuit het lumen in de cel transporteert in ruil voor 1 chloride-ion dat de cel verlaat. Als NDCBE transport gekoppeld is aan pendrin-gemedieerde chloride-bicarbonaat uitwisseling, kunnen de twee transporters samen resulteren in netto natrium-chloride reabsorptie uit het lumen, omdat het bicarbonaat in en uit de cel recycleert terwijl natrium en chloride de cel binnenkomen17 (Fig. 4B). Factoren die de verhouding tussen de hoeveelheden of de activiteiten van deze twee anionenwisselaars veranderen, kunnen het netto-effect op de bicarbonaatafscheiding en de chlorideherabsorptie bepalen. Een andere transporteur die betrokken kan zijn bij de uitscheiding van een teveel aan chloride in het lichaam is de Slc26A9 transporteur, die kan fungeren als een chloridekanaal in de medullaire delen van de verzamelbuis.18 Hij kan het effect van de chloridebelasting wijzigen door de chloride-uitscheiding te verhogen onder omstandigheden van een teveel aan chloride. Knock-out van dit gen resulteert in een aanleg voor hypertensie. Muizen met een tekort aan dit eiwit ontwikkelen hypertensie bij blootstelling aan een hoge natriumchloridebelasting.18 Hoewel de Slc26a9-transporter een belangrijke rol lijkt te spelen bij het verwerken van grote hoeveelheden natriumchloride, blijft de regulatie van de activiteit van de transporter in reactie op wisselende natriumchloridebelastingen onbekend.

(A) Chloride kan worden uitgescheiden of geabsorbeerd in het verzamelkanaal. Een deel van de chloride-absorptie wordt aangedreven door een negatieve potentiaal in het lumen en paracellulaire beweging. (B) Transcellulaire reabsorptie van chloride kan ook plaatsvinden via koppeling van de apicale Pendrin chloride-bicarbonaat wisselaar aan de SLCA48 natrium-afhankelijke chloride-2 bicarbonaat wisselaar (NDCBE). 2 cycli van Pendrin zouden resulteren in 2 chloriden die de cel binnenkomen in ruil voor 2 bicarbonaten, terwijl NDCBE 1 natrium en 2 bicarbonaten zou transporteren in ruil voor 1 chloride eruit. Het netto resultaat zou het transport van 1 natrium en 1 chloride in de cel zijn. Verschillen in de apicale Pendrin- en NDCBE-activiteiten zouden kunnen bepalen of Cl- secretie of absorptie overheerst.
Chlorideconcentratie en hyperchloremie
Het serumchloridegehalte wordt over het algemeen gemeten als een concentratie chloride in een volume serum. De biologisch actieve chlorideconcentratie is de concentratie van vrij chloride in het plasmawater. Chloride wordt meestal gemeten met behulp van een zilverchloride-elektrode, hetzij in een direct serummonster, hetzij in een verdund serummonster.19 Bij geautomatiseerde methoden die in veel laboratoria worden gebruikt, wordt het serummonster verdund met een reagens zodat het volume van het monster een normaal watergehalte heeft en worden schattingen gemaakt op basis van de aanname van een normale verdunningsfactor. Wanneer de vaste bestanddelen van het serum zeer hoog zijn, zoals kan voorkomen bij hypertriglyceridemie en multipel myeloom, kan pseudohypochloremie optreden. Pseudohypochloremie kan ook worden waargenomen bij bromide- of jodidevergiftiging. De interactie van bromide of jodide met de zilver-chloride-elektrode genereert een grotere spanningsverandering dan chloride, waardoor de indruk wordt gewekt dat er te veel chloride in het bloed aanwezig is.20,21
Oorzaken van echte hyperchloremieHyperchloremie door waterverlies
Hyperchloremie kan het gevolg zijn van een aantal mechanismen (tabel 1). Waterverlies dat groter is dan chlorideverlies kan de chlorideconcentratie verhogen.22 Bij dehydratatie is de renale reactie om water te conserveren en de urineproductie te verlagen. Aangezien er bij ernstigere dehydratatie ook sprake kan zijn van volumedepletie, worden zowel chloride als natrium geconserveerd via een verhoogde proximale tubulaire reabsorptie van chloride en andere oplosmiddelen, en een verminderde afgifte van chloride en natrium aan meer distale nefronsegmenten. De verhoogde proximale tubulaire reabsorptie van tubulaire vloeistof en zijn inhoud zal niet noodzakelijk de chlorideconcentratie veranderen aangezien de absorptie van vloeistof isotoon gebeurt. De behandeling van watertekort bestaat uit het oordeelkundig toedienen van elektrolytvrij water, waardoor zowel de natrium- als de chlorideconcentratie zullen dalen.
Oorzaken van hyperchloremie.
Pseudohyperchloremie
Hoge hoeveelheden vaste serumbestanddelen (lipiden of eiwitten) wanneer assays met monsterverdunning worden gebruikt
Bromide- of jodidevergiftiging
Excessieve toediening van chloride
Toediening van grote volumes 0.9% (normale) natriumchlorideoplossing
Toediening van hypertonische zoutoplossing
Zoutwaterverdrinking
Netto waterverliezen
Koorts
Transpiratie
Onvoldoende water inname (slechte dorst of toegang tot water)
Diabetes insipidus
Verlies van water door overmatige elektrolyten
Bepaalde vormen van diarree
Osmotische diurese
Bepaalde gevallen van post-obstructieve diurese
Geassocieerd met metabole acidose
Bepaalde vormen van diarree
Nier tubulaire acidose
Koolzuuranhydraseremmers
Ureterale omleiding (bijv.g., ileale blaas)
Toediening van ammoniumchloride
Toediening van arginine of lysinehydrochloride
Bepaalde gevallen van chronische nieraandoeningen
Organische acidose waarbij het zuuranion snel wordt uitgescheiden (bijv, overdosis tolueen)
Respiratoire alkalose
Hyperchloremie door overmatige blootstelling aan chloride
Hyperchloremie kan optreden wanneer het lichaam wordt blootgesteld aan vloeistoffen die veel chloride bevatten. Een extreem voorbeeld hiervan is verdrinking/vergiftiging met zout water. De plotselinge grote toevoer van zeewater (het gemiddelde zoutgehalte is 3,5%) overweldigt het vermogen van de nieren om de natriumchloridebelasting uit te scheiden en hypernatriëmie en hyperchloremie komen vaak voor.23 Niettemin is een deel van de hypernatriëmie en hyperchloremie die gepaard gaan met excessieve zoutwaterinname afkomstig van vochtverliezen die gepaard gaan met diarree en urineverlies.23 De behandeling van patiënten met hyperchloremie door zoutwaterverdrinking zal afhangen van de volumestatus van de patiënt, alsmede van de inschatting van de lopende vocht- en elektrolytenverliezen en de oordeelkundige vervanging van water en elektrolyten naar behoefte.
Een minder extreem voorbeeld van hyperchloremie met een overmatige natriumchloridebelasting is de toediening van grote volumes isotone (0,9%) natriumchlorideoplossing (normale zoutoplossing) die vaak wordt gebruikt voor volumereanimatie van patiënten. Het is opmerkelijk dat wanneer een normaal persoon een grote bolus isotone zoutoplossing krijgt toegediend, het tot 2 dagen kan duren om terug te keren naar de toestand van natrium- en chloridebalans van voor de behandeling.24 Deze retentie van chloride treedt op bij blootstelling aan de suprafysiologische niveaus van chloride in normale zoutoplossing. De normale chlorideconcentratie in het plasma ligt in het bereik van 95-110meq/L, terwijl normale zoutoplossing een chlorideconcentratie heeft van 154meq/L. De relatief trage uitscheidingsreactie op isotone zoutoplossing kan verband houden met effecten van de chloridebelasting op de renale doorbloeding en op de glomerulaire filtratie (tubuloglomerulaire terugkoppeling). Hoewel down-regulation van chloride reabsorptieve transporter activiteiten optreedt bij natriumchloride belasting,14,25,26 is de snelheid van de reductie van deze transporters niet goed gedefinieerd.
Bij isotone zouttoediening kan de bicarbonaatconcentratie ook dalen als de chlorideconcentratie toeneemt. Naast verdunning van het plasma-bicarbonaat bij toediening van suprafysiologische chloridehoudende, basevrije oplossingen zoals normale zoutoplossing, kunnen ook andere factoren een rol spelen bij de daling van het bicarbonaat- en de stijging van het chloridegehalte. Verlies van urinebicarbonaat kan bijdragen aan de daling van het serumbicarbonaatgehalte, omdat de reabsorptiedrempel voor bicarbonaat bij volume-expansie lager kan zijn.27 Dit verlies van bicarbonaat kan zelfs optreden als de serumbicarbonaatconcentratie laag is.27 In studies bij mensen is het verlies van natrium en kalium gedurende de eerste 24 uur na toediening van een infusie van isotone zoutoplossing groter dan het verlies van chloride. De verminderde uitscheiding van chloride in vergelijking met natrium en kalium suggereert het urineverlies van andere anionen zoals bicarbonaat en andere organische anionen die ook kunnen bijdragen tot een daling van de serumbicarbonaatconcentratie.24 Het gebruik van evenwichtige elektrolytenoplossingen die basen of basenequivalenten en chlorideconcentraties bevatten die meer fysiologisch zijn, kan niet alleen de ontwikkeling van hyperchloremische acidose voorkomen, maar kan ook enkele van de mogelijke schadelijke effecten vermijden die geassocieerd worden met hyperchloremische oplossingen zoals normale zoutoplossing.28,29 In vergelijking met evenwichtige, basische zoutoplossingen resulteerde de toediening van normale zoutoplossing aan gezonde menselijke proefpersonen in een daling van de renale bloedstroom en corticale perfusie30 , hetgeen bezorgdheid doet ontstaan over de overmatige toediening van normale zoutoplossing bij volume reanimatie bij patiënten. Niettemin kunnen bepaalde klinische situaties het gebruik van normale zoutoplossing bevorderen, onder meer bij patiënten met hypochloremische metabole alkalose of patiënten met hersenoedeem.
Hyperchloremie met metabole acidose
Hyperchloremie treedt ook op wanneer zoutzuur (HCl) aan het bloed wordt toegevoegd. HCl wordt zelden gegeven als een directe verzurende stof, maar kan ontstaan uit het metabolisme van ammoniumchloride of kationische aminozuren zoals lysine en arginine.31 De aanmaak van HCl leidt tot een reactie van H+ met HCO3- die leidt tot CO2-productie en een nettoverlies van HCO3- en stijging van de chlorideconcentratie.
Met de ademhaling gaat getitreerd bicarbonaat als CO2 uit het lichaam verloren.
Dus voor elk milli-equivalent HCl dat wordt toegevoegd, wordt een milli-equivalent bicarbonaat verbruikt en omgezet in CO2, zodat het chloridegehalte in dezelfde mate stijgt als het bicarbonaatgehalte daalt.
Renale tubulaire acidosen (proximale RTA type 2 en distale RTA type 1 of 4) resulteren in hyperchloremische metabole acidose. Bij proximale RTA (type 2) is de bicarbonaatreabsorptie in de proximale tubulus verstoord, wat leidt tot verhoogde verliezen van bicarbonaat uit dit segment. Er is ook enige verstoring van de chloride reabsorptie omdat het ontbreken van de extractie van bicarbonaat de normale stijging van de luminale chlorideconcentratie verhindert. Niettemin is in proximale RTA de vermindering van het bicarbonaat transport groter dan de vermindering van het chloride transport, zodat er relatief meer chloride dan bicarbonaat wordt gereabsorbeerd. Als remming van koolzuuranhydrase wordt gebruikt als model voor proximale RTA, lijkt de chloride reabsorptie minder aangetast dan de bicarbonaat reabsorptie, zoals blijkt uit een relatief bescheiden toename van de uitscheiding van chloride in de urine, terwijl de uitscheiding van natrium, kalium en, vermoedelijk, bicarbonaat duidelijk is toegenomen.32
In klassieke distale RTA (type 1) of type 4 RTA verhindert de vermindering van de netto zuursecretie de renale aanmaak van nieuw bicarbonaat door de uitscheiding van ammonium en/of titreerbaar zuur te belemmeren. Als gevolg hiervan leidt het door metabolisme gegenereerde HCl tot een daling van het bicarbonaat die niet wordt gecompenseerd door de aanmaak en het behoud van bicarbonaat en de uitscheiding van chloride. Zolang de nierfunctie in stand wordt gehouden, stapelen de niet-chloridezuuranionen zich niet op in de systemische circulatie, waardoor de anionkloof relatief normaal blijft. De renale excretie van fosfaat- en sulfaatanionen, gegenereerd uit het metabolisme van fosfor- en zwavelhoudende aminozuren31 , wordt zelfs gestimuleerd door acidose.33
Een andere oorzaak van hyperchloremische metabole acidose treedt op bij diarree. In veel segmenten van het maagdarmkanaal en bijbehorende exocriene organen zoals de alvleesklier, wordt bicarbonaat in de darm uitgescheiden in ruil voor chloride, zodat verlies van bicarbonaat, vooral bij secretoire vormen van diarree, gepaard kan gaan met bicarbonaatverliezen die gepaard gaan met chloride-retentie.34
Repair van hyperchloremische vormen van metabole acidose houdt in dat de lopende oorzaak van bicarbonaatverlies of HCl-vorming wordt gestopt terwijl de patiënt bicarbonaat of base-equivalenten (bijv. citraat) krijgt toegediend of dat de nieren van de patiënt bicarbonaat kunnen regenereren als de nierfunctie relatief normaal is. Tijdens het ontstaan van een metabole acidose zijn er aanvankelijk netto natriumverliezen en volumevermindering. Bij langduriger acidose kan natriumretentie optreden als gevolg van hoge aldosteronspiegels en upregulatie van ENaC in de verzamelbuis.35 Bij toediening van bicarbonaat om de acidose te corrigeren, wordt bicarbonaat in de proximale tubulus vastgehouden en wordt ook de normale chlorideherabsorptie hersteld. De daarmee gepaard gaande volume-expansie met bicarbonaat kan bijdragen tot de daling van het chloridegehalte. Wanneer de nieren de metabole acidose herstellen, wordt ammoniumchloride in de urine uitgescheiden, terwijl bicarbonaat, dat in de proximale tubulus wordt aangemaakt als bijproduct van het glutaminemetabolisme, weer in het bloed terechtkomt.
Lijst van hoofdpunten
-
De nier speelt een sleutelrol bij het handhaven van de chloridebalans in het lichaam. Hoewel renaal choridetransport gekoppeld is aan natriumtransport, kan choridetransport soms afwijken van natriumtransport.
-
Hyperchloremie kan het gevolg zijn van verschillende aandoeningen, waaronder watergebrek, overmatige blootstelling aan chloride en metabole acidose.
-
De pathogene oorzaak van hyperchloremie zal richting geven aan hoe de stoornis moet worden behandeld: waterdepletie wordt behandeld met oordeelkundige watersuppletie; overmatige chloortoediening door het onthouden van verdere chloortoediening; en hyperchloremische metabole acidose door het geven van bicarbonaat.
Conflict of interest
De auteur verklaart geen belangenconflict.