Abstract
Arseen stimuleert de proliferatie bij lage concentraties en remt de celgroei bij hoge concentraties, wat een bifasisch effect op het biologisch proces aantoont. Het bifasisch effect vereist dat de arseenconcentratie op een geschikte drempel wordt gehouden om de kankercellen tijdens chemotherapie te remmen. De apoptose kan een primair mechanisme zijn dat verband houdt met de dubbele eigenschappen van het arsenicum.
Key words
arsenicum, bifasisch effect, endemisch arsenisme, carcinogenese, chemotherapie
Highlights
- Arsenicum is een carcinogeen dat bij lage concentraties de celproliferatie kan stimuleren.
- Ook is arseen een kankeronderdrukker die bij hoge concentraties de celgroei remt.
- De biologische rol van arseen vertoont een bifasisch effect op de celgroei.
- Apoptose kan een potentieel mechanisme zijn dat verband houdt met de dubbele eigenschappen van het arseen.
Commentaar
Het element arseen (As) is wijdverspreid in de natuur, en wordt vaak gecombineerd met zuurstof of zwavel om verbindingen te vormen. Het arseen is ook nauw verbonden met het biologische proces. De pathofysiologische kenmerken ervan zijn verwerkt in de volgende aspecten: (a) lage doses arseen stimuleren de celproliferatie en de carcinogenese. Wanneer natriumarseniet gebruikt werd om menselijke HepG2 kankercellen of niet-tumor HHI-5 hepatocyten te behandelen, stelden we vast dat het percentage celdood negatief was in de beginfase, wat betekent dat de lage dosis arseniet de celgroei bevordert (Figuur 1). Het arsenicum kon de levensvatbaarheid van de cellen verbeteren bij een smal bereik van lage concentraties. Naarmate het arsenietgehalte werd verhoogd om een kritiek punt te bereiken, begon het de proliferatie te remmen en de celdood te versnellen. Dit consistente resultaat werd ook door andere studies gerapporteerd. In verschillende geologische regio’s overschrijdt de arseenconcentratie in drinkwater het standaardgehalte (0,01mg/L) dat door de Wereldgezondheidsorganisatie wordt aanbevolen. De plaatselijke bewoners die het met arseen verrijkte water drinken, lijden aan endemisch arsenisme. De incidentie van kanker in verschillende organen (b.v. huid, longen, nieren, urineblaas, lever, enz.) in de endemische gebieden is aanzienlijk hoger dan die in niet-endemische gebieden. Arseen is door het Internationaal Instituut voor Kankeronderzoek aangemerkt als kankerverwekkend voor de mens; b) een hoge concentratie arseen remt de celgroei. In de klinische praktijk worden arseenverbindingen (d.w.z. As2O3, As2S2, enz.) algemeen gebruikt om kankercellen tijdens chemotherapie te doden. Bovendien is arsenide het eerstelijnsmedicijn geweest voor de behandeling van sommige kankers zoals leukemie en solide viscerale neoplasma. Soms worden de arseenverbindingen in combinatie met andere geneesmiddelen gebruikt om het beste therapeutische effect te verkrijgen. Het arsenicum induceert niet alleen de ontwikkeling van tumoren, maar doodt ook kankercellen als basisgeneesmiddel in de klinische behandeling. Het arsenicum heeft dubbele eigenschappen van carcinogeen en kankersuppressor. Aldus wordt een nieuw concept “bifasisch effect” voorgesteld om zijn bidirectionele rol in celgroei te beschrijven.
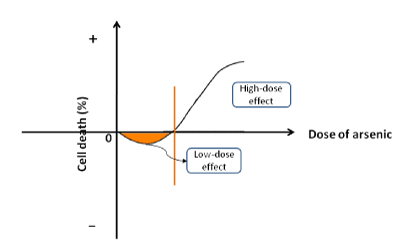
Figuur 1. Schematisch diagram van het bifasisch effect. Het arseen stimuleert de celproliferatie bij lage doses, terwijl het de celdood versnelt bij hoge concentraties
Wat is het exacte mechanisme dat aanleiding geeft tot de dubbele eigenschappen van het arseen? Momenteel is er geen duidelijk antwoord op deze vraag. De beschikbare gegevens ondersteunen echter dat apoptose een cruciale rol speelt. Apoptose is een door genen gecontroleerd, energieverslindend, suïcidaal proces om de weefselstructuur in stand te houden. Een evenwicht tussen apoptotische en anti-apoptotische competenties bepaalt niet alleen de levensvatbaarheid van de cellen, maar beïnvloedt ook rechtstreeks de weefselfunctie. Tot dusver werd apoptose beschouwd als het voornaamste mechanisme om carcinogenese en kankeronderdrukking met elkaar te verbinden. Inhibitor of apoptosis proteins (IAPs) hebben een krachtige functie in het reguleren van celoverleving en het controleren van apoptose cascade. Bovendien wordt de expressie van IAPs gemoduleerd door meerdere nucleaire factoren, zoals NF-kappa B, FoxA2, C/EBP-beta enzovoort. Het verband tussen arseen en apoptose is een zorgvuldig onderzoek waard. We hebben meer bewijzen nodig om aan te tonen dat (a) lage-dosis arsenicum apoptose remt en celproliferatie stimuleert. Het is algemeen bekend dat de carcinogenese de weerstand van apoptose moet overwinnen; (b) hoge-dosis arsenicum apoptose in gang zet en kankercellen doodt. De belangrijkste strategie voor de behandeling van kanker is het induceren van apoptose van kankercellen. Een redelijke hypothese is dat arseen apoptose remt bij lage concentraties, terwijl het apoptose bevordert bij hoge concentraties. Er wordt ook gespeculeerd dat IAPs en hun regulerende netwerk verantwoordelijk kunnen zijn voor de dubbele eigenschappen van arsenicum.
Een onderzoek naar het bifasische effect van arsenicum (arsenicum) is van bijzonder belang voor de klinische behandeling van de kanker. Wanneer arseenverbinding samen met andere geneesmiddelen wordt toegediend, wordt de dosering van de arseenverbindingen vaak verlaagd. Wegens de dubbele eigenschappen van arseen moet men de medicinale waarde van de arseenverbinding evalueren wanneer men geneesmiddelen in combinatie neemt. Op dit moment moet de lokale concentratie van arsenide op een specifiek niveau worden gehouden om de apoptose van kankercellen te induceren. Anders kan het arsenide de proliferatie van kankercellen bevorderen. Er is geen enkel therapeutisch effect, zelfs een tegengestelde uitkomst. Daarom moeten wij rekening houden met een bidirectionele reactie van het arsenide, vooral in combinatie met andere geneesmiddelen. Wat is de exacte drempel voor arsenide om de tumor te remmen? Hoe moet het arsenide worden toegediend om de drempelconcentratie te bereiken en deze constant te houden? Welke biomarkers zijn redelijk om de concentratie van arsenide in het bloed te controleren? Tot op heden zijn er geen antwoorden op bovenstaande vragen. Biologische kenmerken van arseen vormen ook een nieuw onderwerp voor de toxicologie. In de traditionele definitie van toxicologie wordt het doden van cellen of het verhogen van het sterftecijfer over het algemeen beschouwd als toxicologisch gedrag. Het stimuleren van de proliferatie van kankercellen is echter ook giftig voor het lichaam. Dus het gedrag van lage-dosis arsenicum is een ander aspect van toxicologie. Misschien kan het gedefinieerd worden als inverse toxicologie of omgekeerde toxicologie. Momenteel werken wij aan moleculaire markers die de concentratie van arsenicum in het bloed kunnen schatten en het therapeutische effect ervan kunnen evalueren. Leukemie en vaste tumoren kunnen verschillende concentraties arsenicummedicijnen vereisen (4). Klinische trials in grote steekproeven zijn nodig om de ware rol van arsenide bij de behandeling van verschillende kankers te testen. Bovendien is de kwantificering van de functionele toestand van cellen het huidige aandachtspunt.
Samenvattend heeft het arseen een bifasisch effect op de celgroei, dat zich manifesteert door de proliferatie bij lage concentraties en de remming bij hoge concentraties. Vanwege het bifasische effect moet een drempelwaarde van de arseenconcentratie worden aangehouden om kankercellen tijdens de behandeling van kanker te doden. Anders kan het arsenide de proliferatie van kankercellen stimuleren, waardoor een averechts effect wordt bereikt. Voorlopige studies tonen aan dat de anti-apoptotische IAPs familie en haar regulatorisch netwerk een belangrijke rol spelen in de arsenicum biologie. De apoptose kan een essentieel mechanisme zijn dat verband houdt met de dubbele eigenschappen van het arseen.
Belangenverklaring
De auteurs hebben niets te onthullen.
Acknowledgments
Dit werk werd ondersteund door “The National Natural Science Foundation of China”, projectnummer 81773367. Wij danken professor Yang Jianbo’s suggestie en advies bij de voorbereiding van het manuscript.
- Yedjou C, Tchounwou P, Jenkins J, McMurray R (2010) Basismechanismen van arseentrioxide (ATO)-geïnduceerde apoptose in menselijke leukemie (HL-60) cellen. J Hematol Oncol 3: 28.
- Tseng CH, Chong CK, Tseng CP, Centeno JA (2007) Blackfoot disease in Taiwan: its link with inorganic arsenic exposure from drinking water. Ambio. 36: 82-84.
- Smith AH, Marshall G, Roh T, Ferreccio C, Liaw J, et al. (2018) Lung, blaas, and kidney cancer mortality 40 years after arsenic exposure reduction. Journal of the National Cancer Institute 110: 241-249.
- Gill H, Yim R, Lee HKK, Mak V, Lin SY, et al. (2018) Langetermijnuitkomsten van recidiverende acute promyelocytische leukemie behandeld met orale arseentrioxide-gebaseerde reïnductie- en onderhoudsregimes: Een 15-jarig prospectief onderzoek. Cancer 124: 2316-2326.
- Varfolomeev E, Blankenship JW, Wayson SM, Fedorova AV, Kayagaki N, et al. (2007) IAP antagonisten induceren autoubiquitinatie van c-IAPs, NF-kappaB activatie, en TNFalpha afhankelijke apoptose. Cell 131: 669-681.