Triacylglyceride/Phospholipid Stereochemistry
グリセリンはC2が二つの同じ置換基、-CH2OHを持っているので不斉分子と呼ばれる。 体内のグリセロールは化学的にトリアシルグリセリドやリン脂質(PL)に変換されますが、これらはキラルであり、1つのエナンチオマーで存在します。 グリセロール上の2つのCH2OH基が同一であるにもかかわらず、なぜこのようなことが可能なのだろうか? 実は、グリセリン上の2つのCH2OH基は立体化学的に等価であるにもかかわらず、次のように区別することができるのです。 C2上のOHが左を向くようにグリセロールを配向させる。 次にC1のOHをODに置き換える。ここでDは重水素である。 これでC1とC3上の2つのアルコール置換基は同一ではなくなり、結果として分子はキラルとなる。 C2上のHが背面を向くように分子を回転させ、C2上の他の置換基に以下のように優先順位をつけると、キラルになる。 OH = 1, DOCH2 = 2, CH2OH = 3 とすると、この分子はS配位であることがわかる。 従って、C1がproS炭素であると言う。 同様に、C3上のOHをODに置き換えると、Rエナンチオマーを形成することになります。 従って、C3はproR炭素である。 このように、現実には2つの同じCH2OH置換基を区別することができるのです。 グリセロールはキラルではなく、プロキラルであると言います。 (グリセロールは2つの同じ置換基のうち1つを変更することでキラルになる可能性がある、と考えてください)
図: グリセロール-プロキラル分子
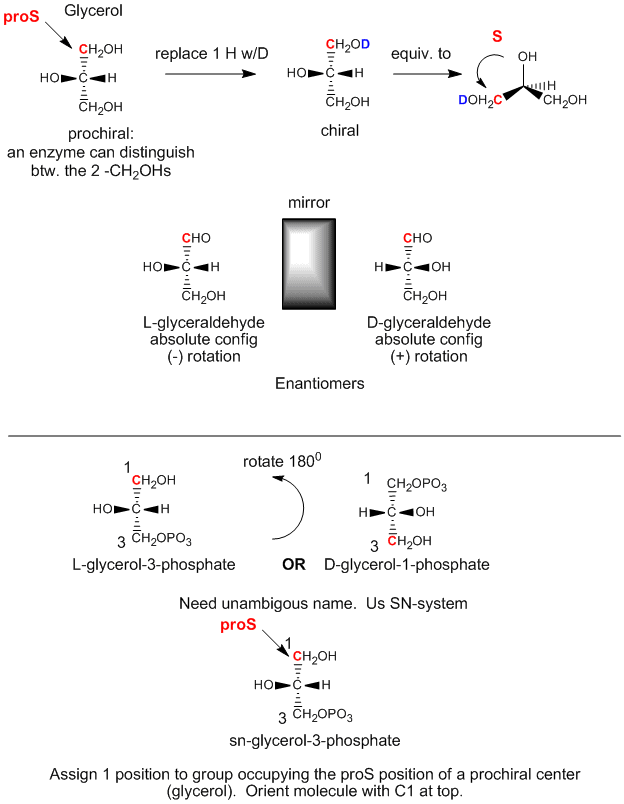
上のグリセロールの構成(C2上のOHが左を向いているとき)を、別の3Cグリセロール誘導体の単純糖(ポリヒドロキシアルデヒドまたはケトン)、L-グリセルアルデヒドの絶対配置と関連づけることができます。 この分子はC2上のOH(唯一の不斉炭素)が左を向いたキラルである。 L糖の場合、最後の不斉炭素上のOHが左を向いていることは簡単に思い出せる。 L-グリセルアルデヒドのエナンチオマー(鏡像異性体)はD-グリセルアルデヒドで、C2上のOHは右を向いている。 生化学者は脂質、糖、アミノ酸の立体化学について、有機化学で用いたR,S命名法の代わりにL,Dを用います。 すべての糖、アミノ酸、グリセロ脂質の立体化学的呼称は、L-およびD-グリセルアルデヒドの絶対配置から決定することができる。
アキラルなグリセロールからキラルな誘導体を生体内(体内)で合成するには、まずC3上のOHをATP(優れたアセチル化剤である無水酢酸に構造が似ているリン酸無水物)でリン酸化してキラル分子グリセロールリン酸を生成します。 L-グリセルアルデヒドの絶対配置から、これを用いてグリセロールを描くと(C2上のOHが左向きになる)、リン酸化された分子はL-グリセロール-3-リン酸と名付けられることが分かる。 しかし、この分子を180度回転させると、分子の立体化学は変えずに、上記のD/L命名法を用いて、回転した分子をD-グリセロール-1-リン酸と命名することになります。 同じ分子に2つの異なる名前をつけることはできない。 そこで生化学者は、プロキラル分子の1位の基をプロSの位置に割り当てる立体特異的番号付けシステム(sn)を開発した。 この命名法を用いると、先ほどのグリセロールリン酸はsn-glycerol-3-phosphateと一義的に命名されることがわかる。 proR炭素上の水酸基置換基はリン酸化されていた<4209><3388>Fig: プロキラルグリセロールからのトリアシルグリセリドとホスファチジン酸の生物学的合成
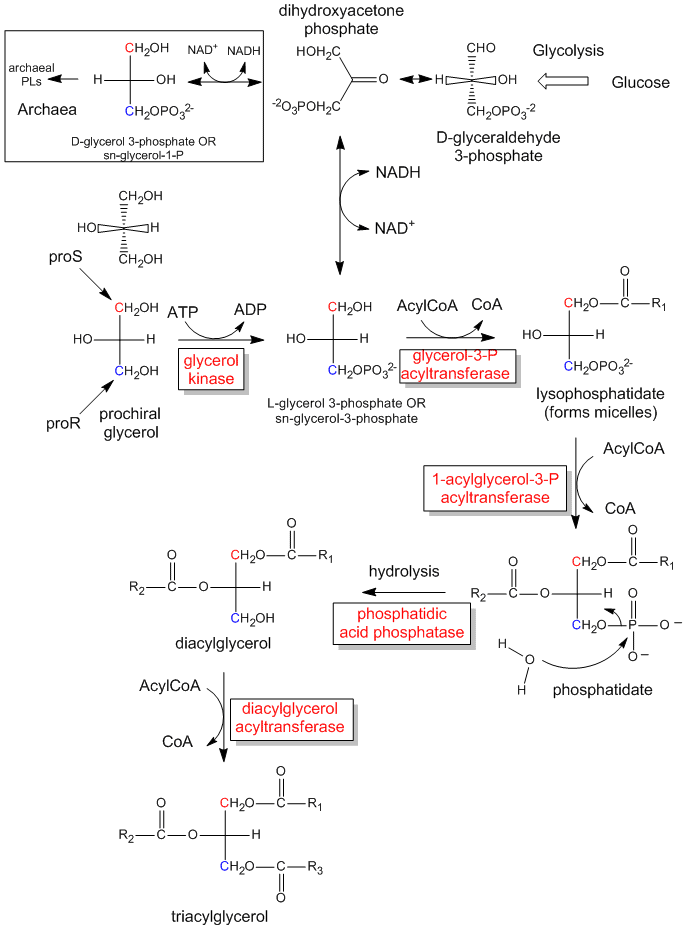
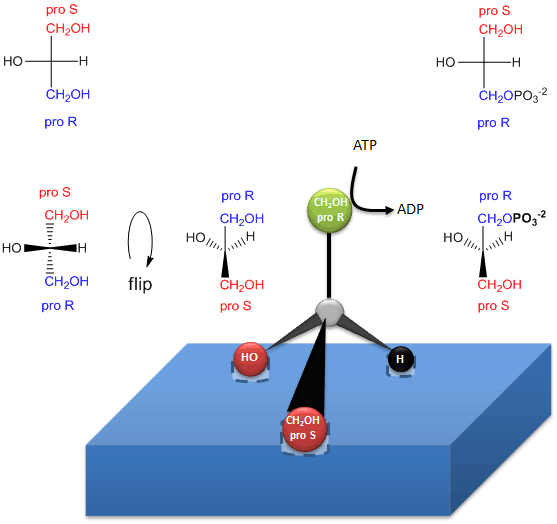
プロキラルグリセロールがproR炭素のOHで酵素的にリン酸化されてsn-グリセロール-3-リン酸になる様子を下のリンクに示す。 2つの同じCH2OH置換基がproSまたはproR炭素のどちらを含むか区別できたように、酵素も区別することができます。 酵素は、プロキラル分子が酵素と3点で相互作用すれば、プロキラル分子上の同一の置換基を区別することができる。 プロキラル反応物/酵素系のもう一つの例として、プロキラル分子であるエタノールをアルコールデヒドロゲナーゼという酵素で酸化する場合がある。この場合、C2上の2つのHのうちプロR Hだけが取り除かれる。 (これについては後述します。)
図. キラルトリアシルグリセロールとホスファチジン酸の生成時に、酵素(グリセロールキナーゼ)がATPからグリセロールのproR CH2OHにPO4を移動させる様子