Nome generico: loperamide hydrochloride
Forma farmaceutica: capsule
Medicamente rivisto da Drugs.com. Ultimo aggiornamento il 22 gennaio 2021.
- Panoramica
- Effetti collaterali
- Dosaggio
- Professionale
- Interazioni
- Più
- Descrizione Imodium
- Imodium – Farmacologia clinica
- Indicazioni e uso di Imodium
- Contraindicazioni
- Avvertenze
- Precauzioni
- Generale
- Informazioni per i pazienti
- Interazioni farmacologiche
- Carcinogenesi, mutagenesi, compromissione della fertilità
- Gravidanza
- Categoria di gravidanza C
- Madri che allattano
- Uso pediatrico
- Reazioni avverse
- Dati degli studi clinici
- Esperienza post-marketing
- Abuso e dipendenza da droghe
- Abuso
- Dipendenza
- Sovradosaggio
- Dosaggio e amministrazione dell’emodio
- Diarrea acuta
- Diarrea cronica
- Bambini sotto i 2 anni
- Anziani
- Malattia renale
- Malattia epatica
- Come viene fornito Imodium
- Domande frequenti
- Più informazioni su Imodium (loperamide)
- Risorse per i consumatori
- Risorse professionali
- Altre formulazioni
- Guide al trattamento correlate
Descrizione Imodium
Imodium® (loperamide cloridrato), 4-(p-clorofenil)-4-idrossi-N,N-dimetil-a,a-difenil-1-piperidinebutyramide monoidrocloride, è un antidiarroico sintetico per uso orale.
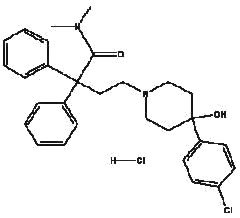
Imodium® è disponibile in capsule da 2 mg.
Gli ingredienti inattivi sono: Lattosio, amido di mais, talco e magnesio stearato. Le capsule di Imodium® contengono FD&C Yellow No. 6.
Imodium – Farmacologia clinica
Studi in vitro e su animali mostrano che Imodium® (cloridrato di loperamide) agisce rallentando la motilità intestinale e influenzando il movimento di acqua ed elettroliti attraverso l’intestino. La loperamide si lega al recettore degli oppiacei nella parete intestinale. Di conseguenza, inibisce il rilascio di acetilcolina e prostaglandine, riducendo così la peristalsi e aumentando il tempo di transito intestinale. La loperamide aumenta il tono dello sfintere anale, riducendo così l’incontinenza e l’urgenza.
Nell’uomo, Imodium® prolunga il tempo di transito del contenuto intestinale. Riduce il volume fecale giornaliero, aumenta la viscosità e la densità di massa, e diminuisce la perdita di liquidi ed elettroliti. La tolleranza all’effetto antidiarroico non è stata osservata. Gli studi clinici hanno indicato che l’emivita di eliminazione apparente della loperamide nell’uomo è di 10,8 ore con un intervallo di 9,1 – 14,4 ore. I livelli plasmatici di farmaco invariato rimangono sotto i 2 nanogrammi per mL dopo l’assunzione di una capsula da 2 mg di Imodium®. I livelli plasmatici sono più alti circa cinque ore dopo la somministrazione della capsula e 2,5 ore dopo il liquido. I livelli plasmatici di picco di loperamide erano simili per entrambe le formulazioni. L’eliminazione della loperamide avviene principalmente per N-demetilazione ossidativa. Gli isozimi del citocromo P450 (CYP450), CYP2C8 e CYP3A4, sono ritenuti svolgere un ruolo importante nel processo di N-demetilazione della loperamide, poiché la quercetina (inibitore CYP2C8) e il ketoconazolo (inibitore CYP3A4) hanno inibito significativamente il processo di N-demetilazione in vitro rispettivamente del 40% e del 90%. Inoltre, il CYP2B6 e il CYP2D6 sembrano svolgere un ruolo minore nella N-demetilazione della loperamide. L’escrezione della loperamide invariata e dei suoi metaboliti avviene principalmente attraverso le feci. Nei pazienti in cui i parametri biochimici ed ematologici sono stati monitorati durante gli studi clinici, non è stata notata alcuna tendenza all’anomalia durante la terapia con Imodium®. Allo stesso modo, le analisi delle urine, l’elettrocardiogramma e gli esami clinici oftalmologici non hanno mostrato tendenze verso l’anormalità.
Indicazioni e uso di Imodium
Imodium® (cloridrato di loperamide) è indicato per il controllo e il sollievo sintomatico della diarrea acuta non specifica e della diarrea cronica associata alle malattie infiammatorie intestinali. Imodium® è anche indicato per ridurre il volume di scarico dalle ileostomie.
Contraindicazioni
Imodium è controindicato nei pazienti con ipersensibilità nota al cloridrato di loperamide o a qualsiasi eccipiente.
Imodium è controindicato nei pazienti con dolore addominale in assenza di diarrea.
Imodium non è raccomandato nei bambini sotto i 24 mesi di età.
Imodium non deve essere usato come terapia primaria:
– nei pazienti con dissenteria acuta, che è caratterizzata da sangue nelle feci e febbre alta, – nei pazienti con colite ulcerosa acuta, – nei pazienti con enterocolite batterica causata da organismi invasivi tra cui Salmonella, Shigella e Campylobacter, – nei pazienti con colite pseudomembranosa associata all’uso di antibiotici ad ampio spettro.
Avvertenze
La deplezione di fluidi ed elettroliti si verifica spesso in pazienti che hanno diarrea. In tali casi, la somministrazione di liquidi ed elettroliti appropriati è molto importante. L’uso di Imodium® non preclude la necessità di un’appropriata terapia con fluidi ed elettroliti.
In generale, Imodium non deve essere usato quando si deve evitare l’inibizione della peristalsi a causa del possibile rischio di sequele significative tra cui ileo, megacolon e megacolon tossico. Imodium deve essere interrotto prontamente quando si sviluppano costipazione, distensione addominale o ileo.
Il trattamento della diarrea con Imodium è solo sintomatico. Ogni volta che un’eziologia sottostante può essere determinata, il trattamento specifico dovrebbe essere dato quando appropriato (o quando indicato).
I pazienti con AIDS trattati con Imodium per la diarrea dovrebbero avere la terapia interrotta ai primi segni di distensione addominale. Ci sono state segnalazioni isolate di megacolon tossico in pazienti con AIDS con colite infettiva da patogeni sia virali che batterici trattati con loperamide cloridrato.
Imodium® deve essere usato con particolare cautela nei bambini piccoli a causa della maggiore variabilità della risposta in questo gruppo di età. La disidratazione, in particolare nei bambini più piccoli, può influenzare ulteriormente la variabilità della risposta a Imodium®.
Precauzioni
Generale
Sono state riportate reazioni allergiche estremamente rare, incluse anafilassi e shock anafilattico. Nella diarrea acuta, se non si osserva un miglioramento clinico entro 48 ore, la somministrazione di Imodium® (loperamide cloridrato) deve essere interrotta e i pazienti devono essere invitati a consultare il proprio medico. Sebbene non siano disponibili dati farmacocinetici in pazienti con insufficienza epatica, Imodium deve essere usato con cautela in tali pazienti a causa del ridotto metabolismo di primo passaggio. I pazienti con disfunzione epatica devono essere monitorati attentamente per i segni di tossicità del SNC. Non sono disponibili dati farmacocinetici in pazienti con insufficienza renale. Poiché è stato riportato che la maggior parte del farmaco viene metabolizzata e i metaboliti o il farmaco invariato vengono escreti principalmente nelle feci, non sono richiesti aggiustamenti del dosaggio nei pazienti con insufficienza renale. Non sono stati condotti studi formali per valutare la farmacocinetica della loperamide in soggetti anziani. Tuttavia, in due studi che hanno arruolato pazienti anziani, non ci sono state grandi differenze nella disposizione del farmaco in pazienti anziani con diarrea rispetto ai pazienti giovani.
Informazioni per i pazienti
I pazienti devono essere avvisati di controllare con il loro medico se la loro diarrea non migliora in 48 ore o se notano sangue nelle loro feci, sviluppano una febbre o sviluppano distensione addominale. Stanchezza, vertigini o sonnolenza possono verificarsi nell’ambito delle sindromi diarroiche trattate con Imodium. Pertanto, si consiglia di usare cautela quando si guida una macchina o si utilizzano macchinari. (vedi Reazioni avverse).
Interazioni farmacologiche
Dati non clinici hanno dimostrato che la loperamide è un substrato della P-glicoproteina. La somministrazione concomitante di loperamide (16 mg in dose singola) con una dose singola di 600 mg di chinidina o ritonavir, entrambi inibitori della P-glicoproteina, ha portato ad un aumento da 2 a 3 volte dei livelli plasmatici di loperamide. A causa del potenziale aumento degli effetti centrali quando la loperamide è co-somministrata con chinidina e con ritonavir, si deve esercitare cautela quando la loperamide è somministrata ai dosaggi raccomandati (2 mg, fino a 16 mg di dose massima giornaliera) con inibitori della P-glicoproteina.
Quando una singola dose da 16 mg di loperamide viene co-somministrata con una dose singola da 600 mg di saquinavir, la loperamide ha diminuito l’esposizione al saquinavir del 54%, che può essere di rilevanza clinica a causa della riduzione dell’efficacia terapeutica del saquinavir. L’effetto del saquinavir sulla loperamide è di minore rilevanza clinica. Pertanto, quando la loperamide viene somministrata con saquinavir, l’efficacia terapeutica di saquinavir dovrebbe essere strettamente monitorata.
Carcinogenesi, mutagenesi, compromissione della fertilità
In uno studio di 18 mesi sui ratti con dosi orali fino a 40 mg/kg/giorno (21 volte la dose umana massima di 16 mg/giorno, basata sul confronto della superficie del corpo), non c’era evidenza di carcinogenesi.
La loperamide non è risultata genotossica nel test di Ames, nel cromotest SOS in E. coli, nel test letale dominante in topi femmina o nel test di trasformazione delle cellule embrionali del topo.
La fertilità e le prestazioni riproduttive sono state valutate nei ratti utilizzando dosi orali di 2,5, 10 e 40 mg/kg/giorno (solo femmine) in un secondo studio. La somministrazione orale di 20 mg/kg/giorno (circa 11 volte la dose umana basata su un confronto della superficie corporea) e superiore ha prodotto una forte compromissione della fertilità femminile. Il trattamento di ratti femmina con fino a 10 mg/kg/giorno per bocca (circa 5 volte la dose umana basata su un confronto della superficie corporea) non ha avuto effetti sulla fertilità. Il trattamento di ratti maschi con 40 mg/kg/giorno per bocca (circa 21 volte la dose umana basata su un confronto della superficie corporea) ha prodotto un deterioramento della fertilità maschile, mentre la somministrazione di fino a 10 mg/kg/giorno (circa 5 volte la dose umana basata su un confronto della superficie corporea) non ha avuto alcun effetto.
Gravidanza
Effetti teratogeni
Categoria di gravidanza C
Sono stati eseguiti studi di teratologia nei ratti con dosi orali di 2,5, 10 e 40 mg/kg/giorno e nei conigli con dosi orali di 5, 20 e 40 mg/kg/giorno. Questi studi non hanno rivelato alcuna prova di compromissione della fertilità o danni al feto a dosi fino a 10 mg/kg/giorno nei ratti (5 volte la dose umana basata sul confronto della superficie corporea) e 40 mg/kg/giorno nei conigli (43 volte la dose umana basata sul confronto della superficie corporea). Il trattamento dei ratti con 40 mg/kg/giorno per bocca (21 volte la dose umana basata su un confronto della superficie corporea) ha prodotto una marcata compromissione della fertilità. Gli studi non hanno prodotto alcuna prova di attività teratogena. Non ci sono studi adeguati e ben controllati in donne incinte. La loperamide dovrebbe essere usata durante la gravidanza solo se il potenziale beneficio giustifica il potenziale rischio per il feto.
Effetti non teratogeni
In uno studio sulla riproduzione peri- e post-natale nei ratti, la somministrazione orale di 40 mg/kg/giorno ha prodotto una riduzione della crescita e della sopravvivenza della prole.
Madri che allattano
Piccole quantità di loperamide possono comparire nel latte materno umano. Pertanto, Imodium non è raccomandato durante l’allattamento.
Uso pediatrico
Vedere la sezione “Avvertenze” per informazioni sulla maggiore variabilità di risposta in questo gruppo di età. In caso di sovradosaggio accidentale di Imodium® da parte dei bambini, vedere la sezione “Sovradosaggio” per il trattamento suggerito.
Reazioni avverse
Dati degli studi clinici
Gli effetti avversi riportati durante le indagini cliniche di Imodium® (loperamide cloridrato) sono difficili da distinguere dai sintomi associati alla sindrome diarroica. Le esperienze avverse registrate durante gli studi clinici con Imodium® erano generalmente di natura minore e autolimitante. Sono stati osservati più comunemente durante il trattamento della diarrea cronica.
Gli eventi avversi riportati sono riassunti indipendentemente dalla valutazione di causalità degli investigatori.
1) Eventi avversi da 4 studi controllati con placebo in pazienti con diarrea acuta
Gli eventi avversi con un’incidenza di 1.0% o superiore, che sono stati segnalati almeno con la stessa frequenza nei pazienti che assumono loperamide cloridrato rispetto al placebo, sono presentati nella tabella sottostante.
| Diarrea acuta | ||
|---|---|---|
| Cloridrato di loperamide | Placebo | |
| No. di pazienti trattati | 231 | 236 |
| AE gastrointestinale% | ||
| Costituzione | 2,6% | 0.8% |
Gli eventi avversi con un’incidenza dell’1,0% o superiore, che sono stati riportati più frequentemente nei pazienti che assumevano placebo che loperamide cloridrato, sono stati: secchezza delle fauci, flatulenza, crampi addominali e coliche.
2) Eventi avversi da 20 studi controllati con placebo in pazienti con diarrea cronica
Gli eventi avversi con un’incidenza dell’1,0% o maggiore, che sono stati riportati almeno con la stessa frequenza nei pazienti con loperamide cloridrato che con placebo, sono presentati nella tabella sottostante.
| Diarrea cronica | ||
|---|---|---|
| Loperamide cloridrato | Placebo | |
| No. di pazienti trattati | 285 | 277 |
| AE gastrointestinale% | ||
| Constipazione | 5.3% | 0,0% |
| Sistema nervoso centrale e periferico AE% | ||
| Sbagliamento | 1,4% | 0,7% |
Gli eventi avversi con un’incidenza di 1.Gli eventi avversi con un’incidenza dell’1,0% o maggiore, che sono stati riportati più frequentemente nei pazienti trattati con placebo che con loperamide cloridrato sono stati: nausea, vomito, mal di testa, meteorismo, dolore addominale, crampi addominali e coliche.
3) Eventi avversi da settantasei studi controllati e non controllati in pazienti con diarrea acuta o cronica
Gli eventi avversi con un’incidenza dell’1.0% o maggiore nei pazienti di tutti gli studi sono riportati nella tabella sottostante.
| Diarrea acuta | Diarrea cronica | Tutti gli studi * | |
|---|---|---|---|
| * Tutti i pazienti in tutti gli studi, compresi quelli in cui non era specificato se gli eventi avversi si fossero verificati in pazienti con diarrea acuta o cronica. | |||
| No. di pazienti trattati | 1913 | 1371 | 3740 |
| Eventi avversi gastrointestinali% | |||
| Nausea | 0,7% | 3,2% | 1.8% |
| Constipazione | 1,6% | 1,9% | 1,7% |
| Crampi addominali | 0.5% | 3,0% | 1,4% |
Esperienza post-marketing
Sono stati riportati i seguenti eventi avversi:
Disturbi della pelle e del tessuto sottocutaneo
Rash, prurito, orticaria, angioedema e casi estremamente rari di eruzione bollosa incluso eritema multiforme, Sindrome di Stevens-Johnson e Necrolisi Epidermica Tossica sono stati riportati con l’uso di Imodium
Disturbi del sistema immunitario
Sono stati riportati casi isolati di reazioni allergiche e in alcuni casi gravi reazioni di ipersensibilità incluso shock anafilattico e reazioni anafilattoidi.
Disturbi gastrointestinali
Bocca secca, dolore addominale, distensione o disagio, nausea, vomito, flatulenza, dispepsia, costipazione, ileo paralitico, megacolon, incluso megacolon tossico (vedi controindicazioni e avvertenze).
Disordini renali e urinari
Ritenzione urinaria
Disordini del sistema nervoso
Sonnolenza, vertigini
Disordini generali e condizioni del sito amministrativo
Stanchezza
Un certo numero di eventi avversi riportati durante le indagini cliniche e l’esperienza post-marketing con la loperamide sono sintomi frequenti della sindrome diarroica sottostante (dolore/disagio addominale, nausea, vomito, bocca secca, stanchezza, sonnolenza, vertigini, stipsi e flatulenza). Questi sintomi sono spesso difficili da distinguere dagli effetti indesiderati della droga.
Abuso e dipendenza da droghe
Abuso
Uno studio clinico specifico progettato per valutare il potenziale di abuso della loperamide ad alte dosi ha dato come risultato un potenziale di abuso estremamente basso.
Dipendenza
Studi su scimmie dipendenti dalla morfina hanno dimostrato che la loperamide cloridrato a dosi superiori a quelle raccomandate per gli esseri umani ha impedito i segni di astinenza da morfina. Tuttavia, nell’uomo, il test pupillare di sfida al naloxone, che quando è positivo indica effetti simili agli oppiacei, eseguito dopo una singola dose elevata, o dopo più di due anni di uso terapeutico di Imodium® (cloridrato di loperamide), era negativo. Imodium® (loperamide formulata con magnesio stearato) somministrato per via orale è altamente insolubile e penetra scarsamente nel SNC.
Sovradosaggio
In caso di sovradosaggio, (incluso il sovradosaggio relativo dovuto a disfunzione epatica), possono verificarsi ritenzione urinaria, ileo paralitico e depressione del SNC. I bambini possono essere più sensibili agli effetti sul SNC rispetto agli adulti. Studi clinici hanno dimostrato che un impasto di carbone attivo somministrato subito dopo l’ingestione di cloridrato di loperamide può ridurre la quantità di farmaco che viene assorbito nella circolazione sistemica fino a nove volte. Se il vomito si verifica spontaneamente dopo l’ingestione, un impasto di 100 g di carbone attivo deve essere somministrato per via orale non appena i liquidi possono essere trattenuti.
Se il vomito non si è verificato, deve essere eseguita una lavanda gastrica seguita dalla somministrazione di 100 g di carbone attivo attraverso il tubo gastrico. In caso di sovradosaggio, i pazienti devono essere monitorati per segni di depressione del SNC per almeno 24 ore.
Se si verificano sintomi di sovradosaggio, il naloxone può essere dato come antidoto. Se risponde al naloxone, i segni vitali devono essere monitorati attentamente per la ricorrenza dei sintomi di overdose di droga per almeno 24 ore dopo l’ultima dose di naloxone.
In considerazione dell’azione prolungata della loperamide e della breve durata (da una a tre ore) del naloxone, il paziente deve essere monitorato attentamente e trattato ripetutamente con naloxone come indicato. Poiché relativamente poco farmaco viene escreto nelle urine, non ci si aspetta che la diuresi forzata sia efficace per il sovradosaggio di Imodium® (loperamide cloridrato).
Negli studi clinici un adulto che ha assunto tre dosi da 20 mg in un periodo di 24 ore ha avuto nausea dopo la seconda dose e vomitato dopo la terza dose. In studi progettati per esaminare il potenziale di effetti collaterali, l’ingestione intenzionale di fino a 60 mg di cloridrato di loperamide in una singola dose a soggetti sani non ha provocato effetti avversi significativi.
Dosaggio e amministrazione dell’emodio
(1 capsula = 2 mg)
I pazienti devono ricevere un’adeguata sostituzione di liquidi ed elettroliti secondo necessità.
Diarrea acuta
Adulti: La dose iniziale raccomandata è di 4 mg (due capsule) seguita da 2 mg (una capsula) dopo ogni feci non formate. La dose giornaliera non dovrebbe superare i 16mg (otto capsule). Il miglioramento clinico è solitamente osservato entro 48 ore.
Bambini: Nei bambini dai 2 ai 5 anni di età (20 kg o meno), dovrebbe essere usata la formulazione liquida senza prescrizione (Imodium® A-D 1 mg/7.5 mL); per l’età dai 6 ai 12 anni, possono essere usate sia Imodium® Capsules che Imodium® A-D Liquid. Per i bambini dai 2 ai 12 anni di età, il seguente schema per capsule o liquido soddisferà solitamente i requisiti di dosaggio iniziale:
Schema di dosaggio del primo giorno consigliato
Da due a cinque anni: 1 mg t.i.d. (3mg dose giornaliera) (da 13 a 20 kg)
Da sei a otto anni: 2 mg b.i.d. (4mg dose giornaliera) (da 20 a 30 kg)
Da otto a dodici anni: 2mg t.i.d. (6mg dose giornaliera) (più di 30 kg)
Dose giornaliera raccomandata successiva
Dopo il primo giorno di trattamento, si raccomanda che le dosi successive di Imodium® (1 mg/10 kg di peso corporeo) siano somministrate solo dopo una feci allentate. Il dosaggio giornaliero totale non deve superare le dosi raccomandate per il primo giorno.
Diarrea cronica
Bambini: Sebbene Imodium® sia stato studiato in un numero limitato di bambini con diarrea cronica; la dose terapeutica per il trattamento della diarrea cronica in una popolazione pediatrica non è stata stabilita.
Adulti: La dose iniziale raccomandata è di 4 mg (due capsule) seguita da 2 mg (una capsula) dopo ogni feci non formate fino a quando la diarrea è controllata, dopo di che il dosaggio di Imodium® deve essere ridotto per soddisfare le esigenze individuali. Quando il dosaggio giornaliero ottimale è stato stabilito, questa quantità può essere somministrata come dose singola o in dosi divise.
Il dosaggio medio di mantenimento giornaliero negli studi clinici era da 4 a 8 mg (da due a quattro capsule). Un dosaggio di 16 mg (otto capsule) è stato raramente superato. Se non si osserva un miglioramento clinico dopo il trattamento con 16 mg al giorno per almeno 10 giorni, è improbabile che i sintomi siano controllati da ulteriori somministrazioni. La somministrazione di Imodium® può essere continuata se la diarrea non può essere adeguatamente controllata con la dieta o con un trattamento specifico.
Bambini sotto i 2 anni
L’uso di Imodium nei bambini sotto i 2 anni non è raccomandato. Ci sono state rare segnalazioni di ileo paralitico associato a distensione addominale. La maggior parte di queste segnalazioni si sono verificate in caso di dissenteria acuta, sovradosaggio e in bambini molto piccoli con meno di due anni di età.
Anziani
Nessuno studio farmacocinetico formale è stato condotto in soggetti anziani. Tuttavia, non sono state riportate differenze importanti nella disposizione del farmaco nei pazienti anziani con diarrea rispetto ai pazienti giovani. Non è richiesto alcun aggiustamento del dosaggio negli anziani.
Malattia renale
Non sono disponibili dati farmacocinetici in pazienti con insufficienza renale. Poiché i metaboliti e il farmaco invariato sono principalmente escreti nelle feci, nessun aggiustamento del dosaggio è richiesto per i pazienti con compromissione renale (vedi sezione PRECAUZIONI).
Malattia epatica
Anche se non sono disponibili dati farmacocinetici in pazienti con compromissione epatica, Imodium deve essere usato con cautela in tali pazienti a causa del ridotto metabolismo di primo passaggio. (vedi Precauzioni).
Come viene fornito Imodium
Capsule – ogni capsula contiene 2 mg di loperamide cloridrato. Le capsule hanno un corpo verde chiaro e un cappuccio verde scuro con impresso “JANSSEN” su un segmento e “Imodium” sull’altro segmento. Le capsule di Imodium® sono fornite in flaconi da 100.
NDC 50458-400-10
(100 CAPSULE)
Conservare a 15°-25°C (59°-77°F).
Revisionato settembre 1996, luglio 1998, aprile 2004
Approvato ottobre 2005
©Janssen Pharmaceutica Inc. 1998
Rx Only
Stampato in USA
U.S. Brevetto 3, 714,159
| Imodium loperamide cloridrato capsula |
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
Etichettatore – McNeil Consumer Healthcare
Domande frequenti
- Come fermare la diarrea – qualche suggerimento di medicine o rimedi?
Più informazioni su Imodium (loperamide)
- Effetti collaterali
- In gravidanza o allattamento
- Dosaggio Informazioni
- Immagini del farmaco
- Interazioni del farmaco
- Compara le alternative
- Gruppo di supporto
- 24 recensioni
- Classe del farmaco: antidiarroici
- FDA Alerts (2)
Risorse per i consumatori
- Lettura avanzata
Risorse professionali
- Informazioni sulla prescrizione
- Loperamide Oral Solution (FDA)
Altre marche Anti-Diarrheal, Up and Up Anti-Diarrheal Solution
Altre formulazioni
- Imodium A-D
Guide al trattamento correlate
- Diarrea, Acuta
- Diarrea, Cronica
- Diarrea del viaggiatore
- Diarrea
Disclaimer medico