Isositraattidehydrogenaasi katalysoi kemiallisia reaktioita:
Isositraatti + NAD+ ⇌ \displaystyle \rightleftharpoons }

2-oksoglutaraatti + CO2 + NADH + H+ Isositraatti + NADP+ ⇌ {\displaystyle \rightleftharpoons }

2-oksoglutaraatti + CO2 + NADPH + H+
Kokonaisvapaa energia tälle reaktiolle on -8,4 kJ/mol.
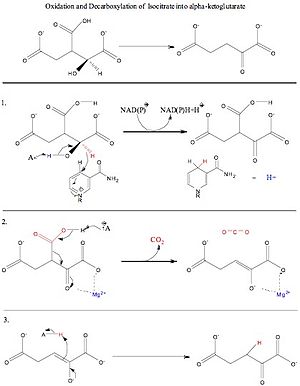
StepsEdit
Sitruunahappokierrossa sitraatin isomerisaatiosta syntyvä isositraatti käy läpi sekä hapetuksen että dekarboksylaation. Isositraattidehydrogenaasi-entsyymin (IDH) avulla isositraatti pysyy aktiivisessa paikassaan ympäröivien arginiini-, tyrosiini-, asparagiini-, seriini-, treoniini- ja asparagiinihappoaminohappojen avulla. Ensimmäisessä laatikossa esitetään isositraattidehydrogenaasin kokonaisreaktio. Tämän entsyymimekanismin toiminnan edellyttämät reaktantit ovat isositraatti, NAD+/NADP+ ja Mn2+ tai Mg2+. Reaktion tuotteet ovat alfa-ketoglutaraatti, hiilidioksidi ja NADH + H+/NADPH + H+. Vesimolekyylejä käytetään apuna isositraatin happigeenien (O3) deprotonoinnissa.
Kakkoslaatikko on vaihe 1, joka on alfa-C:n (C#2) hapettuminen. Hapettuminen on ensimmäinen vaihe, jonka isositraatti käy läpi. Tässä prosessissa alfa-hiilen (C#2) alkoholiryhmä deprotonoituu ja elektronit virtaavat alfa-C:hen muodostaen ketoniryhmän ja poistamalla hydridin C#2:sta käyttäen NAD+/NADP+:a elektronia hyväksyvänä kofaktorina. Alfa-C:n hapettuminen mahdollistaa aseman, jossa elektronit (seuraavassa vaiheessa) tulevat alas karboksyyliryhmästä ja työntävät elektroneja (jotka muodostavat kaksoissidoksisen hapen) takaisin hapen päälle tai nappaavat läheisen protonin läheiseltä lysiiniaminohapolta.
Kolmas laatikko on vaihe 2, joka on oksalosukkinaatin dekarboksylaatio. Tässä vaiheessa karboksyyliryhmän happi deprotonoituu läheisestä tyrosiiniaminohaposta ja nämä elektronit virtaavat alas hiileen 2. Hiilidioksidi poistuu isositraatin beetahiilestä poistuvana ryhmänä, ja elektronit virtaavat alfa-C:n ketonihappoon, jolloin alfa-C:n happi varautuu negatiivisesti ja muodostuu alfa-beta-tyydyttymätön kaksoissidos hiilien 2 ja 3 välille. Alfa-C-hapen yksinäinen pari ottaa protonin läheisestä lysiini-aminohaposta.
Neljäs ruutu on vaihe 3, joka on hiilien 2 ja 3 välisen alfa-beta-tyydyttymättömän kaksoissidoksen kyllästäminen. Tässä reaktiovaiheessa lysiini deprotonoi hapen pois alfahiilestä, ja alfahiilen hapen yksinäinen elektronipari laskeutuu reformoimalla ketonisen kaksoissidoksen ja työntämällä yksinäisen parin (joka muodostaa kaksoissidoksen alfa- ja beetahiilen välille) pois, jolloin se poimii protonin läheisestä tyrosiini-aminohaposta. Tämän reaktion tuloksena muodostuu alfa-ketoglutaraattia, NADH + H+/NADPH + H+ ja CO2.
Yksityiskohtainen mekanismiMuokkaa
Kaksi aspartaattiaminohappojäännöstä (vasemmalla alhaalla) ovat vuorovaikutuksessa kahden vierekkäisen vesimolekyylin (w6 ja w8) kanssa Mn2+ -isositraatti-possun IDH-kompleksissa, jotta alkoholi saadaan poistettua deprotonoitua alfa-hiiliatomista. Tässä kuvassa tapahtuu myös alfa-C:n hapettuminen, jossa NAD+ ottaa vastaan hydridin, jolloin syntyy oksalosukkinaattia. Alfa-C:n ympärillä tapahtuvan sp3:n ja sp2:n välisen stereokemiallisen muutoksen ohella alkoholiryhmästä muodostuu ketoniryhmä. Tämän ketoni-kaksoissidoksen muodostuminen mahdollistaa resonanssin syntymisen, kun poistuvasta karboksylaattiryhmästä tulevat elektronit siirtyvät kohti ketoniryhmää.
Oksalosukkinaatin dekarboksylaatio (alla keskellä) on keskeinen vaihe alfa-ketoglutaraatin muodostumisessa. Tässä reaktiossa viereisen tyrosiinihydroksyylin yksinäinen pari abstrahoi protonin karboksyyliryhmältä. Tätä karboksyyliryhmää kutsutaan myös isositraattimolekyylin beeta-alayksiköksi. Karboksyyliryhmän deprotonoituminen saa aikaan sen, että yksinäinen elektronipari siirtyy alaspäin muodostaen hiilidioksidia ja irtautuen oksalosukkinaatista. Elektronit liikkuvat edelleen kohti alfahiiltä ja työntävät kaksoissidoksen elektroneja (jotka muodostavat ketonin) ylöspäin abstrahoidakseen protonin viereisestä lysiinijäännöksestä. Hiilen 2 ja 3 välille syntyy alfa-beta-tyydyttymätön kaksoissidos. Kuten kuvasta näkyy, vihreä ioni edustaa joko Mg2+:a tai Mn2+:a, joka on kofaktori, joka on välttämätön, jotta tämä reaktio voisi tapahtua. Metalli-ioni muodostaa pienen kompleksin ionisten vuorovaikutusten kautta neljännen ja viidennen hiilen happiatomien kanssa (tunnetaan myös isositraatin gamma-alayksikkönä).
Hiilidioksidin irrottua oksalosukkinaatista dekarboksylaatiovaiheessa (oikealla alhaalla), enoli tautomerisoituu ketoksi alkaen. Ketonin kaksoissidoksen muodostuminen käynnistyy kyseisen hapen deprotonoinnilla alfa-hiilestä (C#2) saman lysiinin toimesta, joka protonoi hapen alun perin. Yksinäinen elektronipari siirtyy alaspäin ja irrottaa kaksoissidoksen muodostaneet yksinäiset elektroniparit. Tämä yksinäinen elektronipari irrottaa protonin tyrosiinista, joka poisti karboksyyliryhmän protonin dekarboksylaatiovaiheessa. Syy siihen, miksi voimme sanoa, että Lys- ja Tyr-jäämät ovat samat kuin edellisessä vaiheessa, on se, että ne auttavat pitämään isositraattimolekyylin entsyymin aktiivisessa paikassa. Nämä kaksi residuaalia pystyvät muodostamaan vetysidoksia edestakaisin, kunhan ne ovat tarpeeksi lähellä substraattia.
 Oksidoreduktaasivaihe, jossa NAD+:n avulla otetaan vastaan hydridi.
|
 Oksalosukkinaatin dekarboksylaatio.
|
 Tyydyttymättömän alfa-beta-kaksoissidoksen tyydyttäminen.
|
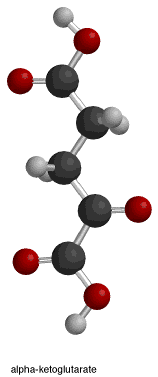
Edellä mainittu isositraattidehydrogenaasientsyymi tuottaa alfa-ketoglutaraattia, hiilidioksidia ja NADH + H+/NADPH + H+. Reaktiossa tapahtuu kolme muutosta. Hiilidioksidin 2 hapettuminen, hiilidioksidin 3 dekarboksylaatio (hiilidioksidin häviäminen) ja ketoniryhmän muodostuminen stereokemiallisella muutoksella sp3:sta sp2:ksi.
 |
 Sian mitokondrioiden NADP+-riippuvainen isositraattidehydrogenaasi kompleksoituu Mn2+:n ja isositraatin kanssa. Pintanäkymä aktiivisen alueen taskusta, jossa isositraatti on sidottu polaarisiin aminohappoihin.
|
 Sian mitokondriaalinen NADP+-riippuvainen isositraattidehydrogenaasi kompleksissa Mn2+:n ja isositraatin kanssa.
|
 Sian entsyymikompleksi; aktiivinen kohta isositraatti ja viereinen A.A.
|
Aktiivinen alueEdit
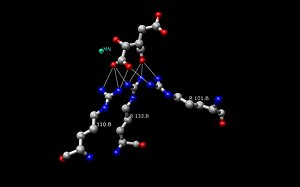
Escherichia colin isositraattidehydrogenaasi (IDH) -entsyymin rakenne oli ensimmäinen rakenne, joka selvitettiin ja ymmärrettiin. Sittemmin useimmat tutkijat ovat käyttäneet Escherichia coli -entsyymin IDH:n rakennetta tehdessään vertailuja muihin isositraattidehydrogenaasientsyymeihin. Tästä bakteerientsyymistä on paljon yksityiskohtaista tietoa, ja on todettu, että useimmat isositraattidehydrogenaasit ovat rakenteeltaan ja siten myös toiminnaltaan samanlaisia. Tämä rakenteen ja toiminnan samankaltaisuus antaa aihetta uskoa, että rakenteet ovat konservoituneet samoin kuin aminohapotkin. Näin ollen useimpien prokaryoottisten isositraattidehydrogenaasientsyymien aktiivisten paikkojen pitäisi myös olla konservoituneita, mikä on havaittu monissa prokaryoottisista entsyymeistä tehdyissä tutkimuksissa. Eukaryoottisia isositraattidehydrogenaasientsyymejä sen sijaan ei ole vielä täysin löydetty.IDH:n kullakin dimeerillä on kaksi aktiivista aluetta. Kumpikin aktiivinen alue sitoo NAD+/NADP+-molekyylin ja kaksiarvoisen metalli-ionin (Mg2+, Mn2+). Yleisesti ottaen kullakin aktiivisella kohdalla on konservoitu aminohapposekvenssi kutakin erityistä sitoutumiskohtaa varten. Desulfotalea psychrophilassa (DpIDH) ja sian (PcIDH) aktiiviseen kohtaan sitoutuu kolme substraattia.
- Isositraatti sitoutuu aktiivisen kohdan sisällä noin kahdeksan aminohapon konservoituneeseen sekvenssiin vetysidosten kautta. Näitä happoja ovat (voivat vaihdella jäämien suhteen, mutta niillä on samanlaiset ominaisuudet) tyrosiini, seriini, asparagiini, arginiini, arginiini, arginiini, tyrosiini ja lysiini. Niiden sijainti selkärangassa vaihtelee, mutta ne ovat kaikki lähellä toisiaan (esim. Arg131 DpIDH ja Arg133 PcIDH, Tyr138 DpIDH ja Tyr140 PcIDH).
- Metalli-ioni (Mg2+, Mn2+) sitoutuu kolmeen konservoituneeseen aminohappoon vetysidosten kautta. Näihin aminohappoihin kuuluu kolme aspartaattijäämää.
- NAD+ ja NADP+ sitoutuvat aktiivisen alueen sisällä neljällä alueella, joilla on samanlaisia ominaisuuksia IDH-entsyymien välillä. Nämä alueet vaihtelevat, mutta ovat noin , , , ja . Jälleen alueet vaihtelevat, mutta alueiden läheisyys on konservoitunut.