Ongelman määritelmä
Primäärinen hyperparatyreoosi on lisäkilpirauhashormonin (PTH) sääntelemätön ylituotanto, joka johtaa epänormaaliin kalsiumin homeostaasiin.
Erityisyys
Primäärinen hyperparatyreoosi on yleisempää naisilla, sillä ilmaantuvuus on naisilla 66/100 000 henkilötyövuotta ja miehillä 25/100 000 henkilötyövuotta. Suuressa tutkimuksessa, johon osallistui 3,5 miljoonaa eteläisen Kalifornian Kaiser Permanente -liikelaitoksen vakuutettua, esiintyvyys vaihteli ajan myötä, mutta sen ei havaittu vähentyneen merkittävästi. Päinvastoin, primaarisen hyperparatyreoosin esiintyvyys lisääntyi huomattavasti tässä väestössä. Diagnoosin keski-ikä on pysynyt 52-56 vuoden välillä.
Etiologia
Primäärisen hyperparatyreoosin aiheuttaa noin 85 prosentissa tapauksista yksittäinen adenooma. Tapauksista 15 %:ssa on mukana useita rauhasia (eli joko useita adenoomia tai hyperplasiaa). Harvoin primaarisen hyperparatyreoosin aiheuttaa lisäkilpirauhaskarsinooma. Adenoomien tai hyperplasian etiologia jää useimmissa tapauksissa tuntemattomaksi. Perinnölliset tapaukset voivat esiintyä joko osana multippelin endokriinisen neoplasian oireyhtymää (MEN 1 tai MEN 2a), hyperparatyreoosi-leukakasvainoireyhtymää (HPT-JT) tai familiaalista isoloitua hyperparatyreoosia (FIHPT). Myös familiaalinen hypokalsiurinen hyperkalsemia ja vastasyntyneen vaikea hyperparatyreoosi kuuluvat tähän ryhmään. MEN 1:n molekyyligeneettinen perusta on kromosomikaistalla 11q13 sijaitsevan MEN1-geenin inaktivoiva mutaatio. MEN 2a johtuu kromosomissa 10 sijaitsevan Ret-proto-onkogeenin sukusolumutaatiosta. HPT-JT:n aiheuttaa kromosomihaaraan 1q lokalisoituneen HRPT2:n sukusolumutaatio, kun taas FIHPT on geneettisesti heterogeeninen.
Patofysiologia
Adenoomista johtuvassa primaarisessa hyperparatyreoidismissa solunulkoisen kalsiumin aiheuttama normaali takaisinkytkentä lisäkilpirauhashormonituotannolle näyttäisi katoavan, mikä johtaa asetusarvon muuttumiseen. Näin ei kuitenkaan ole lisäkilpirauhasen liikakasvusta johtuvassa primaarisessa hyperparatyreoosissa. Syynä on todennäköisesti solujen määrän lisääntyminen.
Ylimääräisen lisäkilpirauhashormonin aiheuttama krooninen liiallinen kalsiumin resorptio luusta voi johtaa osteopeniaan. Vaikeissa tapauksissa tämä voi johtaa osteitis fibrosa cysticaan, jolle on ominaista distaalisten falangien subperiosteaalinen resorptio, distaalisten solisluiden kapeneminen, kallon suola-pippurimainen ulkonäkö ja pitkien luiden ruskeat kasvaimet. Tätä ei nykyään tavata yleisesti. Lisäksi kroonisesti lisääntynyt kalsiumin erittyminen virtsaan voi altistaa munuaiskivien muodostumiselle.
Yliparatyreoosin muut oireet johtuvat itse hyperkalsemiasta eivätkä ole hyperparatyreoosille ominaisia. Niitä voivat olla lihasheikkous, väsymys, tilavuuden väheneminen, pahoinvointi ja oksentelu sekä vaikeissa tapauksissa kooma ja kuolema. Neuropsykiatriset ilmenemismuodot ovat erityisen yleisiä, ja niihin voi kuulua masennusta, sekavuutta tai hienovaraisia puutteita, jotka ovat usein huonosti luonnehdittuja ja joita potilas ei välttämättä huomaa (tai joiden voidaan katsoa johtuvan ikääntymisestä). Lisääntynyt kalsium voi lisätä mahahapon eritystä, ja henkilöillä, joilla on lisäkilpirauhasen liikatoiminta, saattaa esiintyä useammin mahahaavatautia. Harvinaiset haimatulehdustapaukset on myös liitetty hyperkalsemiaan.
Ejlsmark-Svenssonin ym. prospektiivisessa kohorttitutkimuksessa raportoitiin, että primaarista hyperparatyreoosia sairastavilla potilailla elämänlaatukyselylomakkeen pistemäärät olivat merkitsevästi alhaisemmat keskivaikean ja vaikean hyperkalsemian yhteydessä kuin lievän hyperkalsemian yhteydessä. Elämänlaatu ei kuitenkaan näyttänyt olevan yhteydessä primaarisen hyperparatyreoosin elimiin liittyvien ilmenemismuotojen, kuten osteoporoosin, munuaisten kalkkeutumisen ja munuaistoiminnan heikkenemisen, esiintymiseen. Tämä viittaa siihen, että hyperkalsemia on ensisijainen elämänlaadun heikkenemisen aiheuttaja.
Kliininen esitys
Historia
Primäärisen hyperparatyreoosin kliininen oireyhtymä voidaan helposti muistaa ”luina, kivinä, vatsan huokauksina ja psyykkisinä valituksina”. Kun veren kalsiumin rutiinimittaus otettiin käyttöön 1970-luvun alussa, primaarisen hyperparatyreoosin yleisin kliininen esitys muuttui vaikeasta luusairaudesta tai munuaiskivistä oireettomaksi hyperkalsemiaksi.
Primäärisen hyperparatyreoosin luustoon liittyviin ilmenemismuotoihin kuuluu ensisijaisesti selektiivinen kortikaalinen luukato. Myös luu- ja nivelkipuja, pseudokouristusta ja kondrokalsinoosia on raportoitu. Primaarisen hyperparatyreoosin varhaisissa kliinisissä kuvauksissa joillekin potilaille kehittyi erityyppinen luusairaus, joka tunnettiin nimellä osteitis fibrosa cystica ja jolle oli ominaista lisääntynyt yleistynyt osteoklastinen luun resorptio. Osteitis fibrosa cysticaan liittyviin röntgenkuvausmuutoksiin kuuluvat subperiosteaalinen resorptio falangioissa ja suolapippurikalloksi kutsuttu löydös. Tätä esiintymismuotoa nähdään nykyään harvoin, paitsi lääketieteellisesti alihoidetuissa väestöryhmissä.
Munuaisten ilmentymiä ovat polyuria, munuaiskivet, hyperkalsiuria ja harvoin nefrokalsinoosi.
Ruoansulatuskanavan ilmentymiä ovat epämääräinen vatsakipu, anoreksia, pahoinvointi, oksentelu, ummetus, mahahaava ja akuutti haimatulehdus.
Neuromuskulaarisiin ja psykologisiin ilmenemismuotoihin kuuluvat väsymys, lihasheikkous, masennus, keskittymiskyvyttömyys ja muistihäiriöt tai hienovaraiset puutteet, joita usein luonnehditaan huonosti ja joita potilas ei välttämättä huomaa, yleinen kuvaus on ”aivosumu”. Nämä oireet johtuvat usein ikääntymisestä, ja joillakin potilailla diagnosoidaan krooninen väsymysoireyhtymä tai fibromyalgia.
Kardiovaskulaarisiin ilmenemismuotoihin kuuluvat verenpainetauti, bradykardia, lyhentynyt QT-väli ja vasemman kammion hypertrofia.
Fyysinen
Kuntotutkimuslöydökset ovat tavallisesti epäolennaisia. Tutkimuksessa voi ilmetä lihasheikkoutta ja masennusta. Palpoitavaa kaulan massaa ei yleensä odoteta hyperparatyreoosin yhteydessä, vaikka harvinaisissa tapauksissa se voi viitata lisäkilpirauhassyöpään. Palpoitavan kyhmyn lähteenä on paljon yleisemmin aiemmin diagnosoimaton kilpirauhaskyhmy.
Diagnostiset näkökohdat
Hyperkalsemian syitä, jotka johtavat samanaikaisesti kohonneeseen lisäkilpirauhashormonipitoisuuteen, on vähän. Näitä ovat familiaalinen hyvänlaatuinen (hypokalsiurinen) hyperkalsemia (FHH) (ks. Aiheeseen liittyvät häiriöt), litiumin aiheuttama hyperkalsemia ja tertiäärinen hyperparatyreoosi. Vähemmistöllä potilaista (eli 10-15 %:lla), joilla on hyperparatyreoosi, lisäkilpirauhashormonipitoisuudet ovat viitealueella, mutta ne ovat epäasianmukaisesti korkeat, kun seerumin kalsiumpitoisuudet ovat koholla. Osalla potilaista kalsiumpitoisuudet ovat normaalit ja parathormonipitoisuudet koholla, jolloin kyseessä on niin sanottu normokalkeeminen hyperparatyreoosi. Tätä diagnoosia harkittaessa on kuitenkin suljettava pois kaikki sekundaarisen hyperparatyreoosin mahdolliset syyt (esim. vähäinen kalsiumin saanti, ruoansulatuskanavan häiriöt, munuaisten vajaatoiminta, D-vitamiinin puute, munuaisperäinen hyperkalsiuria). Potilaita, joiden kalsiumpitoisuus on normaali ja lisäkilpirauhashormonipitoisuus koholla ilman tunnistettavaa sekundaarista syytä, on seurattava hyperkalsemian etenemisen varalta.
Sekundaarinen ja tertiaarinen hyperparatyreoosi diagnosoidaan tyypillisesti kliinisen kontekstin perusteella. Syövän aiheuttamaan hyperkalsemiaan liittyy matala lisäkilpirauhashormonitaso mutta mahdollisesti korkea lisäkilpirauhashormoniin liittyvä peptiditaso.
Työstö
Laboratoriotutkimukset
Seerumin kokonaiskalsium- ja albumiinitasot tai ionisoidun kalsiumin pitoisuudet on mitattava. Hyperkalsemia on dokumentoitava useampaan kuin yhteen otteeseen ennen diagnostisen työn aloittamista.
Parathormonipitoisuuden testaaminen ehjänä on diagnoosin ydin. Kohonnut ehjä lisäkilpirauhashormonitaso, johon liittyy kohonnut seerumin ionisoidun kalsiumin taso, on primaarisen hyperparatyreoosin diagnoosi. Virtsan 24 tunnin kalsiummittaus on välttämätön FHH:n poissulkemiseksi.
Aiemmat määritykset mittasivat lisäkilpirauhashormonimolekyylin fragmentteja, kuten lisäkilpirauhashormonin C-terminaalista tai keskiosasta. Näitä ensimmäisen sukupolven määrityksiä pidetään kliinisen käytännön kannalta vanhentuneina. Toisen sukupolven lisäkilpirauhashormonimäärityksissä, joita kutsutaan yleisesti ”ehjiksi” lisäkilpirauhashormonimäärityksiksi, ja kolmannen sukupolven lisäkilpirauhashormonimäärityksissä, joita kutsutaan ”kokonaisiksi” tai ”biologisesti koskemattomiksi” lisäkilpirauhashormonimäärityksiksi, käytetään kahta erilaista vasta-ainetta lisäkilpirauhashormonin kahta erilaista segmenttiä vastaan. Toisen ja kolmannen sukupolven lisäkilpirauhashormonimääritykset tuottavat paljon kliinisesti tyydyttävämpää tietoa kuin ensimmäisen sukupolven määritykset, mutta niillä on joitakin rajoituksia, joita arvioidaan edelleen useissa tutkimuksissa.
Muut laboratoriolöydökset primaarisessa hyperparatyreoidismissa ovat lievä hyperkloorimeettinen asidoosi, hypofosfatemia ja lievä tai kohtalainen kalsiumin erittymisnopeuden nousu virtsaan.
D-vitamiinipitoisuudet tulisi mitata primaarisen hyperparatyreoidismia arvioidessa. D-vitamiinin puute (25-hydroksivitamiini-D-taso alle 20 ng millilitrassa) voi aiheuttaa sekundaarista hyperparatyreoosia, ja D-vitamiinin puutteen täydentäminen voi auttaa alentamaan lisäkilpirauhashormonitasoja. Useimmissa tutkimuksissa seerumin 25-hydroksivitamiini D -varastojen kasvattaminen vähintään 37,5 ng:aan millilitrassa riittää lisäkilpirauhashormonin suppressioon ja sekundaarisen hyperparatyreoosin ehkäisyyn henkilöillä, joilla on normaali munuaistoiminta (vaikka joissakin tutkimuksissa on ehdotettu varastojen kasvattamista 50 ng:aan millilitrassa).
Kuvantamistutkimukset
Kuvantamistutkimuksia ei käytetä primaarisen hyperparatyreoosin diagnoosin tekemiseen (joka perustuu laboratoriotietoihin) tai kirurgisen hoidon aloittamista koskevan päätöksen tekemiseen (joka perustuu kliinisiin kriteereihin). Kuvantamistutkimuksia käytetään kirurgin ohjaamiseen, kun kirurgisesta hoidosta on päätetty. Jos halutaan tehdä rajoitettu lisäkilpirauhasen tähystys, tarvitaan paikallistava tutkimus. Kuvantamistutkimusten muu käyttö primaarista hyperparatyreoosia sairastavan potilaan alkuvaiheen arvioinnissa on kiistanalaista (ks. kohta Kirurgisen hoidon valinta, jäljempänä).
Monille potilaille suositellaan edelleen täydellistä lisäkilpirauhasen tähystystä, johon kuuluu kaikkien mukana olevien rauhasten resektio. Monet kirurgit ovat yhtä mieltä siitä, että kuvantamistutkimuksia ei tarvita, kun valitaan tämä kirurginen hoito. Kuitenkin potilailla, joilla on uusiutuva tai jatkuva hyperparatyreoosi edellisen kirurgisen tähystyksen jälkeen, kuvantamistutkimus mukana olevien rauhasten lokalisoimiseksi on ehdottomasti aiheellinen.
Kaulan ultraäänitutkimus on turvallinen ja laajalti käytetty tekniikka epänormaalien lisäkilpirauhasten lokalisoimiseksi. Sillä voidaan saavuttaa suuri tarkkuus, mutta se on operaattorista riippuvainen, ja sen raportoitu tarkkuus on vaihdellut suuresti kirjallisuudessa. Yksi kaulan ultraäänitutkimuksen eduista on se, että kliinikko voi suorittaa sen nopeasti ensiarvion yhteydessä. Kliinikon suorittamaa ultraäänitutkimusta koskevat tutkimukset osoittavat tarkkuusprosentteja, jotka ovat 75-80 prosentin luokkaa ja verrattavissa perinteisten radiologian osastojen tarkkuuteen. Ultraäänitutkimus, samoin kuin ydinlääketieteellinen tähystys, ei ole ollut luotettava monirakkulataudin havaitsemisessa.
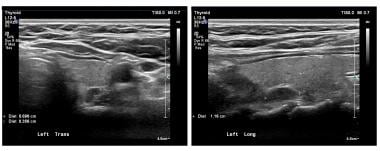 Paneeleissa on esitetty poikittais- ja pitkittäisnäkymä (sagittaalinen) vasemmanpuoleisesta ylemmästä lisäkilpirauhasen adenoomasta ultraäänitutkimuksessa. Mittatikun merkit kuvaavat adenoomaa. Adenoomat ovat tyypillisesti homogeenisia ja hypoekaikuisia.
Paneeleissa on esitetty poikittais- ja pitkittäisnäkymä (sagittaalinen) vasemmanpuoleisesta ylemmästä lisäkilpirauhasen adenoomasta ultraäänitutkimuksessa. Mittatikun merkit kuvaavat adenoomaa. Adenoomat ovat tyypillisesti homogeenisia ja hypoekaikuisia. Nukleaarikuvaus radiomerkityllä sestamibilla on myös laajalti käytetty tekniikka. Sestamibia käytetään yleisesti sydämen kuvantamisessa, ja sen havaittiin sattumalta kertyvän lisäkilpirauhasen adenoomiin. Tämä radionuklidi keskittyy kilpirauhas- ja lisäkilpirauhaskudokseen, mutta huuhtoutuu tavallisesti pois normaalista kilpirauhaskudoksesta alle tunnissa. Se säilyy epänormaalissa lisäkilpirauhaskudoksessa. Katso alla oleva kuva.
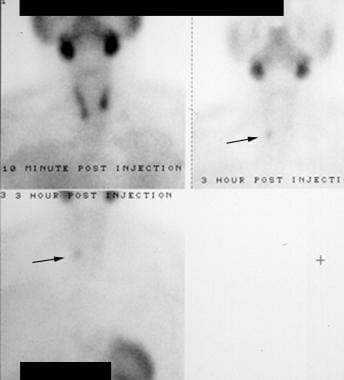 Hyperparatyreoosi. Teknetium-99m (99mTc) sestamibi radionukliditutkimus. Varhaisessa kuvassa (ylhäällä vasemmalla) näkyy hyväksikäyttö sylkirauhasissa ja kilpirauhasessa. Myöhemmissä kuvissa (oikealla ja alhaalla) näkyy kilpirauhasen huuhtoutuminen mutta pysyvyys oikean alemman kilpirauhaslohkon alueella (nuolet). Tämä osoittautui oikean lisäkilpirauhasen adenoomaksi.
Hyperparatyreoosi. Teknetium-99m (99mTc) sestamibi radionukliditutkimus. Varhaisessa kuvassa (ylhäällä vasemmalla) näkyy hyväksikäyttö sylkirauhasissa ja kilpirauhasessa. Myöhemmissä kuvissa (oikealla ja alhaalla) näkyy kilpirauhasen huuhtoutuminen mutta pysyvyys oikean alemman kilpirauhaslohkon alueella (nuolet). Tämä osoittautui oikean lisäkilpirauhasen adenoomaksi. Viivästyneissä kuvissa epänormaali lisäkilpirauhanen näkyy pysyvänä aktiivisuuskeskittymänä. Skannauksen herkkyys yksinäisten adenoomien havaitsemisessa on kirjallisuudessa vaihdellut suuresti, mutta yleensä sen ilmoitetaan olevan 60-90 %. Testin suurin heikkous on monirakkulaisen sairauden diagnosointi. Tällöin herkkyys laskee noin 50 prosenttiin. Useimmat nykyaikaiset sestamibi-tutkimukset tehdään yhden fotonin tietokonetomografialla (SPECT). Tässä tekniikassa (ks. kuva alla) yhdistetään radioaktiivisuuden havaitseminen ja tietokonetomografiakuvauksen yksityiskohtainen kuvantaminen, mikä mahdollistaa paremman herkkyyden ja tarkemman anatomisen paikannuksen kuin tavallinen tasokuvaus (kuten edellä on esitetty).
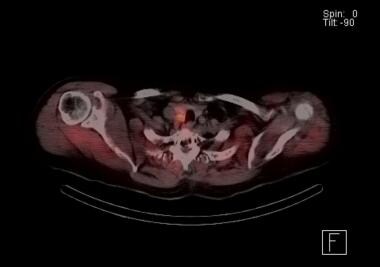 Sestamibi-tutkimus lisäkilpirauhasista SPECT-kuvauksella. Oranssi osoittaa radionuklidin kertymistä. Löydökset viittaavat oikeanpuoleiseen lisäkilpirauhasen adenoomaan heti kilpirauhaslohkon takana. Tutkimuksessa todettiin, että tällä potilaalla oli oikealla puolella vierekkäisiä kaksoisadenoomia.
Sestamibi-tutkimus lisäkilpirauhasista SPECT-kuvauksella. Oranssi osoittaa radionuklidin kertymistä. Löydökset viittaavat oikeanpuoleiseen lisäkilpirauhasen adenoomaan heti kilpirauhaslohkon takana. Tutkimuksessa todettiin, että tällä potilaalla oli oikealla puolella vierekkäisiä kaksoisadenoomia. Yksi sestamibi-lisäkilpirauhaskuvauksen suurista eduista on kyky havaita ektooppiset lisäkilpirauhaset, erityisesti välikarsinassa.
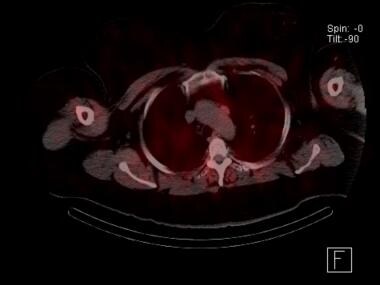 Sestamibi-tutkimus lisäkilpirauhasista SPECT-kuvauksella, jossa näkyy ektooppinen mediastinaalinen lisäkilpirauhasen adenooma aortan kaaren vieressä. Tälle potilaalle oli tehty epäonnistunut kaulan tähystys. Tranthorakaalinen robottileikkaus oli parantava.
Sestamibi-tutkimus lisäkilpirauhasista SPECT-kuvauksella, jossa näkyy ektooppinen mediastinaalinen lisäkilpirauhasen adenooma aortan kaaren vieressä. Tälle potilaalle oli tehty epäonnistunut kaulan tähystys. Tranthorakaalinen robottileikkaus oli parantava. Neliulotteisen (4D) tietokonetomografian käyttö lisäkilpirauhasen paikantamisessa on lisääntymässä. Tutkimus voidaan tehdä joko ilman kontrastia tai dynaamisen kontrastikuvauksen avulla. Lisäkilpirauhasen adenoomat korostuvat kirkkaasti kontrastilla niiden suuren verisuonituksen vuoksi, minkä jälkeen kontrasti huuhtoutuu nopeasti pois. Neliulotteisten tietokonetomografiatutkimusten herkkyysprosentti on ollut jopa 88 %. Suurimmassa tätä kirjoitettaessa saatavilla olleessa retrospektiivisessä tutkimuksessa kokonaisherkkyydeksi ilmoitettiin 79 %. Muiden kuvantamistutkimusten tavoin 4D-CT-kuvaus ei ole yhtä herkkä havaitsemaan monirauhastautia (43-67 % ) kuin yhden rauhasen tautia (92-94 % ). Joissakin tutkimuksissa on väitetty, että kaksivaiheinen tietokonetomografiakuvaus on yhtä tehokas kuin 4D-tutkimusmenetelmä lisäkilpirauhasten paikantamisessa, myös pienten adenoomien, uusintaleikkausten ja multiglandulaarisen taudin tapauksessa, ja potilaan säteilyaltistus on pienempi. ) Vaikka kaksivaiheinen tekniikka alentaa säteilyaltistusta, tämä tapahtuu todennäköisesti optimaalisen tarkkuuden kustannuksella.
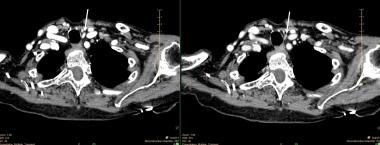 Pieni, vasemmanpuoleinen inferiorinen lisäkilpirauhasen adenooma 4D-CT-kuvauksessa. Vasemmassa paneelissa on yksittäinen kuva varhaisesta kontrastivaiheesta, jossa näkyy voimakas tehostuminen. Oikeassa paneelissa näkyy kontrastin nopea huuhtoutuminen. Valkoiset nuolet osoittavat adenoomaan.
Pieni, vasemmanpuoleinen inferiorinen lisäkilpirauhasen adenooma 4D-CT-kuvauksessa. Vasemmassa paneelissa on yksittäinen kuva varhaisesta kontrastivaiheesta, jossa näkyy voimakas tehostuminen. Oikeassa paneelissa näkyy kontrastin nopea huuhtoutuminen. Valkoiset nuolet osoittavat adenoomaan. Magneettiresonanssikuvausta (MRI) ei ole yleisesti käytetty lisäkilpirauhasen lokalisointiin useimmissa keskuksissa, ja tätä menetelmää koskevat tutkimukset ovat yleensä olleet pieniä ja niissä on kaikissa käytetty kontrastia. Uusia tekniikoita, jotka käsitteellisesti muistuttavat 4D-CT-skannausta, ollaan kehittämässä, mikä voi lisätä magneettikuvauksen herkkyyttä ja laajentaa sen käyttökelpoisuutta.
Dual energy radiographic absorptiometry on hyödyllinen väline primaarisen hyperparatyreoosin luuston osallistumisen osoittamiseen. Huomaa, että hyperparatyreoosi vaikuttaa ensisijaisesti radiuksen kortikaaliseen luuhun (distaalinen kolmannes). Vaikeassa primaarisessa hyperparatyreoosissa luuston röntgenkuvissa nähdään patognomonisia muutoksia, kuten suoliluun ja pippurin hajoamista kallossa ja subperiosteaalista luun resorptiota falangissa. Tavalliset röntgenkuvat eivät kuitenkaan yleensä ole käyttökelpoisia rutiinikäytössä hyperparatyreoosin diagnostiikassa ja hoidossa.
Thimmappan ym. tutkimuksessa ehdotettiin, että kuvantamistutkimuksia voidaan käyttää intraoperatiivisten lisäkilpirauhasnäytteiden (joita käsitellään jäljempänä) sijasta ennustamaan paranemista primaarisen hyperparatyreoosin leikkauksessa. Tutkijat kuvasivat seuraavan protokollan :
-
Suoritetaan kaksi preoperatiivista paikannustutkimusta, joista toisessa kirurgin suorittama ultraäänitutkimus
-
Arvioidaan preoperatiiviset D-vitamiinitasot, ja täydennetään tarvittaessa
Kertomuksessa väitettiin, että valikoiduilla potilailla, joilla kahden lokalisointitutkimuksen ja näiden tutkimusten kanssa yhdenmukaisten intraoperatiivisten löydösten välillä on vahva vahvistus, intraoperatiivisia lisäkilpirauhasen määrityksiä ei ehkä tarvita, ja tutkimuksessa todettiin, että niiden potilaiden paranemisprosentit, joilla tätä protokollaa käytettiin, olivat yhtä korkeat kuin lisäkilpirauhasen määrityksiä käyttäen saavutetut.
Menetelmät
Bilateraalista kaulalaskimon sisäistä näytteenottoa käytetään auttamaan ektooppisten lisäkilpirauhasen adenoomien paikallistamisessa yleensä tapauksissa, joissa kirurginen tutkimus ei ole onnistunut, kun tavanomaisista kuvantamistekniikoista ei ole ollut apua. Tämä tekniikka olisi yleensä varattava keskuksiin, joissa on erikoislääkäreitä, ja hyvin valikoiduille potilaille.
Hoito
Peräisten lisäkilpirauhasten kirurginen poisto (ks. jäljempänä kirurgista hoitoa koskevat yksityiskohdat) tarjoaa primaarisen hyperparatyreoosin ainoan pysyvän, parantavan hoidon. Yleisesti ollaan yhtä mieltä siitä, että kirurgista hoitoa olisi tarjottava kaikille potilaille, joilla on oireinen tauti. Kirjoittajat huomauttavat kuitenkin, että sekä lääkärit että potilaat jättävät usein oireet huomiotta; väsymys on erittäin yleinen oire, joka jätetään usein huomiotta erityisesti iäkkäillä henkilöillä, jotka pitävät sitä yleensä ikääntymisen tai muiden syiden aiheuttamana. Oireettomien potilaiden optimaalisesta hoidosta on jonkin verran kiistaa.
Oireettoman primaarisen hyperparatyreoosin hoitoa koskevat ohjeet päivitettiin vuonna 2013 oireetonta primaarista hyperparatyreoosia käsittelevässä neljännessä kansainvälisessä työpajassa. Leikkausindikaatioita ovat seuraavat :
-
Serumkalsium >1 mg/dl yli viitealueen ylärajan
-
Luun mineraalitiheyden T-pistemäärä -2 tai alle.5 (perimenopausaalisilla tai postmenopausaalisilla naisilla ja 50-vuotiailla tai sitä vanhemmilla miehillä) lannerangassa, lonkassa, reisiluun kaulassa, tai sädekehän distaalisessa 1/3:ssa
-
Röntgenkuvauksella tai nikamamurtuman arvioinnilla (VFA)
-
Kreatiniinipuhdistuma < 60 cc/min
-
Nefrolitiaasin tai nefrokalsinoosin esiintyminen määritettynä radiografialla, ultraäänitutkimuksella, tai tietokonetomografia
-
Aikä alle 50 vuotta
Kahdeksankymmentäneljän tunnin kalsiumin erittyminen virtsaan >400 mg/vrk ja suurentunut kiviriski biokemiallisella kiviriskianalyysillä arvioituna.
Jotkut kliinikot kannattavat kirurgista hoitoa kaikille primaarista hyperparatyreoosia sairastaville potilaille, ja sitä muokataan vain niille potilaille, jotka eivät siedä leikkausta. He väittävät, että leikkaus on yleensä hyvin siedetty, että tällainen hoito ehkäisee komplikaatioita (esim. osteoporoosia) ja että se voi kumota oireita, joita potilaat eivät useinkaan tajua (esim. väsymys, lievä masennus). Lisäksi oireettomien potilaiden seuranta on kallista ja hankalaa. American Association of Clinical Endocrinologistsin ja American Association of Endocrine Surgeonsin koolle kutsuma asiantuntijaryhmä on ilmaissut tämän vapaamielisemmän lähestymistavan. He totesivat, että ”…operatiivista hoitoa olisi harkittava ja suositeltava kaikille oireettomille PHPT-potilaille, joilla on kohtuullinen elinajanodote ja sopivat operatiiviset ja anestesiariskitekijät”. Tämän ennakoivan lähestymistavan, kuten kaikkien paratyroidektomioiden, tulisi riippua kokeneen, hyvin koulutetun kirurgin saatavuudesta.
Sharatan ym. tekemässä kyselytutkimuksessa, joka koski perusterveydenhuollon tarjoajia Yhdysvalloissa, todettiin, että vain vähemmistö vastaajista oli vakaasti perehtynyt primaarisen hyperparatyreoosin hoitostrategioihin. Tutkijat havaitsivat, että 31 % kyselyyn vastanneista 109 kliinisestä lääkäristä tunsi koko valikoiman kriteerejä, jotka koskevat kirurgista toimenpidettä oireettomilla potilailla, ja että 34 % pystyi tunnistamaan tarkasti oikeat seurantatestit tarkkailtaville potilaille. Tarkkailussa olevista potilaista vain 16 prosentille tehtiin asianmukaiset seurantatutkimukset.
Seuran vaikean hyperkalsemian hoito akuutissa tilanteessa
Seerumin kohonneen kalsiumin vähentäminen voidaan toteuttaa käyttämällä verisuonensisäistä tilavuuden laajentamista natriumkloridilla ja loop-diureetteja, kuten furosemidiä, kun verisuonensisäinen tilavuus on saatu palautettua. Lääkkeitä, kuten kalsitoniinia ja iv-bisfosfonaattia, on käytetty tilapäisenä toimenpiteenä ennen kirurgista hoitoa.
Ei-kirurginen hoito ja pitkäaikaisseuranta
Osymptomaattiset potilaat, joille ei tehdä leikkausta, tarvitsevat pitkäaikaisseurantaa. Suosituksiin kuuluu hyperparatyreoosin avointen merkkien ja oireiden arviointi vuosittain, seerumin kalsiumin ja kreatiniinin vuosittainen testaus sekä luun mineraalitiheyden (selkäranka, lonkka ja kyynärvarsi) arviointi 1-2 vuoden välein.
Potilaiden, joilla on primaarinen hyperparatyreoosi, tulisi ylläpitää kohtuullista 800-1000 mg:n päivittäistä alkuaineen kalsiumin saantia ja ikään ja sukupuoleen sopivaa D-vitamiinin saantia. Hyvän nesteytyksen ylläpitäminen, säännölliseen liikunta-aktiivisuuteen osallistuminen sekä immobilisaation ja tiettyjen lääkkeiden (kuten tiatsidien, diureettien ja litiumin) välttäminen ovat suotavia.
Farmakoterapia
Estrogeenihoidon postmenopausaalisilla naisilla on osoitettu aiheuttavan pientä seerumin kalsiumin vähenemistä (0,5-1 mg/dl) ilman, että lisäkilpirauhashormoni muuttuu. Estrogeenilla on myös suotuisia vaikutuksia lannerangan ja reisiluun kaulan luun mineraalitiheyteen (BMD). Estrogeenikorvaukseen liittyvien riskien vuoksi sitä ei kuitenkaan pitäisi käyttää pelkästään primaarisen hyperparatyreoosin hoitoon.
Selektiivisten estrogeenireseptorimodulaattoreiden, kuten raloksifeenin, on osoitettu aiheuttavan seerumin kalsiumin vähenemistä samassa suuruusluokassa kuin estrogeenin käytön yhteydessä on havaittu.
Bisfosfonaattien, erityisesti alendronaatin, on osoitettu parantavan selkärangan ja lonkkien BMD:tä potilailla, joilla on primaarinen hyperparatyreoosi. Merkittävää muutosta lisäkilpirauhashormonissa, kalsiumissa tai 24 tunnin virtsakalsiumissa ei ole raportoitu. Hoitoa bisfosfonaatilla, kuten alendronaatilla, voidaan harkita primaarista hyperparatyreoosia ja matalaa BMD:tä sairastavilla potilailla, joille ei voida tai haluta tehdä leikkausta.
Kalsiumlääkkeet aktivoivat kalsiumia aistivan reseptorin ja estävät lisäkilpirauhassolujen toimintaa. Hoito kinakalsetilla johti lisäkilpirauhashormonipitoisuuksien pienenemiseen ilman, että ne normalisoituivat, seerumin kalsiumin pienenemiseen ja jopa normalisoitumiseen, mutta BMD:n lisääntymistä ei havaittu.
Muut hoidot
Perkutaanista alkoholin injektiota, ultraäänienergialla tehtävää ablaatiota ja muita lisäkilpirauhasen perkutaanisia ablaatiotekniikoita on ehdotettu vaihtoehtoisiksi hoitomuodoiksi potilailla, joilla on primaarinen liikatoiminta (primaarinen liikatoiminta), mutta jotka eivät voi tai jotka eivät suostu menemään leikkaukseen. Vaikka näitä tekniikoita koskevat tutkimukset jatkuvat, niiden rutiinikäyttöä ei voida vielä tukea.
Kirurginen hoito
Kirurgista hoitoa olisi tarjottava useimmille primaarista hyperparatyreoosia sairastaville potilaille. Historiallinen kriteeri-standardi operatiivinen lähestymistapa on täydellinen kaulan tähystys, jossa tunnistetaan kaikki lisäkilpirauhaset ja poistetaan kaikki epänormaalit rauhaset. Noin 85 prosenttia primaarisen hyperparatyreoosin tapauksista johtuu yksittäisestä adenoomasta. Siksi useimmat potilaat, joille tehdään täydellinen kaulan tähystys kaikkien lisäkilpirauhasten arvioimiseksi, joutuvat kärsimään jonkin verran tarpeettomasta leikkelystä. Kaikkien lisäkilpirauhasten tutkimisen sijaan on kehitetty uudempi tekniikka, suunnattu paratyroidektomia. Tämä tekniikka perustuu leikkausta edeltäviin kuvantamistutkimuksiin epänormaalin rauhasen paikallistamiseksi. Tämän jälkeen kirurgi poistaa vain kyseisen rauhasen ilman muiden rauhasten visualisointia.
Nykyaikaisilla kuvantamistekniikoilla epänormaali lisäkilpirauhanen voidaan havaita preoperatiivisesti 70-80 prosentissa tapauksista. Mikään nykyinen kuvantamistutkimus ei kuitenkaan ole luotettava useiden epänormaalien rauhasten havaitsemiseksi. Sen vuoksi tarvitaan lisämenetelmä, jolla voidaan varmistaa, ettei muita epänormaaleja rauhasia ole kuvannetun leesion poiston jälkeen. Tähän tarkoitukseen useimmat keskukset käyttävät intraoperatiivista lisäkilpirauhashormonimääritystä. Koska lisäkilpirauhashormonin puoliintumisaika plasmassa on vain noin 4 minuuttia, taso laskee nopeasti lähteen resektion jälkeen. Jos taso ei laske tunnistetun epänormaalin rauhasen resektion jälkeen, toimenpidettä jatketaan lisätutkimusten mahdollistamiseksi. Intraoperatiivinen lisäkilpirauhashormonimääritys on kuitenkin yleensä käytettävissä vain sellaisissa keskuksissa, joissa tehdään paljon paratyroidektomioita.
Muutamat kirjoittajat ovat kannattaneet radio-ohjattua paratyroidektomiaa, jossa leimattu sestamibi havaitaan epänormaalissa rauhasessa käsikäyttöisellä anturilla. Useimmat keskukset ovat luopuneet tästä tekniikasta, koska jos rauhanen leimautuu hyvin sestamibilla, mikä mahdollistaa riittävän preoperatiivisen kuvantamisen, käsisondin käyttö intraoperatiivisesti on useimmissa tapauksissa tarpeetonta.
Greene ym. tutkivat suuntauksia, joita on havaittavissa, kun kirurgit käyttävät kahdenvälistä vs. rajoitettua eksploraatioleikkausta paratyroidektomiassa vuosien 1998 ja 2008 välillä. Tutkijat tekivät kyselytutkimuksen 256 kirurgille (American Association of Endocrine Surgeonsin ja American College of Surgeonsin jäsenille), jotka yhdessä tekivät 46 % lisäkilpirauhasleikkauksista Yhdysvalloissa, ja havaitsivat, että vuonna 2008 10 % kirurgeista käytti kaulan bilateraalista eksploraatiota, 68 % käytti rajoitettua eksploraatiota ja 22 % käytti molempia eksploraatiotekniikoita omassa käytännössäan. Vuonna 1998 kahdenvälistä, rajoitettua tai molempia eksploraatiotekniikoita käyttävien kirurgien osuus oli 74 %, 11 % ja 15 %. Tutkimus osoitti, että lääkärit, jotka todennäköisimmin käyttävät rajoitettua eksploraatiota, ovat endokriinikirurgeja, kirurgeja, joilla on suuren volyymin praktiikka, ja kirurgeja, joiden mentorit käyttivät rajoitettua eksploraatiota.
Tekijät havaitsivat myös, että vuonna 2008 puolet tutkimukseen osallistuneista yleiskirurgien lääkäreistä ei koskaan tarkkaillut lisäkilpirauhashormoneja leikkauksen aikana (riippumatta siitä, käyttivätkö he bilateraalista vai rajoitettua eksploraatiota), kun taas endokriinisistä kirurgeista alle 10 %:lla oli vastaava tilanne. Lisäksi ”kirurgien alaryhmien välillä oli suurta vaihtelua operatiivisissa volyymeissä, kahdenvälisen kaulan tähystyksen indikaatioissa, hoidossa, asiantuntemuksessa sestamibin kanssa ja sestamibin kanssa sekä käsityksissä paranemis- ja komplikaatiomääristä”. Greene ja hänen kirjoittajakumppaninsa päättelivät, että hyperparatyreoosin kirurgisessa hoidossa esiintyvien monien erojen vuoksi saattaa olla tarpeen määritellä parhaita käytäntöjä koskevat ohjeet.
Sukuisissa sairauksissa, kuten MEN 1:ssä, suoritetaan totaalinen paratyreoidektomia yhdessä kaulan tyremektomian ja kyynärvarren autotransplantaation kanssa. Joidenkin lisäkilpirauhaskudosten kryosäilytystä suositellaan myös.
Paratyroidektomia on yleensä hyvin siedetty. Suurimmat riskit ovat kurkunpään takautuvien hermojen vammautuminen ja hypoparatyreoosi, joka johtuu kaikkien lisäkilpirauhasten resektiosta tai devaskularisaatiosta. Vaikka paikallispuudutusta on käytetty menestyksekkäästi tässä toimenpiteessä, erityisesti suunnatuissa lähestymistavoissa, joissa yksittäinen adenooma paikallistetaan preoperatiivisesti, yleisimmin käytetään yleisanestesiaa. Potilailla, joilla hyperkalsemia (ja siten myös nestehukka) on ollut vakava, on kiinnitettävä erityistä huomiota nestetasapainon palauttamiseen perioperatiivisesti. Kaulan liikkuvuus on arvioitava, jotta voidaan varmistaa oikea asento leikkaussalissa.
Tekniikka kaulan täydelliseen tähystykseen, jossa tunnistetaan kaikki lisäkilpirauhaset
Kriittisin näkökohta tämän leikkauksen onnistumisen varmistamiseksi on kaikkien neljän lisäkilpirauhasen tunnistaminen ja kaikkien epänormaalien rauhasten poistaminen. Jos kyseessä on 4 rauhasen liikakasvu, tehdään 3,5 rauhasen (subtotaalinen) paratyroidektomia. Jäljelle jää noin 50-70 mg normaalimmalta näyttävää kudosta. Imeytymätön ommel jätetään merkiksi, jonka avulla rauhanen voidaan tunnistaa, jos uusintaleikkaus on tarpeen.
Potilas asetetaan nurmikkotuoliasentoon niin, että kaula on ojennettuna poikittain asetetun hartiarullan päällä. Tämä asento mahdollistaa kaulan etuosan rakenteiden täydellisen paljastumisen ja parantaa laskimotiehyttä.
Matalalla poikittaisella viillolla, joka on sijoitettu ihopoimun sisään, saadaan paras kosmeettinen tulos. Viillon pituuden on oltava riittävä, jotta kaikki lisäkilpirauhasten mahdolliset sijainnit voidaan tutkia perusteellisesti; ottaen kuitenkin huomioon kaulan iholäpän joustavuus, 2-5 cm:n viilto mahdollistaa yleensä tärkeiden rakenteiden turvallisen tunnistamisen.
Kun ihoviillon hemostaasi on saatu aikaan, subplatysmaaliset läpät kehitetään ylempänä kilpirauhasruston loveen ja alempana manubriumin litteään osaan. Sternohyoideus- ja sternothyroid-lihakset erotetaan keskiviivalla kilpirauhasen paljastamiseksi. Jos preoperatiiviset lokalisointitutkimukset viittaavat lisäkilpirauhasen adenoomaan, kyseistä puolta lähestytään ensin.
Usein keskimmäinen kilpirauhasen laskimo voi vaatia ligointia kilpirauhaslohkon riittävän mobilisoinnin varmistamiseksi. Kilpirauhaslohko nostetaan pois yhteisestä kaulavaltimosta ja vedetään takaisin mediaalisesti. Alempi kilpirauhasvaltimo tunnistetaan sen jälkeen, kun areolaarinen kudos on leikattu tylpällä ja terävällä leikkauksella anteriorisesti ja mediaalisesti yhteiseen kaulavaltimoon nähden ja posteromediaalisesti kilpirauhaslohkoon nähden. Kurkunpäähermo tunnistetaan seuraavaksi kilpirauhasen alalohkon alapuolelta ja lateraalisesti.
Kilpirauhasen alaosan valtimon ja kurkunpäähermon risteyskohta on tärkeä kiintopiste, koska useimmat lisäkilpirauhaset, ylemmät ja alemmat, sijaitsevat kahden senttimetrin etäisyydellä tästä alueesta. Ylemmät lisäkilpirauhaset sijaitsevat kilpirauhaslohkon kahden ylemmän kolmanneksen dorsaalipuolella ja takapuolella kurkunpään kiertäjähermosta. Alemmat rauhaset, joiden sijainti on epäyhtenäisempi, sijaitsevat yleensä alempana kilpirauhasen alemman valtimon alapuolella ja vatsanpuoleisesti kurkunpäähermon alapuolella. Ne sijaitsevat yleensä 1 cm:n etäisyydellä kilpirauhasen alapuolisesta lohkosta.
Joskus kaikkia lisäkilpirauhasia ei voida tunnistaa. Tällaisissa tapauksissa tavanomaiset sijainnit tutkitaan ensin uudelleen, koska useimmat lisäkilpirauhaset sijaitsevat tyypillisillä alueilla. Jos lisäkilpirauhasia ei tunnisteta näissä paikoissa, suoritetaan systemaattinen etsintä ottaen huomioon ylempien ja alempien lisäkilpirauhasten laskeutumisreitti.
Ylempien lisäkilpirauhasten laskeutumisreitti voi sijaita kilpirauhasen ligamentissa. Niitä voi olla vaikea tunnistaa, erityisesti alemman kilpirauhaslaskimon jakamisen jälkeen, mikä on manööveri, joka mahdollistaa rauhasen vetäytymisen ylempään välikarsinaan. Toinen ektooppisten alempien lisäkilpirauhasten sijaintipaikka on kateenkorva. Jos inferiorista rauhasta ei voida paikallistaa, voidaan tehdä kaulan tymeektomia, jossa nostetaan niin paljon kateenkorvan kudosta yläviistoon mediastinumista kuin voidaan turvallisesti tehdä.
Superioriset lisäkilpirauhaset ovat tavallisesti dorsaalisesti kilpirauhasen kahden ylemmän kolmanneksen yläpuolella. Toisinaan nämä rauhaset ovat ylempien kilpirauhassuonten vieressä. Muita sijainteja ovat kaulavaltimon tuppeen tai ruokatorven tai nielun taakse (retroesofageaalinen). Lopuksi sekä ylemmät että alemmat lisäkilpirauhaset voivat sijaita poikkeavasti kilpirauhasen kapselissa. Jotkut kirurgit tekevät kilpirauhasleikkauksen puuttuvan poikkeavan rauhasen puolelta sen jälkeen, kun edellä mainituista paikoista on tehty perusteellinen etsintä. Median sternotomiaa ei yleensä pitäisi tehdä kaulan alkututkimuksen yhteydessä hyperparatyreoosin vuoksi.
Epänormaalisti suurentuneet rauhaset poistetaan sen jälkeen, kun muiden rauhasten normaali koko on varmistettu. Poistamisen aikana on tärkeää välttää epänormaalin rauhasen kapselin repeämistä, koska siihen voi liittyä lisäkilpirauhassolujen istuttaminen leikkausalueelle ja myöhempi paratyromatoosi. Kokeneet kirurgit voivat tunnistaa lisäkilpirauhaset ulkonäön ja sijainnin perusteella. Tarvittaessa lisäkilpirauhasten tunnistaminen on varmistettava histologisesti pakastetutkimuksella. Tapauksissa, joissa tehdään totaalinen paratyroidektomia, johon liittyy autotransplantaatio, lisäkilpirauhaskudosta olisi kryosäilytettävä tulevaa autotransplantaatiota varten siltä varalta, että alkuperäinen transplantaatio ei toimi asianmukaisesti.
Suuntautuneen paratyroidektomian tekniikka
Toimintatekniikka on monessa suhteessa samanlainen kuin edellä kuvatussa täydellisessä lisäkilpirauhasten tähystyksessä. Jäljempänä mainitaan eroja.
Poikkeavan rauhasen riittävä kuvantaminen ennen leikkausta on välttämätöntä. Lisäksi olisi vahvistettava järjestelyt lisäkilpirauhashormonin intraoperatiivista mittausta varten. Perifeerisen laskimoveren näytteenottolinja on perustettava. Usein distaalinen vena saphenus tarjoaa kätevimmän pääsyn.
Jotkut kirurgit muuttavat leikkaushaavan sijaintia adenooman preoperatiivisen sijainnin perusteella. Tämä kirjoittaja suosii pientä viiltoa (eli ~2 cm) kaulusviillon vakiopaikassa. Tätä viiltoa voidaan helposti laajentaa, jos laaja tutkimus osoittautuu tarpeelliseksi.
Lisäkilpirauhashormonipitoisuus otetaan välittömästi ennen ihon viiltoa. Kun adenooma on tunnistettu ja leikattu, otetaan leikkausta edeltävä taso. Rauhasen manipulointi aiheuttaa toisinaan merkittäviä, joskus yli kymmenkertaisia nousuja lisäkilpirauhashormonitasossa. Rauhasen poiston jälkeen lisäkilpirauhashormonitasot mitataan 5 minuuttia ja 10 minuuttia leikkauksen jälkeen. Riittävän poiston kriteerit ovat joko 50 prosentin lasku lisäkilpirauhashormonipitoisuudessa lähtötasosta 10 minuutin kuluttua poistosta mitattuun tasoon tai 50 prosentin lasku lisäkilpirauhashormonipitoisuudessa 10 minuutin kuluttua poistoa edeltävästä tasosta ja poiston jälkeinen taso alle lähtötason.
Viilto voidaan sulkea viimeisten lisäkilpirauhashormonitasojen käsittelyn ajaksi, mutta potilaan on pysyttävä anestesiassa ja steriiliä kenttää on ylläpidettävä, kunnes lisäkilpirauhashormonimääritystulokset ovat tiedossa.
Jos suunnattu lisäkilpirauhasen poistoleikkaus onnistuu onnistuneesti, useimmat näistä potilaista voidaan turvallisesti kotiuttaa leikkauspäivänä.
Komplikaatiot ja postoperatiivinen hoito
Kokonaisen lisäkilpirauhasen tähystyksen yhteydessä postoperatiivinen hypoparatyroidismi ja hypokalsemia ovat huolenaiheita, mutta ne ovat erittäin harvinaisia suunnatun paratyroidektomian ja rajoitetun kaulan tähystyksen jälkeen. Hypokalsemia on yleisempää molemminpuolisen lisäkilpirauhasen tähystyksen jälkeen, erityisesti silloin, kun tehdään subtotaalinen paratyroidektomia. Seerumin kalsiumin alimmillaan se on yleensä 24-72 tuntia leikkauksen jälkeen. Monille potilaille tulee hypokalsemia, mutta vain harvat potilaat oireilevat. Toisaalta jopa silloin, kun on tehty rajoitettu tähystys, lieviä hypokalsemian oireita voi esiintyä paratyroidektomian jälkeisinä ensimmäisinä päivinä ilman todennettavissa olevaa hypokalsemiaa. Tämän vuoksi jotkut lääkärit antavat rutiininomaisesti suun kautta otettavia kalsiumvalmisteita postoperatiivisesti.
Hypokalsemia lisäkilpirauhasleikkauksen jälkeen voi johtua nälkäisen luun oireyhtymästä, jossa kalsium ja fosfori laskeutuvat nopeasti luuhun. Tälle on ominaista hypoparatyreoosi ja ohimenevä, mutta toisinaan vakava hypokalsemia, kunnes normaalit rauhaset saavat herkkyytensä takaisin.
Jos hypoparatyreoosi jatkuu, tarvitaan suun kautta annettavaa kalsium- ja D-vitamiinilisää. Kalsiumsitraattia tai kalsiumkarbonaattia voidaan aloittaa 400-600 mg alkuainekalsiumia neljä kertaa päivässä. Jotkut potilaat tarvitsevat huomattavasti enemmän. Kalsitriolin käyttö aloitetaan 0,5 mcg:lla kahdesti päivässä ja sitä lisätään tarpeen mukaan. Potilaiden, joille tehdään totaalinen paratyroidektomia ja autotransplantaatio, voidaan olettaa tarvitsevan tilapäistä kalsiumlisää.
Jos takautuva kurkunpään hermo leikataan paratyroidektomian aikana, välitön korjaus on aiheellista. Jos rekurrenssihermon ei tiedetä loukkaantuneen intraoperatiivisesti, mutta toimintahäiriö viittaa siihen, koska potilaalle on ilmaantunut uutta käheyttä, aluksi valitaan odottava hoito, koska useimmat potilaat toipuvat hermon toiminnasta muutamassa viikossa tai kuukaudessa. Laryngoskopia on aiheellinen sekä toimintahäiriön että toiminnan palautumisen dokumentoimiseksi.
Potentiaalinen henkeä uhkaava hätätilanne leikkauksen jälkeisenä aikana on laajenevan hematooman kehittyminen pretrakeaaliseen tilaan. Tämä komplikaatio on tunnistettava ja hoidettava välittömästi avaamalla haava ja poistamalla hematooma. Hoitamattomana kurkunpään turvotus voi edetä nopeasti ja aiheuttaa hengitysteiden tukkeutumisen. Lisäksi turvotus voi estää endotrakeaalisen intubaation, ja haavan avaamisen tulisi edeltää intubaatioyritystä.
Useimmat pienet hematoomat eivät vaadi hoitoa. Subplatysmaalinen nestekertymä voi joskus muodostua, ja nämä hoidetaan yleensä asianmukaisesti yhdellä imulla. Muutamissa tapauksissa aspiraatio saatetaan joutua toistamaan. Harvoin voidaan joutua asettamaan dreeni toistuvien nestekertymien vuoksi.
Hoitotulokset
Primäärisen hyperparatyreoosin leikkauksen jälkeiset paranemisprosentit ovat asiantuntijoiden käsissä erittäin korkeat, noin 97-98 %. Parannus määritellään yleensä seerumin kalsiumin normalisoitumisena. Lisäkilpirauhashormonipitoisuudet voivat kuitenkin olla koholla leikkauksen jälkeen jopa 20-40 prosentilla potilaista. Jos seerumin kalsiumpitoisuus pysyy viitealueella, tämä kohonnut tila ei yleensä viittaa pysyvään tautiin, mutta se voi merkitä suurempaa uusiutumisriskiä. Monilla primaarista hyperparatyreoosia sairastavilla potilailla on D-vitamiinin puutos, ja korvaaminen voi korjata kohonneen lisäkilpirauhashormonipitoisuuden. On myös jonkin verran heikkoa näyttöä siitä, että kalsiumlisän antaminen voi vähentää lisäkilpirauhashormonin yksittäistä kohoamista paratyroidektomian jälkeen.
Elämänlaadun on toistuvasti osoitettu paranevan paratyroidektomian jälkeen. Huomionarvoista on, että elämänlaadun on todettu parantuneen mitattavasti myös ”oireettomilla” potilailla, mikä korostaa sitä tosiasiaa, että jotkin lievät oireet saattavat jäädä potilailta ja lääkäreiltä huomaamatta.
Seuranta
Potilaat nähdään 1-2 viikkoa leikkauksen jälkeen, ja seerumin kalsium-, 25-hydroksivitamiini-D- ja lisäkilpirauhashormonipitoisuudet määritetään. D-vitamiinin puute on erityisen yleistä potilailla, joilla on hyperparatyreoosi. Monet lääkärit lisäävät rutiininomaisesti kalsium- ja D-vitamiinilisää postoperatiivisesti luukadon palauttamiseksi ja puutteellisen ravinnonsaannin täydentämiseksi.
Analyysit ovat osoittaneet, että onnistuneen paratyroidektomian jälkeinen uusiutumisprosentti on pitkäaikaisseurannassa noin 10 – 15 %, mikä on paljon korkeampi kuin aiemmin on ajateltu. Siksi suositellaan pitkäaikaista seurantaa, jossa kalsium ja lisäkilpirauhashormoni määritetään vuosittain.